Лечение на деца със стероиди
Внадбъбречната корамогат да се разграничат три функционални зони. Най-външната зона произвежда алдостерон, минералкортикоиден стероид, който регулира баланса на натрий и извънклетъчната течност чрез увеличаване на реабсорбцията на натрий от бъбречните тубули и други части на тялото в замяна на калий и водород. Секрецията на алдостерон се стимулира главно от ренин, ангиотензин и в по-малка степен от повишен калий или намален натрий в кръвта.
Средната зонана надбъбречната корасекретира глюкокортикоиди, главно кортизол, който е основният секреционен продукт на надбъбречната кора като цяло. Глюкокортикоидите защитават тялото по време на стресови ситуации, очевидно чрез подпомагане на съдовия отговор към катехоламините, както и чрез повишаване на нивата на кръвната захар, засилване на протеиновия катаболизъм и регулиране на скоростта на гломерулна филтрация и по този начин отделянето на вода.
Секрецията наглюкокортикоиди, от своя страна, се контролира главно от хипофизния ACTH. Най-вътрешната зона на надбъбречната кора синтезира предшествениците на половите хормони, които определят окосмяването като вторична полова характеристика, но имат малък ефект върху сексуалната функция. Секрецията на полови стероиди се регулира от предполагаем, но все още неизолиран хипофизен фактор, надбъбречен андроген-стимулиращ хормон или вероятно ACTH.
Естественитеглюкокортикоидиимат по-слабо изразен минералкортикоиден ефект, а минералкортикоидите могат да имат глюкокортикоидни свойства, но те обикновено се класифицират според основния физиологичен ефект. Тези хормони не действат моментално, тъй като са стероиди, чийто механизъм на действие е бавното индуциране на ензими след директновзаимодействия с клетъчната ДНК, а не с бързодействащите рецептори на клетъчната повърхност, които активират cAMP.
Много естествени и синтетични кортикостероиди сега се използват широко вмедицината. Те се използват като физиологични заместители на ендогенния кортизол, когато последният е дефицитен (напр. при болест на Адисон, адреногенитален синдром), и често във фармакологични дози поради техните противовъзпалителни свойства. Дългосрочната физиологична заместителна терапия с тези лекарства обикновено не предизвиква странични ефекти.
В същото време лечениетона деца с фармакологични дозиза алергии, възпаление или злокачествено заболяване често инхибира растежа и причинява развитието на кушингоидни характеристики и също е придружено от такива добре известни странични ефекти като остеопороза, пептични язви, хипокалциемия, мозъчен псевдотумор, намалена устойчивост към инфекции, диабет, оток, артериална хипертония, миопатия, промени в настроението, катаракта, повишена интра очно налягане и други офталмологични усложнения.
Във фармакологични дозиглюкокортикоидитедиректно инхибират стимулираното производство на ACTH от хипофизната жлеза и следователно могат да причинят атрофия на надбъбречната кора, тежестта на която е пропорционална на активността на кортикостероида и продължителността на приложението му.
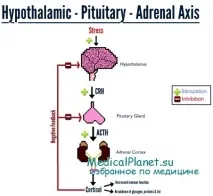
Когато се изисква бързо действие,кортизолъте лекарството на избор. Единична доза кортикостероид, включително голяма, обикновено е безвредна и дори лечението с високи (но не екстремни) дози за няколко дни е малко вероятно да има неблагоприятен ефект при липса на специфични усложнения. Въпреки това, ако кортикостероидната терапия е продължителна или превишаваеквивалентно на обикновена подмяна, честотата на усложнения и потенциално смъртоносни последици нараства пропорционално.
Съответно, внезапното прекъсване на дългосрочно лечение с високи дозикортикостероидие изпълнено с животозастрашаваща надбъбречна недостатъчност, така че такова лечение и неговото прекратяване трябва периодично да се коригира в зависимост от стадия и активността на това заболяване. В повечето случаи "еквивалентните дози" на надбъбречните стероиди се определят въз основа на техните противовъзпалителни и други неендокринни ефекти при възрастни. В същото време, по отношение на деца, за които физиологичният растеж, често използваните стероидни препарати могат да имат по-активен ефект от необходимото.
Така, например, противовъзпалителната активност на преднизона е 4 пъти по-висока откортизола, но в същото време преднизонът инхибира растежа 8 пъти по-силно от кортизола.
Физиологична стероидна заместителна терапия
Поддържаща стероидна терапия. Нормално надбъбречните жлези отделят 12 ± 3 mg кортизол на 1 m2 телесна повърхност на ден. Като се има предвид непълната абсорбция в стомашно-чревния тракт, дозата на лекарствата, приемани перорално, трябва да бъде 2 пъти повече, т.е. 25 mg / m2 / ден. Краткодействащите стероиди (напр. таблетки кортизон ацетат) трябва да се дават на разделени дози, поне два пъти на ден. Дневната доза от лекарства с продължително действие (например преднизон, дексаметазон) може да бъде разделена на 2 дози.
Стрес със стероиди. При условия на стрес, като например телесна температура над 38 ° C, анестезия, секрецията на кортизол обикновено се увеличава 3-5 пъти в сравнение с нормата; съответно най-малко 3 пъти е необходимо да се увеличи дозата на екзогенния стероид (т.е. 45 mg / m2 / ден парентерално или 75 mg / m2 / денперорално) по време на периоди на остър стрес. При надбъбречна криза трябва да се приложи интравенозен хидрокортизон натриев сукцинат (Solu-Cortef), както е посочено по-долу.
Подготовка за операция със стероиди. 36-48 часа преди операцията и след това на всеки 12 часа трябва да се приложи интрамускулно "стресова" доза кортизон ацетат (45 mg/m2), така че по време на операцията да има максимален ефект, състоящ се от 18-часов пик на активност и 48-72-часова продължителност на лекарството. Или, по време на въвеждането в анестезия, можете да инжектирате интравенозно доза „стрес“ (45 mg / m2) хидрокортизон натриев сукцинат и да влеете 100 mg / m2 / ден повече капково. Дозата "стрес" трябва да се поддържа 2-3 дни след операцията и след това да се върне към поддържаща терапия.
Фармакологична употреба на стероиди. При липса на общоприети схеми за фармакологично приложение на стероиди при хронични възпалителни заболявания, предлагаме следните емпирични препоръки: преднизон или иреднизолон 1–2 mg/kg/ден в 2–4 разделени дози; дексаметазон 0,1-0,2 mg/kg/ден в 2-4 приема. По време на вирусни инфекции дозата трябва да се намали до "стресови" нива. Преди продължително лечение с фармакологични дози кортикостероиди трябва да се направят туберкулинови кожни проби.
Оттегляне на кортикостероиди. Ако пациентът е бил лекуван със „стрес“ или фармакологични дози глюкокортикоиди повече от 14 дни, последните трябва да бъдат прекратени постепенно. Дозата трябва да се намалява наполовина на всеки 3-4 дни, докато се достигне заместващото физиологично ниво (25 mg/m2/ден перорално). След това дозата се намалява наполовина на всеки 2 седмици, еквивалентно на 5 mg кортизол седмично. Всеки пациент, който е получил фармакологична доза глюкокортикоиди за повече от 14 дни, трябва да вземе „стрес“ през следващата година по време на стрес.доза (75 mg/m2/ден перорално) кортизол или негов еквивалент.
Като се има предвид трудността напостепеннооттегляне на фармакологичните дози преднизон и дексаметазон съгласно предложената схема, по-лесно е първо да отмените тези лекарства, като ги замените с еквивалентна доза кортизон ацетат, приемана перорално 2-3 пъти на ден, и след това постепенно да намалите дозата на последния.
По време на периода на спиране настероидие важно да не пропускате симптомите на надбъбречна недостатъчност (слабост, мускулна болка, шум в ушите, хипогликемия, артериална хипотония) и, ако се появят, увеличете дозата и след това я намалете по-бавно.