3 Киселинно-алкални свойства на аминокиселините
4. Ароматни - фенилаланин, тирозин, триптофан:

5. С анионообразуващи групи в страничните вериги - аспарагинова и глутаминова киселини:

6. и амиди на аспарагиновата и глутаминовата киселини - аспарагин, глутамин.
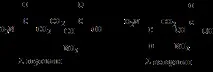
7. Основните са аргинин, хистидин, лизин.

Вторият тип класификация се основава на полярността на R групите на аминокиселините. Разграничете полярните и неполярните аминокиселини. Неполярните радикали имат неполярни C-C, C-H връзки, има осем такива аминокиселини: аланин, валин, левцин, изолевцин, метионин, фенилаланин, триптофан, пролин.
Всички други аминокиселини са полярни (R-групата има полярни C–O, C–N, –OH, S–H връзки). Колкото повече аминокиселини с полярни групи има в един протеин, толкова по-висока е неговата реактивност. Функциите на протеина до голяма степен зависят от реактивността. Ензимите се характеризират с особено голям брой полярни групи. Обратно, има много малко от тях в такъв протеин като кератин (коса, нокти).
Аминокиселините също се класифицират въз основа на йонните свойства на R-групите (Таблица 1). Киселинни (при pH = 7, R-групата може да носи отрицателен заряд) са аспарагиновата, глутаминовата киселина, цистеинът и тирозинът. Основните (при pH = 7, R-групата може да носи положителен заряд) са аргинин, лизин, хистидин. Всички други аминокиселини са неутрални (R групата е незаредена).
Таблица 1 - Класификация на аминокиселините въз основа на полярността на R-групите.
Аминокиселини
Приети еднобуквени обозначения и символи
Изоелектрична точка, pI
символ
Български.
2. Полярни, незаредени R-групи
3. Отрицателно заредени R-групи
4. Положително заредени R-групи
Хистидин
Според броя на амино и карбоксилни групиаминокиселините са разделени на моноаминомонокарбоксилни, съдържащи по една карбоксилна и аминова група; моноаминодикарбоксилна (две карбоксилни и една аминова група); диаминомонокарбоксилна (две аминогрупи и една карбоксилна група).
Според способността да се синтезират в организма на човека и животните, всички аминокиселини се делят на незаменими, незаменими и частично незаменими.
Незаменимите аминокиселини не могат да се синтезират в организма на човека и животните, те трябва да се доставят с храната. Съществуват осем абсолютно незаменими аминокиселини: валин, левцин, изолевцин, треонин, триптофан, метионин, лизин, фенилаланин.
Частично есенциални - синтезирани в тялото, но в недостатъчни количества, така че те трябва да идват частично от храната. Тези аминокиселини са арганин, хистидин, тирозин.
Неесенциалните аминокиселини се синтезират в човешкото тяло в достатъчни количества от други съединения. Растенията могат да синтезират всички аминокиселини.
1.3 Киселинно-алкални свойства на аминокиселините
Киселинно-базовите свойства на аминокиселините са свързани с наличието в тяхната структура на две йонизиращи се групи - карбоксилни и аминогрупи, следователно аминокиселините могат да проявяват свойствата както на киселини, така и на основи, т.е. те са амфотерни съединения. В кристално състояние и във водни разтвори, а-аминокиселините съществуват като биполярни йони, наричани още цвитериони. Йонната структура причинява някои характеристики на свойствата на а-аминокиселините: висока точка на топене (200-300 ° C), нелетливост, разтворимост във вода и неразтворимост в неполярни органични разтворители. Разтворимостта на аминокиселините във вода е свързана с тяхното усвояване и транспортиране в тялото. Йонизацията на молекулите на аминокиселините зависи от рН на разтвора. За моноаминомонокарбоксилниПроцесът на киселинна дисоциация има следната форма:

В силно киселинни разтвори аминокиселините присъстват като положителни йони, докато в алкални разтвори те присъстват като отрицателни йони.
Киселинно-алкалните свойства на аминокиселините могат да бъдат обяснени въз основа на теорията на Брьонстед-Лоури за киселините и основите. Напълно протонирана а-аминокиселина (катионна форма) от гледна точка на теорията на Brönsted е двуосновна киселина, съдържаща две киселинни групи: недисоциирана карбоксилна група (-COOH) и протонирана аминогрупа (NH3), които се характеризират със съответните стойности pKa1 и pKa2.
Стойностите на pKa за аминокиселини се определят от кривите на титруване. Помислете за кривата на титруване на аланин (фиг. 1).

Ориз. 1 – криви, получени при титруване на 0,1 М разтвор на аланин с 0,1 М разтвор на HCl (а) и 0,1 М разтвор на NaOH (б).
От кривата на титруване на аланин следва, че карбоксилната група има pKa1 = 2,34, а протонираната аминогрупа pKa2 = 9,69. При pH = 6,02 аланинът съществува като биполярен йон, когато общият електрически заряд на частицата е 0. При тази стойност на pH молекулата на аланин е електрически неутрална. Тази стойност на pH се нарича изоелектрична точка и се обозначава като pHiet или pI. За моноаминомонокарбоксилните киселини изоелектричната точка се изчислява като средноаритметично от две стойности на pKa. Например за аланин е равно на:
pI = ½ × (pKa1 + pKa2) = ½ × (2,34 + 9,69) = 6,02
При стойност на pH, надвишаваща изоелектричната точка, аминокиселината е отрицателно заредена, а при стойност на pH под pI, аминокиселината носи нетен положителен заряд. Например при pH = 1,0 всички молекули на аланин съществуват под формата на йони