Двигател на болестта на Алцхаймер - тау протеин
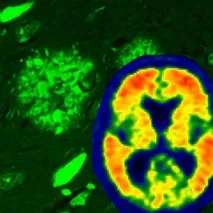
Мозъчната патология приболестта на Алцхаймер се открива чрез тиофлавин-S флуоресцентна микроскопия, показваща както неврофибриларни възли (структури, подобни на пламък), така и амилоидни плаки (кръгли структури). Сканирането на мозъка може да визуализира натрупването наамилоид в мозъците на живи индивиди (по-топлите цветове показват амилоид). (Снимка: Mayo Clinic)
След изследване на повече от 3600 проби от мозъчна тъкан след смъртта, учените от клиниката Mayo в Джаксънвил, Флорида и Рочестър, Минесота заключиха, че прогресивният когнитивен спад и загубата на памет, които са характерни за пациенти сболестта на Алцхаймер, са причинени от неизправност натау протеина.Амилоид, друг токсичен протеин, характерен заБолестта на Алцхаймер, се натрупва с напредването на болестта, но не е основният виновник за нейното развитие.
В допълнение, според изследователите, техните данни показват, че нова посока в лечението на болестта на Алцхаймер трябва да бъде блокиране на действието на токсичнияtau.
„През последните 25 години по-голямата част от изследванията на Алцхаймер наистина се фокусираха върху амилоида,” продължава д-р Морей. „Първоначално беше установено, че пациентите, които носят мутации или промени в амилоидния ген, имат тежка форма на патология на Алцхаймер - по-специално, повишени нива на амилоид. Сканирането на мозъка през последното десетилетие показа, че амилоидът се натрупва с остаряването и следователно повечето модели на болестта на Алцхаймер се основават на токсичността на този протеин. По този начин полето на изследване на болестта на Алцхаймер беше стеснено.
Учените от клиниката Майо успяха да видятвърху еволюцията както на амилоида, така и на тау протеина
„Представете си, че гледате пръстените на едно дърво. Чрез изучаване на напречното му сечение можете да идентифицирате модели като смяната на сезоните и стареенето на дървото“, казва д-р Mörey. „Изучаването на мозъчни проби в различни стадии на болестта на Алцхаймер ни дава представа за въздействието на различните степени на тежест както на амилоида, така и на тау патологията върху когнитивната функция и ние сме много щастливи, че успяхме да използваме ресурса на банката на Mayo Clinic, на която хиляди хора са дарили мозъците си посмъртно. Това ни позволи да разберем промените в тау и амилоида с течение на времето.
„Тау може да се сравни с траверси, които стабилизират железопътната линия, която мозъчните клетки използват за транспортиране на храна, съобщения и други жизненоважни товари в неврона“, обяснява д-р Морей. „При болестта на Алцхаймер промените в тау водят до нестабилност на тези пътища в невроните в хипокампуса, центъра на паметта. Анормален тау се натрупва в невроните, което в крайна сметка води до тяхната смърт. Има доказателства, че анормалният тау след това се разпространява от клетка на клетка, разпространявайки се в мозъчната кора. Кортексът е външната част на мозъка, участваща в по-високи нива на мислене, планиране, поведение и внимание, отразявайки по-късни промени в поведението на пациенти с Алцхаймер. Амилоидът, за разлика от тау, започва да се натрупва във външния кортекс и след това се разпространява в хипокампуса и евентуално в други области. Нашето проучване показва, че натрупването на амилоид е ясно свързано с когнитивен спад. Въпреки това, ако се вземе предвид тежестта на тау патологията, връзката между амилоида и умствените способности изчезва, което предполагаче тау протеинът е двигател на болестта на Алцхаймер.
Амилоидното изображение в мозъка се използва само от около десетилетие и "все още има много въпроси без отговор днес за това какво открива", добавя Mörey. „Изучаването на това каква мозъчна патология е в основата на прага за болестта на Алцхаймер чрез сканиране на мозъка с амилоидни отлагания е възможно само при пациенти, които са били сканирани и са дарили мозъка си за изследване.“
Изследването е проведено на два етапа. Учени от клиниката Майо във Флорида са изследвали 3618 мозъчни проби от нейната банка, от които 1375 са от пациенти с потвърдена болест на Алцхаймер. Тези пациенти с различна степен на деменция са починали на различна възраст, което дава възможност да се оцени заболяването в неговото развитие.
Изследователите са използвали препоръчани системи за оценяване, за да проучат еволюцията на амилоида и тау в секциите на мозъчната тъкан. Те откриха, че възрастта, на която се появява когнитивен спад, продължителността на заболяването и умственото увреждане се определят от тежестта натау патологията, но не и от тежестта на патологията, свързана с амилоид.
Втората част от изследването е проведена в сътрудничество с техните колеги от Рочестър. Заедно учените проучиха и сравниха предсмъртни мозъчни сканирания на пациенти с амилоидни отлагания, за да оценят амилоидната и тау патологията.
Изследователите откриха, че сигналът от тези сканирания корелира с мозъчна амилоидна патология, а не с съдов амилоид, и не корелира с тау патология. В мозъците на някои участници в проучването се наблюдава отлагане на амилоид, характерно за патология, която не достига прага, установен при сканиране на пациенти сБолест на Алцхаймер. Това е важно, тъй като амилоидът може да бъде открит в мозъците на възрастни хора, които нямат когнитивен спад, казаха изследователите.
„Нашите резултати показват, че по отношение на терапията трябва да се съсредоточим върху тау. Те обаче още веднъж потвърждават, че методът на мозъчно сканиране, използван днес за оценка на нивото на амилоид, е ценен за проследяване на развитието на болестта на Алцхаймер“, обобщава д-р Mörey. „Докато тау беше„ победителят “в нашето проучване, вярно е също, че амилоидните мозъчни сканирания могат да се използват, за да се потвърди, че при пациенти, включени в клинични изпитвания, амилоидният праг съответства на болестта на Алцхаймер - вместо маркера тау.“