Натриев йодид Калиев йодид
Фармакопейни препарати от йодиди са
Natrii iodidum Nal М. м. 149.89
Калиев йодид Kalii iodidum KI М. м. 166.01
И двете лекарства са бели кристални прахове.
Йодидите се използват като носители на йод при хипертиреоидизъм,
Ако храната или водата не съдържат достатъчно йод, както се случва в някои планински райони, тогава местното население развива заболяване - кретинизъм или гуша. Задайте йодиди под формата на разтвори (отвари)' за перорално приложение.
Методи за получаване на халогениди. Натриевият хлорид е единственият от халогенидите, който е широко разпространен в природата под формата на масивни находища на каменна сол. Той е основният източник за получаване на фармакопейния препарат. Водните солеви разтвори се изпаряват, след което натриевият хлорид се подлага на пречистване от примесите, които го придружават. В крайна сметка натриевият хлорид се прекристализира от вода, наситена с концентрирана солна киселина, в която е слабо разтворим.
По-чист препарат може да се получи чрез третиране с натриев карбонат или калиев х. включително солна киселина.
Съпътстващият продукт на реакцията (CO2) е летлив и следователно натриевите (калиевите) хлориди са чисти.
Бромидите и йодидите се получават по абсолютно същия начин. В промишлеността те се получават по следния начин: железните стружки се обработват с вода и се добавя съответно бром или йод. В този случай се образува железен бромид (йодид) (FeBr2 или Fel2). След това към реакционната маса отново се добавя Br,(I,).
След това се изпарява разтвор на бромид (йодид) железен оксид и се добавя разтвор на натриев карбонат.
Утайките от железни хидроксиди се отфилтруват. Кристализира от филтрата след изпаряване.натриев бромид или съответно натриев йодид.
За да се получи калиев бромид и калиев йодид, вместо сода се взема поташ K2CO3.
Автентичността на всички тези лекарства (хлориди, бромиди, йодиди) се определя от Na + и K + катиони и от съответния C1 анион
Натриевият йон обикновено се открива по жълтия цвят на пламъка. От химичните реакции HF X води до реакция с цинккуранил ацетат - в присъствието на Na + се отделя жълта кристална утайка.
Тази реакция може да се счита за специфична за Na* йона, тъй като повечето от катионите не пречат на нейното осъществяване.
Калиевият йон се идентифицира по цвета на пламъка на горелката в лилаво, а когато се гледа през синьото стъкло, пламъкът изглежда оцветен в лилаво-червено.
От използваните химични реакции:
а) реакция с винена киселина в присъствието на натриев ацетат.
За да се избегне разтварянето на утайката от калиев хидротартарат в образуваната минерална киселина (НС1), тя се свързва с натриев ацетат;
б) реакция с разтвор на натриев кобалтинитрит (хексанит-
Реакцията се провежда в среда с оцетна киселина чрез триене на пръчица по стените на съда.
Тази реакция може да открие калиев йон само в отсъствието на NH4 + -hohob, който също се утаява с този реагент. Следователно, преди да се изследват калиеви соли чрез тази реакция, те трябва да бъдат калцинирани, за да се отстранят възможните примеси на амониеви соли.
Всички горепосочени реакции се препоръчват от GF X.
За потвърждаване на автентичността на аниони C1 - , Br
, I - GF X води до две основни реакции:
а) реакция с разтвор на сребърен нитрат в присъствието на азотна киселина; когато хлоридите, бромидите, йодидите се третират с разтвор на сребърен нитрат в присъствието на азотна киселина, се образуват сиренести утайки,съответно:
Реакцията се провежда в присъствието на азотна киселина, която не разтваря утайките от сребърен халогенид.
Тъй като сребърните хлориди и бромиди понякога са трудни за разграничаване по цвят, се препоръчва да се тества разтворимостта на тези утайки в разтвори на амоняк и амониев карбонат.
Сребърният хлорид лесно се разтваря в разредени разтвори на амоняк и амониев карбонат, за да образува съответните разтворими комплекси.
Сребърният бромид е трудно разтворим в разредени разтвори на амоняк и се разтваря само в концентрирани разтвори, докато изобщо не се разтваря в разтвор на (rW^rCO3).
Сребърният йодид не се разтваря нито в амонячни разтвори, нито в разтвор (MHN-CO3.
б) реакция на окисление на халогенидни йони (C1
, I -) до елементарен халоген; халидните йони в кисела среда са редуциращи агенти и сами по себе си могат да се окисляват до свободен халоген. Това свойство се използва за определяне на автентичността на бромидите и йодидите.
Към разтвор на бромид или йодид (NaBr, Nal) добавете минерална киселина, като солна киселина, хлороформ и окислител. Обикновено в случай на бромиди се добавя хлорамин като окислител, а в случай на йодиди се добавя натриев нитрит NaN02 или железен хлорид FeCl3. Реакционната маса се разклаща и се оставя да се утаи. Хлороформният слой става жълт (Br2) в случай на бромиди и виолетов в случай на йодиди (12).
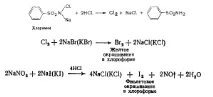
Хлоридите (NaCl, KCI) също се окисляват до свободен хлор, но тъй като хлорът е летлив, тази реакция не е удобна за удостоверяване на хлориди и не се препоръчва от GF X.
Често бромати (NaBrO3) и съответно йодати (NaI03) се използват за отваряне на бромиди и йодиди, които, като окислители, окисляват Br в кисела среда.
предисъответно свободен бром и йод. Реакцията се провежда в присъствието на хлороформ, който става жълт (Br2) и съответно виолетов (b).
Тест за чистота. За натриеви и калиеви хлориди GF X изисква липсата на примеси от магнезиеви, бариеви и амониеви соли.
В натриев хлорид не се допускат примеси на калиеви соли, а в калиев хлорид - натриеви соли, тъй като калият и натрият са антагонисти в действие.
Примеси като калций, желязо, тежки метали, сулфати, арсен, GF X са разрешени в препаратите на натриев и калиев хлорид в границите на стандартите, тъй като допустимата граница на тези примеси не влияе върху терапевтичния ефект на лекарствата и не предизвиква странични ефекти.
В бромидите не се допускат примеси на барий, калций, бромати, йодиди (токсични).
Смесването на разтворими бариеви и калциеви соли се определя чрез добавяне на разредена сярна киселина към разтвора на препарата. В присъствието на Ba 2+ и Ca 2+ разтворът ще стане мътен поради образуването на неразтворими калциеви и бариеви соли (CaSO4 и BaSO-i).
Смесването на йодиди се определя чрез добавяне на окислител, като железен хлорид, към разтвора на препарата.
Когато се добави хлороформ, освободеният йод ще го оцвети в лилаво.
Броматите са най-опасните примеси поради тяхната токсичност. Те могат да бъдат открити в бромидите чрез добавяне на солна киселина. При наличие на примес от бромати ще се отдели свободен бром, който ще оцвети разтвора в жълто.
Примеси от сулфати, тежки метали и арсен са разрешени в бромидите в рамките на стандартите.
Примесите на нитрати се откриват чрез редуцирането им до амоняк, което се установява органолептично или чрез синьо оцветяване на мокра червена лакмусова хартия.
примесцианидът се определя от образуването на пруско синьо.
Реакцията с бромиди протича по подобен начин.
Йодидите не могат да бъдат определени по метода на Мор, тъй като тяхното титруване е придружено от образуване на колоидни системи от сребърен йодид и адсорбция, което затруднява установяването на крайната точка на титруването. Следователно йодидите се определят чрез титруване със сребърен нитрат, като се използват адсорбционни индикатори, които са соли на слаби органични киселини, като динатриева сол на флуоресцеин (I) или натриев еозинат (II).
Тъй като йодидът се титрува със сребърен нитрат, се образува колоидна Agl утайка, чиито частици имат висок адсорбционен капацитет. Положително заредени, те адсорбират отрицателно заредени индикаторни аниони върху повърхността си и в еквивалентната точка предизвикват промяна в цвета на повърхността на Agl утайката от жълто до розово.
Съхранение. Хлоридите, бромидите, йодидите трябва да се съхраняват при условия, които предотвратяват окисляването на тези лекарства: в добре запушени буркани, на сухо място. Йодидите и бромидите обикновено се съхраняват в оранжеви стъклени буркани, тъй като светлината стимулира процеса на окисление.