ТЕРМОДИНАМИКА НА ФАЗОВИТЕ РАВНОВЕСИЯ
Разделът "Термодинамика на фазовите равновесия" е пряко свързан с прогнозирането на състоянието на отделните лекарствени вещества и техните смеси. Теорията на фазовите равновесия позволява да се идентифицират случаи на физикохимична несъвместимост на фармацевтичните препарати. Термодинамичните методи се използват за теоретично описание и практически изчисления на такива широко разпространени процеси на разделяне и пречистване на многокомпонентни смеси като проста дестилация и ректификация, парна дестилация и екстракция. Моделите, изследвани в този раздел, позволяват разумно да се изберат оптималните условия за извършване на изброените процеси, при които се постига най-доброто качество на фармацевтичните продукти.
Фазови равновесия в еднокомпонентни системи. Фазовото правило на Гибс. Уравнения на Клапейрон, Клапейрон - Клаузиус
Основни уравнения
Термодинамична системае тяло или група от тела, които са във взаимодействие и условно изолирани от околната среда.
Една система се наричахомогенна, ако се състои от една фаза. Една система се наричахетерогенна, ако се състои от две или повече фази.
Фазае набор от хомогенни части на системата (т.е. идентични по физични, химични и термодинамични свойства), отделени от другите части на системата чрез физически (действително съществуващ) интерфейс. Отделно вещество в твърдо агрегатно състояние винаги образува независима фаза.
Течните и твърдите фази се наричат кондензирани.
Ако веществото се съдържа едновременно в различни фази, то преминава от една фаза в друга, такъв преход се наричафаза. Състояние, в което скоростите на противоположни фазови преходиса равни, се наричафазово равновесие.
Компоненти(съставни вещества) са всички химически вещества, които могат да бъдат изолирани от системата и да съществуват извън нея.
Броят на степените на свободае броят на интензивните термодинамични параметри, които могат произволно да се променят в определени граници, така че броят и естеството на фазите в системата да не се променят.
Изчисляванетона числото Cв равновесна система в зависимост от броя на компонентитеK, броя на фазитеФи от броя на термодинамичните параметриn, които се различават от химичните потенциали (параметритериТучастват в изчислението) се извършва с помощта нафазовото правило на Гибс(1876):
Ако външните параметриpиTвлияят на системата, тогаваn= 2 и фазовото правило приема формата
Ако само температурата влияе на системата от външни параметри и налягането е постоянно (или обратно), тогава фазовото правило приема формата
Заеднокомпонентни системи, пример за които е система, образувана от вода като компонент,
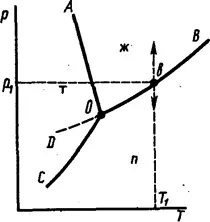
Ориз. 40. Диаграма на състоянието на водата
фазовото правило (135) приема формата
Ако минималният брой степени на свобода (Сmin) е равен на нула (системата е инвариантна), то съгласно (138)Ф= 3. В равновесна еднокомпонентна система могат да съществуват едновременно максимум три фази (m, l, z). Системата има максимален брой степени на свобода (Сmax) приФmin, който не може да бъде по-малък от една. СледователноСmax=1 – 1 + 2 = 2. Тези степени на свобода са налягане и температура.
Надиаграмата на състоянието на водатаима три полета: лед (m), течност (l) и пара (p). В рамките на всяко поле можете свободно да променяте температурата и налягането безпромени в броя на фазите, тъй като приФ= 1 броят на степените на свобода
КривитеAO, VOиСОхарактеризират онези стойностириТ,, при които две фази са в равновесие в системата. Всяка от кривите показва зависимостта на температурата на фазовия преход от външното налягане.
Система, дадена от точка на която и да е крива, емоновариантна, тоест има една степен на свобода (C= 3 - 2 = 1). Следователно или налягането, или температурата могат да се променят произволно. Вторият параметър се променя в зависимост от първия. Например, при избрана температураT1 (фиг. 40), равновесие w p може да съществува само при наляганеp1 (точкаb).Ако налягането се промени произволно приT1, тогава системата ще премине от двуфазна към еднофазна.
ТочкаOна диаграмата съответства на система, в която има три фази (m, w, n). В този случайС= 1 – 3 + 2 = 0 (системата е инвариантна). Системата може да бъде в това състояние приt =0,0076 °C и налягане от 610 Pa. ТочкатаOсе наричатройна точкана водата. Дори малка промяна в един от параметрите нарушава равновесието и води до изчезване на една или две фази.
Уравнението на Клапейрон(1834) свързва налягането, при което се извършва фазовият преход, и температурата на фазовия преход. За процеса на изпаряване на водата в диференциална форма има формата