Хидрогеохимия - 1
1. СВОЙСТВА И СТРУКТУРА НА ВОДАТА
1.1. Аномалия на свойствата на водата
Едва в края на 18 и началото на 19в. разбра какво представлява веществото, наречено вода. Експериментите на Г. Кавендиш, А. Лавоазие, А. Хумболт, Ж.Л. Гей-Люсак доказа, че водата се образува от два обема водород и един обем кислород, т.е. има химична формулаН2Oи молекулно тегло 18. Постепенно обаче става ясно, че по почти всички физикохимични показатели това вещество е уникално, рязко различно от другите природни съединения.
Точки на топене и кипене на водата
Те се основават на приетите температурни референтни системи.
Избор на вода за създаване на температурни скали.
Целзий(1701-44). Скалата по Целзий е 1741.Точките на кипене и топене на водатапри атмосферно налягане са съответно 100 o C и 0 o C,
Ромюр(1683-1757). Скалата на Réaumur от 1730 г. Точката на кипене на водата се приема като 80 o (1 o C \u003d 5/4 o R).
Фаренхайт(1686-1736). Точката на топене на леда се приема като 32 o F, точката на кипене на водата е 180 o F (t o C \u003d 5/9 t o F - 32).
Откриване на периодичния законD.I.Mendeleev(1869). Несъответствието между физичните параметри на водата и периодичния закон.
Несъответствието с периодичния закон може да се види от сравнението на точките на кипене и топене на водородните съединения на елементите от кислородната група. Данните за H2Se са взети от графиката. За водата се вижда, че в съответствие с периодичния закон точката на топене на водата ще бъде около минус 90 °, а точката на кипене - около -70 °. Водата при „нормални“ условия би била токсичен газ с неприятна миризма.Животът на Земята би бил невъзможен.
Благодарение на тезиСъс своите „аномални” свойства водата защитава живота и регулира топлинния и газов режим на нашата планета.
Специфичният топлинен капацитет на водата е най-високият от всички течности. И тук водата се приема като стандарт: за да се загрее 1 g вода с 1 o C, се изразходва 1 калория топлинна енергия (calor - топлина, лат.). За сравнение: гипс - 0,27, суха глина 0,22 кал. (1 кал = 4,187 J.). Специфичният топлинен капацитет на леда и парата е два пъти по-нисък - 0,5 cal / g. град. Скритите топлина на топене и изпаряване на водата също са необичайно големи - 79 и 539 кал. По този начин, за да превърнете 1 g лед с температура 0 ° C в пара, трябва да изразходвате 79 + 100 + 539 = 718 калории топлина. Поради такъв изключително висок топлинен капацитет, водата е основният регулатор на топлинния режим на нашата планета. Влиянието на Световния океан засяга почти всички точки на Земята, дори и най-отдалечените от морския бряг, характеризиращи се с така наречения континентален климат. Големите водни басейни и преди всичко Световният океан са регулатори на топлинния режим на Земята. За почвения слой годишният топлообмен е 1,5-3 kcal / cm 2, например за Балтийско и Черно море 48-52. При липса на водни басейни температурата ще се повиши през лятото и ще падне с няколкостотин градуса през зимата иживотът на Земята би билневъзможен;напротив, ако Земята беше изцяло покрита от океана, годишната амплитуда на въздуха би се променила от 0 на екватора до 5-6 o C на полюсите. Влиянието на океана се простира върху цялата планета, включително полюсите на студа в Антарктида.
Високият топлинен капацитет на водата се свързва с такива показатели католатентна топлина на топенекомпонент 333,7·10 3 J/kg,и латентна топлина на изпарениекомпонент 2258,10 3 J/kg, т.е. Необходима е огромно количество енергия, за да се превърне 1 кг лед в течност и 1 кг течна вода в пара.Това свидетелства за високата енергийна интензивност на водата, което предопределя изключителната й роля на енергиен акумулатор в протичането на природните процеси.
Стойността надиелектрична константаза вода е най-високата от всички течности и е равна на 80,1 при температура от 20 ° C. При температура от около 0 ° C тя е около 82. Това означава, че когато солите се разтварят във вода, силата на електрическото взаимодействие между противоположно заредените частици намалява 80 пъти, в резултат на което солите се дисоциират на йони. Повечето разтворители имат не повече от 50, неполярните течности (бензин, керосин) имат не повече от 3. Това свойство на водата предопределя явлениетоелектролитна дисоциация, т.е. способността на соли, киселини, алкали да се разлагат във водни разтвори на противоположно заредени йони. Водата е инертна като разтворител. Той носи хранителни вещества на живите организми и извежда токсините и няма какво да го замени. Че. и без това свойство на водатаживотът на Земята би билневъзможен.
Водата разтваря минералите, но те се прераждат, ако водата се изпари. Тази характеристика има колосално геоложко и биологично значение, предопределяйки водни цикли от различен порядък, които се извършват за няколко часа (в живите организми) и продължават много милиони години в недрата на Земята (геологични). Очевидно появата на живот на Земята до голяма степен се дължи на това невероятно свойство на водата.
Всички вещества имат максимална плътност при точката на топене, с изключение на водатаМаксималната плътност на водата(1,0 g / cm 3) съответства на температура от 3,98 о; плътност на леда 0,918 g/cm 3 ; само водата не потъва в собствената си стопилка; Талес от Милет обърна внимание на това. Когато водата замръзне, се образува тънък защитен слой лед.осигуряване на опазването на водните тела, преди всичко на Световния океан - основният регулатор на въздушния режим на планетата. И без това свойство на водатаживотът би придобил напълно различни форми.
1.2. Идеи за скритата структура на водата
Структурата на водата.Тридесетте години на ХХ век донесоха ново голямо откритие, свързано с изучаването на водата: английските физици Дж. Бернал и Р. Фаулър, въз основа на рентгенови и спектроскопски изследвания, установиха, че водните молекули са подредени по определен начин, всяка водна молекула е заобиколена от четири други в тетраедър. Така се потвърждава твърдението, направено в края на 18 век. V. Roentgen мисли за сложната структура на течната вода и съществуването на допълнителни връзки между отделните молекули. Учените наричат това явлениеструктурата на водата,въпреки че е ясно, че е невъзможно напълно да се идентифицира с кристалната решетка на твърди вещества, тъй като течната вода е смес от мономерни и полимерни молекули, връзките между отделните мономери са динамични: те постоянно се появяват, разрушават, укрепват, отслабват.
Основната причина за съществуването на структурата на водата е специален вид връзка между отделните атоми - водород. Тази връзка е електростатична по природа, но е по-слаба от нормалната валентна връзка между водородните и кислородните атоми, които образуват отделни мономери. Във всеки H2O мономер разстоянието между водородните и кислородните атоми е 0,1 nm, а ъгълът, образуван между валентните връзки, е около 105º. При водородна връзка разстоянието между атомите се увеличава до 0,176 nm и не е строго постоянно.
Има няколко модела на структурата на водата, базирани на идеята за свързване на отделни мономери чрез водородна връзка. J. Bernal и R. Fowler предполагат съществуванетотри типа разположение на молекулите: а) структури, приближаващи се до кристалната решетка на леда, съществуват при температури от 0 до 4ºС; б) структури като кварца преобладават при температура 4-200ºС; в) плътно опаковани структури, типични за нормалните течности (почти лишени от водородни връзки), се появяват при температури над 200 ºС [Blokh A.M. Структурата на водата и геоложките процеси, Л., 1969, стр. 216].
Интересен подход към тълкуването на структурните характеристики на водата е предложен от италианския физик М. Анджено (1967). Според неговите идеи всяка водна молекула може да участва в не повече от две, но така наречените колективни водородни връзки, в резултат на което комбинацията от валентни и водородни връзки образува звена от различен тип (фиг. 1).
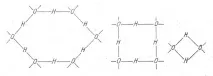
Ориз. 1. Молекулни агрегати в течна вода (по М. Аджендо).
Тези връзки могат да образуват вериги, пръстени и по-сложни системи, които непрекъснато се образуват, разрушават и обменят молекули. В този случай общият брой на водородните мостове в системата остава постоянен и възможните типове агрегати присъстват във водата в различни пропорции в статично равновесие, определено от температурата. Пръстените от шест молекули изглежда се доближават до структурата на леда.
От гледна точка на структурната структура на течната вода са обяснени всички нейни аномални свойства. Необходимостта от разрушаване на водородните връзки предопределя високата енергийна интензивност на водата, в резултат на което точките на топене и кипене, топлинният капацитет и латентните топлина на топене и изпаряване стават необичайно високи. При охлаждане на водата в температурния диапазон от 4 до 0ºС структурата се преструктурира от по-плътна тетрагонална към хексагонална ледена опаковка. Силната връзка между водните молекули я прави инертна за разтваряневещества. Тъй като структурата на водата се формира от електростатични връзки, тя се влияе от различни полета (температурни, геодинамични, магнитни, електрически).
Когато се приложи налягане, молекулите на течностите се приближават една към друга и техният вискозитет се увеличава. Водата се държи съвсем различно. Първите етапи на натоварванията водят до преструктуриране на структурата на водата, запълване на междумолекулни празнини, придружени от намаляване на нейния вискозитет и едва от налягане от около 100 MPa (достатъчно високо за естествени условия) започва постепенно увеличаване на вискозитета.
1.3. Разновидности на водата
Структурните свойства на водата и наличието на няколко изотопа на кислорода и водорода са причината, поради която водата може да образува много физикохимични видове. Ето някои от тях.
Идеи за активирана вода
Експериментите на учените от Новосибирск (F.A. Letnikov и др.) за обработка на вода в автоклави при температури 300-400 ºС и налягане до 100 MPa показаха, че това увеличава способността на водата да разтваря много минерали (до сулфиди, гипс, кварц), pH намалява, електрическата проводимост се увеличава. Влиянието на температурата и налягането върху промяната във водните структури доведе експертите до идеята за възможността за симулиране на свойствата на водата, намираща се на голяма дълбочина (т.е. при високи температури и налягания), и доведе до откриването на така нареченатаактивирана вода. След пречистване на вода в автоклави Откриването на активирано състояние във водата на термалните минерални извори предполага, че лечебните свойства на някои видове минерални води могат да бъдат свързани не само с техния химичен състав, но и с повишаване на биологичната активност на водата, когато се активира. Откриването на феномена на активиране не само прави възможно обяснениетонякои свойства на хидротермалните разтвори, но също така открива перспективи за изкуствено приготвяне на минерални води.
Влияние на електрическото поле
Когато водата се постави велектрично поле, могат да настъпят определени промени в нейната структура. И така, електрическият ток отслабва структурните връзки и след обработката на водата с променлив електрически ток скоростта на изпарение се увеличава, според малкото налични данни, с 11-18%. Отбелязано е влиянието на електрическите полета върху интензивността на поглъщане на светлинните лъчи от водата.
Влияние на магнитното поле
Вода-II.В началото на 60-те години на ХХв. Н.Н. Федякин открива изключително интересно явление: при кондензация на водни пари в тънки кварцови капиляри (5-20 микрона в диаметър) се образува течност, която значително се различава по свойства от обикновената вода. По-късно тази течност, наречена вода-II, е изследвана от видни наши и чуждестранни изследователи, по-специално от голям екип от учени, ръководени от Б.В. Дерягин. Установено е, че вода-II е вискозна течност с плътност около 1 g/cm 3 и коефициент на пречупване 1,49 (срещу 1,33 за обикновена вода). Тази течност преминава в твърдо състояние при охлаждане до минус 35÷40 ºС без скок на обема. Точката на кипене на вода-II при атмосферно налягане е приблизително 250 ºС. Water-II има уникален инфрачервен абсорбционен спектър, който не съответства на нито едно от известните вещества. Модифицираното състояние на полученото вещество е стабилно и се запазва по време на дестилацията (тази процедура е използвана за огрубяване на порции вода-II). Доказано е, че новополученото вещество стриктно отговаря на формулата H2O; кварцът, очевидно, играе ролята на катализатор в синтеза на вода-II.
Водни изследвания-IIръководи Б.В. Дерягин и неговите сътрудници стигнаха до извода за възможността за съществуването на специален тип силна молекулярна връзка между водород и кислород, която образува полимери, състоящи се от 6-10 мономерни молекули H2O. Все още е трудно да се определи ролята на вода-II в природните системи, но е ясно, че нейното изследване обещава определени перспективи в изследването на дълбоки геоложки процеси.
Тежка вода.Понастоящем са известни три изотопа на водорода (1Н-протиум, 2Н-деутерий D, 3Н-тритий Т) и три изотопа на кислорода (16О, 17О, 18О). Това означава, че може да има значителен брой разновидности на водата с различни изотопни комбинации. Най-стабилният от тях е така наречената тежка вода D2O, съдържаща се като примес в обикновената вода в стотни от процента. По своите свойства тежката вода се различава значително от обикновената вода: максималната плътност се отбелязва при t=11,2 ºС и е 1,056 g/cm 3 ; вискозитетът е с 20% по-висок; диелектричната константа е с 0,3-0,5% по-ниска. Точката на топене на тежката вода е 3,8 ºС; точка на кипене 101,4 ºС. Съдейки по дадените данни и редица други данни, деутериевата връзка е дори по-здрава от водородната.Тежката вода се използва като забавител на неутрони в ядрените реактори. Тежката вода е токсична, в нея умират живи същества и растения. Някои учени свързват еволюцията на живота на нашата планета с промените в концентрацията на деутерий във водата: по-специално, по-ниската концентрация на деутерий във водата в сравнение със съвременната концентрация на деутерий във водата обяснява съществуването на гигантски тревопасни животни в мезозоя. Тези разпоредби обаче са противоречиви.
Дадените тук примери за разновидности на водата, предопределени от нейната сложна структура и изотопия, показват колко неизчерпаеми са перспективите за появата на нови открития приизследването на такова невероятно вещество като водата.