Хлорофил - MEL химия
Защо растенията са зелени?

Направете този експеримент у дома

Този експеримент е включен в комплекта "Растителна химия" заедно с "Обезцветяване" и "Антоцианини". Регистрирайте се и вземете всичко необходимо, за да проведете този експеримент у дома.
Безопасност
- Преди да започнете експеримента, поставете защитни ръкавици и очила.
- Направете опита върху поднос.
- Провеждайте експеримента в добре проветриво помещение, далеч от източници на запалване.
- Ако реактивите попаднат в очите, изплакнете ги обилно с вода, като ги държите отворени, ако е необходимо. Незабавно потърсете медицинска помощ.
- При поглъщане изплакнете устата с вода, изпийте малко чиста вода. Не предизвиквайте повръщане. Незабавно потърсете медицинска помощ.
- В случай на вдишване на реактиви, изведете пострадалия на чист въздух.
- В случай на контакт с кожата или изгаряне, промийте засегнатата област обилно с вода в продължение на 10 минути или повече.
- Ако се съмнявате, незабавно се консултирайте с лекар. Вземете със себе си химически реагент и контейнер от него.
- В случай на нараняване винаги се консултирайте с лекар.
- Неправилната употреба на химикали може да причини нараняване и увреждане на здравето. Извършвайте само експериментите, посочени в инструкциите.
- Този набор от експерименти е предназначен само за деца на 12 и повече години.
- Способностите на децата се различават значително дори в рамките на една възрастова група. Ето защо родителите, които провеждат експерименти с децата си, трябва да решат по свое усмотрение кои експерименти са подходящи за техните деца и ще бъдат безопасни за тях.
- Родителите трябва да обсъдят правилата за безопасност с детето или децата си, преди да експериментират. Особено внимание трябва да се обърне на безопасното боравене скиселини, алкали и запалими течности.
- Преди да започнете експерименти, изчистете мястото на експериментите от предмети, които могат да ви пречат. Съхраняването на хранителни продукти в близост до тестовата площадка трябва да се избягва. Мястото за изпитване трябва да е добре проветрено и близо до кран или друг източник на вода. За експерименти се нуждаете от стабилна маса.
- Веществата в опаковките за еднократна употреба трябва да се използват напълно или да се изхвърлят след един експеримент, т.е. след отваряне на опаковката.
ЧЗВ
Къде мога да получа 96% разтвор на алкохол (етанол)?
Алкохолът може да бъде закупен в аптека или получен чрез лабораторен метод. За да направите това, ще ви трябват три свещи и силен алкохол или 40-60% разтвор на етанол. Останалите ще намерите в кутията Plant Chemistry и стартовия комплект.
- Поставете металния адаптер в тапата с един отвор.
- Поставете силиконова тръба на адаптера.
- Поставете фуния в колбата и налейте 40 ml силен алкохол или 40-60% разтвор на етанол.
- Запушете колбата.
- Налейте студена вода в стъклена чаша (до средата). Пуснете епруветката в чашата.
- Поставете три свещи на горелката и ги запалете. Покрийте горелката с разпределител на пламъка.
- Поставете колбата върху дифузера на пламъка. Спуснете свободния край на тръбата в епруветката. Изчакайте, докато епруветката се напълни с течност до две трети.
- Загасете свещите.
- Изсипете течността от епруветката в чаша с натрошени зелени листа и продължете опита, като следвате инструкциите.
Други експерименти




Инструкция стъпка по стъпка
Хлорофилът е веществото, което давалистата са зелени. Той е практически неразтворим във вода, но е разтворим в много органични разтворители, като етилов алкохол.
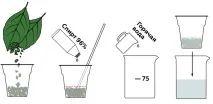
Когато достатъчно хлорофил се разтвори в алкохола, вземете две проби от разтвора.
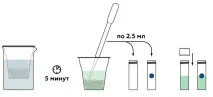
В молекулата на хлорофила има магнезиев йон Mg 2+ (зелен). В присъствието на киселина тя лесно "напуска" молекулата. Образува се феофитин - съединение с по-малко ярък и наситен цвят.

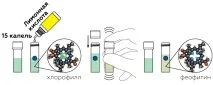
Освободеното от магнезий място лесно може да бъде заето от медния йон Cu 2+ (кафяв) от медната сол CuSO4. Полученият феофитинов меден комплекс е подобен по цвят на хлорофила.

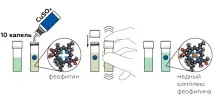
Медният комплекс на феофитина е по-стабилен от хлорофила. Ако оставите и двете проби на светлина, хлорофилът ще избледнее и разликата между веществата ще бъде ясно видима.
Изхвърляне
Изхвърлете твърдите отпадъци от експеримента с битовите отпадъци. Изцедете разтворите в мивката и след това изплакнете обилно с вода.
Какво стана
Защо използваме разтворител?
Алкохолът помага за извличането на хлорофила от натрошените листа. Молекулата на хлорофила има дълга хидрофобна („страхуваща се от вода“) опашка, която пречи на веществото да се разтвори във вода. Но в алкохол (или например в ацетон) разтворимостта на хлорофила вече е доста висока.
Хлорофилът се разтваря и в мазнините. Поради това някои растителни масла, като рапично и маслиново, често имат подчертан зелен оттенък. За обезцветяване на такива масла те се третират с алкали. В резултат на това молекулата на хлорофила губи хидрофобната си опашка, а с това и способността да се разтваря в мазнините.
По-добре от ацетона и алкохола, хлорофилът се разтваря само в течности като бензин. Но бензинът не може да направи същотоефективно извлича пигмента от листата. Факт е, че в растението молекулите на хлорофила са тясно свързани с протеиновите молекули. За да се прекъсне връзката с протеина, разтворителят трябва да съдържа вода, която не се смесва с въглеводороди (бензин, керосин, петролев етер).
Защо зеленият разтвор избледня след добавяне на лимонена киселина?
Цветът на разтвора става по-малко наситен, тъй като в кисела среда водородните йони Н + заместват магнезиевите йони Mg 2+ и хлорофилът се превръща във феофитин. В сравнение с оригиналното вещество, феофитинът има по-тъмен, но в същото време по-малко ярък цвят.
Феофитинизацията е много често срещано явление. Тази ужасна дума се нарича процесът на обезцветяване на хлорофила поради загубата на магнезиеви йони Mg 2+ в присъствието на киселини. Сигурно сте забелязали, че пресните зелени зеленчуци са склонни да потъмняват при готвене. Ефектът на феофитинизацията е особено очевиден при ецване на краставици: след добавяне на марината яркозелената кожа на плода става кафеникава.
Какво се случва, когато се добави CuSO4?
Когато добавим разтвор на меден сулфат CuSO4, в епруветката се появяват медни йони Cu 2+. Те заемат място в молекулата на хлорофила, от което преди това е бил изместен магнезият Mg 2+. Комплексът от хлорофил с мед има ярко зелен цвят, така че разтворът отново придобива подчертан зелен цвят. Дори след няколко дни, когато съдържащият магнезий хлорофил вече е имал време да се срине, цветът на разтвора на медния комплекс на хлорофила остава наситен.
Продуктът от взаимодействието на разтвор на феофитин с медни йони Cu 2+ има грубо име - "меден хлорофилен комплекс". Това вещество е регистрирано под код E141 като одобрен хранителен оцветител. Такова вещество може да се използва само в строго ограничени дози, т.ксъдържащата се в него мед е тежък метал, опасен за здравето в количества над 5 мг на ден. Американската администрация по храните и лекарствата (FDA) разрешава използването на E141 в храни изключително за оцветяване на сухи смеси при производството на цитрусови напитки. В този случай делът на багрилото трябва да бъде не повече от 0,2% от теглото на сухия продукт. В Европа, България и повечето страни от Азия, Африка и Южна Америка е разрешено използването на хлорофил медния комплекс в производството на сладкарски изделия, зеленчукови консерви, козметични продукти и лекарства.
Какви други метали могат да заемат мястото на магнезия в хлорофила?
Не само медта Cu 2+ може да възстанови цвета на подкиселен разтвор на хлорофил. Солите на цинка Zn 2+ и живака Hg 2+ също образуват зелено оцветени съединения с хлорофила. Реакциите с тези йони обаче са много по-бавни и изискват специални условия, а цветът на комплексите с хлорофила не е толкова наситен, колкото при медта. Също така си струва да запомните, че живачните соли са изключително токсични и изобщо не са предназначени за домашни експерименти.
Защо разтворът на хлорофил побледня?
С течение на времето се получава фотохимично окисление в разтвор на магнезиевия комплекс на хлорофила. Поради това разтворът губи наситения си цвят. Медният комплекс на хлорофила е много по-стабилен от своя естествен предшественик. Не се окислява толкова бързо и затова разтворът му запазва цвета си по-дълго.
Листата на кои растения са най-подходящи за експеримента?
Много свежи зелени листа ще свършат работа. Преди да проведете експеримента, уверете се, че растението не е отровно. Също така не използвайте листата на растения с млечен сок (еуфорбия, глухарче, любимия на майката фикус идруго). За да проверите дали има млечен сок в растението, погледнете разреза на листа: изпъкнали бели (понякога жълти, бежови или червеникави) непрозрачни капчици показват, че е по-добре да не вземате такъв материал за експеримента. Със сочни месести листа (седум, каланхое, традесканция и други) разтворът ще се окаже блед, тъй като пулпата на листата на такива растения съдържа твърде малко хлорофил.
Опитайте този експеримент у дома с абонамент за MEL Chemistry