кломифен. Кломифен цитрат. Клостилбегит.
Кломифен. Кломифен цитрат. Клостилбегит.
Физични свойства. Химическа структура. Фармакодинамика. Фармакокинетика.
Кломифенът е нестероиден селективен модулатор с добър капацитет за свързване с естрогенните рецептори.
Външен вид бял или бледожълт прах, без мирис, нестабилен на въздух и светлина.
Според химичната структура кломифенът е (E,Z)-2-(4-(2-хлоро-1,2-дифенилетенил)фенокси)-N,N-диетил-етанамин под формата на цитрат с молекулно тегло 598.09
Лекарството има висока бионаличност (повече от 90%), метаболизира се в черния дроб и се характеризира с продължителна ентерохепатална рециркулация. Полуживотът е 5-7 дни. Основният път на екскреция е с изпражнения, в по-малка степен с урина. След въвеждане на кломифен в продължение на 5 дни в доза от 100 mg на ден, той се открива в серума до 30 дни. Това е продължителността на екскрецията на лекарството, което обяснява лекия стимулиращ ефект, който понякога може да се наблюдава при следващия индуциран естествен менструален цикъл.
Кломифен във формулировки се предлага като рацемична смес от два стереохимични изомера:
- Зукломифен (Zu-кломифен). Това е CIS конфигурация
- Енкломифен (En-clomiphene). Представлява TRANS конфигурация
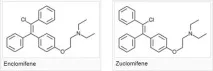
Високотехнологична оценка на фармакокинетиката на отделните изомери (Mikkelson TJ et al., 1986) показа, че всеки изомер изгражда свой собствен индивидуален профил концентрация-време. En-кломифенът се появява и изчезва от кръвната плазма много по-бързо и по-пълно, рисувайки относително по-крива линия на графиката от Zu-кломифен. Ивъпреки факта, че делът на Zu-изомера е само 38% от общия дял на приеманото лекарство, реално регистрираните му плазмени концентрации са много по-високи и по-стабилни. В тази връзка трябва да се отбележат проучвания, които показват, че биологичната ефективност на лекарството при жените се дължи предимно на активността на Zu-кломифен (Charles D et al., 1969; Pandya G et al., 1972). Не е ясно обаче дали Zu-кломифенът е по-ефективен по отношение на овулацията, зачеването и степента на бременност в сравнение с класическата смес от изомери (MacLeod SC et al., 1970; Murthy YS et al., 1971; Van Campenhout J et al., 1973; Connaughton JF et al., 1974)
Все по-често кломифенът се оценява по отношение на възможностите за лечение на вторичен мъжки хипогонадизъм (Ioannidoukadis Stella, Wright Pat J. et al., 2006). Има мнение, че лекарството в някои случаи може да бъде по-привлекателна опция от ХЗТ с тестостерон, особено като се имат предвид неговите очевидни предимства под формата на непропорционално по-ниска цена и удобство на перорално приложение (Taylor Frederick et al., 2010), както и липсата на вторично инхибиране на гонадите, рискът от което в някои случаи, плюс всичко, изисква допълнителни инжекции на гонадотропини (Kaminetsky Jed et al., 2009). Интересното е, че наблюденията показват, че по отношение на мъжете En-clomiphene вече демонстрира по-голяма ефективност (Hill S, Arutchelva V, Quinton R, 2009).
Основният механизъм на действие е да се прекъсне отрицателната обратна връзка на ендогенните естрогени на ниво хипоталамични рецептори (Kahwanago I et al., 1970; Etgen AM et al., 1979) съгласно принципа на антагонистична селективна блокада на рецепторите, което от своя страна причинява вторично увеличениеосвобождаване на гонадотропин-освобождаващ хормон (GnRH) от хипоталамуса в хипоталамо-хипофизния циркулационен портал, причинявайки повишаване на нивата на FSH и LH, редовно активиране на кохортата на антралния фоликул - действителната индукция на овулация (Dickey RP et al., 1996; Kousta E et al., 1997). Увеличаващите се фоликули от своя страна произвеждат естрадиол, чиято концентрация, въпреки факта, че надвишава физиологичната, в присъствието на кломифен не е в състояние да работи ефективно в регулаторните структури. В същото време, на ниво хипоталамус-хипофиза, тялото продължава да възприема ниско ниво на естрадиол, приблизително съответстващо на средата на лутеалната фаза на менструалния цикъл. Всъщност се оказва, че естрадиолът вече не е в състояние ефективно да прилага отрицателен биологичен лост върху дейността на хипоталамуса. В същото време амплитудата на секрецията на GnRH придобива по-чест, но нисък пулсационен характер. Въпреки че това се реализира в повишаване на серумните концентрации на гонадотропини (FSH, LH), концентрацията на LH в кръвния серум често надвишава концентрацията на FSH (Vandenberg G et al., 1973), което не може да се счита за физиологично и, наред с други неща, вероятно е фактор за намаляване на качеството на фоликул-овоцит-ембрион и цикъла на лечение като цяло. Трябва да се отбележи, че физиологичната природа на циркоралния ритъм в началото на фоликуларната фаза предполага по-високи импулси на секреция на GnRH от хипоталамуса, което се реализира във физиологичното преобладаване на FSH над LH. Втората значителна отрицателна последица от действието на лекарството се счита за клинично значима блокада на ендогенните естрогенни рецептори на нивото на миометриума, ендометриума и цервикалния канал, което се реализира в неадекватна пролиферация на маточната лигавица, слаба реакция на жлезите на цервикалния канал и редица други отрицателнивлияния. Ето защо, въпреки факта, че кломифенът е в състояние да предизвика овулация при повечето ановулаторни жени (според различни данни от 70% до 92% от всички клинични случаи), процентът на бременност остава доста нисък, поради следните основни факти:
- Промени в условията на узряване на комплекса ооцит-кумулус
- Антиестрогенен ефект върху ендометриума.
- Антиестрогенен ефект върху цервикалния канал
- Намалена маточна перфузия
- Промени в контрактилната активност на матката, маточните тръби и промени в механизмите на ембрионален транспорт
Лекарството е показано при ановулаторно безплодие при липса на клинично доказани хипогонадотропни и хипергонадотропни състояния като причини за ановулация. Спорно е употребата на лекарството при LUF-синдром, недостатъчност на лутеалната фаза, безплодие с неясен или тубарен произход, всякакво изразено безплодие на партньора, както и в IVF цикли като моноиндуктор.
За дълъг период на употреба на лекарството е натрупана значителна база от доказателства за употребата на кломифен в групата на ановулаторни пациенти (Практически комитет на ASRM (август 2013 г.). Според преглед на Cochrane от 1998 г. на пет рандомизирани проучвания (Deaton, 1990; Mels, 1987; Fisch, 1989; Glazener, 1990), доминирането на c Освен това, друг систематичен преглед на 12 рандомизирани проучвания (Beck JI et al., 2005) още по-убедително потвърди ефективността на кломифен в сравнение с плацебо.и др., 2010; Hughes E et al., 2000) клинични проучвания, които вече оценяват полезността от употребата на кломифен при жени с неясен генезис на репродуктивна дисфункция в сравнение с плацебо или очаквано лечение, демонстрират липсата на ефективност на този подход.
Въпреки високата ефективност на опита за предизвикване на овулация с кломифен в условията на правилен подбор на пациентите и протокола за стимулация, статистически всяка пета жена, особено в случай на PCOS, остава резистентна към него. В тази връзка е напълно логично да се разшири обхватът на терапевтичните действия до опит за предизвикване на овулация с гонадотропини, включително в рамките на ин витро оплождане, или да се обсъди изборът на оптимална стъпка за хирургично лечение с цел корекция на поликистозни яйчници, а при неефективност - включването на донор на яйцеклетки в програмата за АРТ.
Странични ефекти. Безопасност за жена и дете.
Лекарството се понася добре и като цяло се характеризира с редки нежелани реакции. И така, от най-често срещаните:
- горещи вълни (10%)
- дискомфорт, подуване на корема или газове (5%)
- гадене и повръщане (2%)
- дискомфорт в гърдите (2%)
- зрителни прояви (замъгляване, мигане, нарушено цветоусещане)
- главоболие (1,5%)
- многоплодна бременност (5%), в по-голямата част от случаите близнаци (Kausta E et al., 1997)
- OHSS (по-малко от 1%), преобладаващо лек (Kausta E et al., 1997)
Има проучвания, показващи повишен риск от вродени дефекти, особено дефекти на невралната тръба на плода (Anencephaly овулация стимулация субфертилност и нелегитимност, 1973; Singh M et al., 1978; Dyson JL et al., 1973; Sandler B 1973; Field B et al., 1974; Berman P, 1975; James WH 1974; Shoham Z et al. 1991), но според други данни тези прояви се вписват в нормалния диапазон на общата популация (Bridgewater NJ, 2013; Harlap S, 1976). При обсъждането на риска от спонтанен аборт, сравнителното проучване на Dickey RP et al., 1996, което включва 1744 бременни жени след индуцирана овулация с кломифен и 3245 жени, при които бременността е настъпила спонтанно, се счита за най-обективно. Авторите демонстрират абсолютно еднаква честота на абортите и в двете групи.
Като отклонение от правата линия, трябва да се отбележи, че кломифенът е включен в списъка на Световната антидопингова агенция на незаконните допингови лекарства в спорта (Забраненият списък на WADA 2012).
И до днес кломифенът остава най-често използваното и едно от най-популярните лекарства за индуциране на овулация, особено в етапите до високоспециализираните етапи.лечение. Въпреки ниската степен на бременност, това се обяснява много просто.
- Минимална цена
- Висока сигурност
- Лесен контрол на текущото лечение
- Лекарствена форма, предполагаща перорално приложение и без необходимост от инжекции