Методи за диаграми
Цели и задачи
Целта на тази работа е практически анализ на кривите на охлаждане на бинарни системи и изграждането на диаграми на равновесие въз основа на тях.
Основните цели на доклада включват:
1. Дефиниции на методите за конструиране на диаграми.
2. Обяснения на принципа на конструиране на триъгълници на Таман.
3. Изследване на инвариантното състояние.
4. Построяване на диаграми на състоянието.
5. Определете фазовото равновесие в зоните на диаграмата на двукомпонентна система по време на охлаждане.
Раздел 1. Теоретична част
Методи за построяване на диаграми. Триъгълник на Тамман
Изграждането на диаграми на равновесие се основава на изследването на броя и състава на фазите при различни температури. За тези цели се използват два метода:
1. динамичен (метод на кривата на охлаждане);
2. статичен (метод на закаляване).
Същността на динамичния метод се състои в изграждането на криви на охлаждане (нагряване) за първоначалните състави на системата в координатите ²температура - време² при постоянна скорост на изменение на температурата. В същото време с помощта на специално оборудване се откриват топлинни ефекти, причинени от физикохимични процеси, протичащи в системата:
¾ кристализация и топене;
¾ разширяване на системните връзки.
При постоянна скорост на охлаждане дължината на хоризонталната зона на кривата на охлаждане зависи от количеството фаза в началото на процеса, което определя този процес. Тоест, ако площта на кривата на охлаждане е следствие от кристализацията на евтектична стопилка, то за първоначалния състав, който съвпада с евтектичния състав, дължината на хоризонталната зона ще бъде максимална. Геометричният метод се основава на това правило.намиране на точното местоположение на някои елементи от диаграмите, така нареченият метод на триъгълника на Тамман. На фиг. 1 показва примери за конструиране на триъгълници за изброените по-горе ситуации.
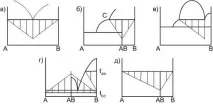
Фигура 1. Елементи за конструиране на диаграми на двукомпонентни системи: а - кристализация на стопилка с евтектичен състав; b - образуване на химично съединение, топящо се неконгруентно; в - ликвация; d – полиморфни трансформации на кристални фази; д - образуването на химично съединение, което се разлага в твърдата фаза.
За силикатни системи, при които скоростта на установяване на равновесното състояние е ниска, динамичният метод не винаги дава правилен резултат. В този случай използвайте статичен метод за това:
1. Хомогенизираната смес от компоненти се нагрява до предварително определена температура.
2. Поддържайте дълго време при тази температура.
3. Рязко охлаждане.
4. След това се използват методи за химичен анализ за определяне на състава и количеството на образуваните фази.
Тази процедура за един състав се повтаря многократно с промяна на температурата на задържане и въз основа на получените резултати се изгражда диаграма на равновесие. Методът се отличава с висока точност, но по-трудоемък, отколкото при динамичния метод.
Елементи на диаграмата
Диаграмата се състои от вертикална ос - температурната ос, хоризонтална ос - концентрационната ос на компонентите.
Външният вид на диаграмата е показан на фигура 2. Левият край на хоризонталната ос на концентрациите на компонентите, означен с буквата А, съответства на 100% съдържание на компонент А, десният край - 100% съдържание на компонент Б.
Ta и TV са съответно точките на топене на чистите компоненти A и B. Ако точката на състава е на една от вертикалните оси на диаграмата (на A или B), тогава в товаслучай разглеждаме процесите, протичащи в еднокомпонентна система.
Кривите Ta - E и E - TV се наричат криви на ликвидус. Кривите на ликвидус са температурни зависимости на пренасищането на стопилката по отношение на всеки компонент или химично съединение. Кривата Ta - E показва температурата на началото на кристализацията в системата на компонент А от стопилката по време на нейното охлаждане, кривата E - Tb - съответно началото на кристализацията на компонент B.
Точка E се нарича евтектична точка и характеризира състава на стопилката с минималната температура за съществуване на течната фаза за дадена система, стопилка с евтектичен състав. Тази стопилка е едновременно пренаситена по отношение на двата компонента А и В. По време на кристализацията на стопилка с евтектичен състав, компонентите винаги се изолират в твърдата фаза в строго определено съотношение, определено от позицията на евтектична точка.
Хоризонтална линия, начертана при температура T2 от линията на ликвидус до вертикалата на утаената твърда фаза, се нарича конод.
Фигура 2. Диаграма на двукомпонентна система
Линията Te - E - Te * се нарича солидус линия. Това е линията на края на кристализацията или началото на топенето на всеки бинарен състав на системата. Под линията на солидус само фазите в твърдо състояние могат да бъдат в равновесие. Трябва също да се отбележи, че солидусната линия не винаги е хоризонтална.
Основните елементи на кривите на охлаждане са инфлексната точка и хоризонталната платформа.
Инфлексната точка на кривата на охлаждане при постоянна скорост на охлаждане се появява, когато скоростта на охлаждане се промени. А това от своя страна е свързано с началото на процеси в системата, придружени от топлинни ефекти, които по правило имат екзотермичен характер приохлаждане на системата. Допълнителното отделяне на топлина намалява скоростта на охлаждане на системата и наклонът (между кривата на охлаждане и абсцисата на графиката) се увеличава.
За бинарните системи промяната в наклона на кривата на охлаждане се свързва предимно с началото на кристализацията на една кристална фаза: компонент или химическо съединение.