Определяне на масата на амоняка по време на окисляването му с калиев перманганат, задачи за USE-тест по химия
Този проблем е интересен по две причини: първо, наличието на примес в едно от веществата; второ, неяснотата на реакциите, описани в условието.
Задача 3.10. За окисляването на определено количество амоняк е необходим такъв обем кислород (н.о.), който се образува при разлагането на 245,6 g калиев перманганат, съдържащ 3,5% безкислороден примес. Определете масата на реагиралия амоняк и обема на образувания азотсъдържащ окислителен продукт (n.o.).Дадено е: маса на калиев перманганат с примеси: m (KMnO4 + примеси) = 245,6 g; масова част от примеси в KMnO4: (примеси) = 3,5% . Намерете: маса на am моний: m (NH3 ); обем на азотсъдържащ реакционен продукт (n.c.): V(продълж.) = ?Решение: Две последователни реакции са описани в условието на проблема:
Окисляване на амоняк с кислород, получен в първата реакция. Но процесът на окисляване може да протече по различни начини. По време на горене (специален случай на окислителната реакция) се образуват азот и вода:
По време на окисление в присъствието на катализатор първо се образуват азотен оксид (II) и вода:
При изчисляване за всяко от последните две уравнения се получават различни отговори. Индикацията в състояние на азотсъдържащ окислителен продукт (а не изгаряне) предполага образуването на NO. Но в инструкциите за проверка на USE тестовете цялото изчисление е извършено, като се вземе предвид производството на азот. В ситуацията на решаване на този проблем на изпита беше възможно да се използва някоя от предложените тук реакции на окисление и в случай на незаслужено ниски резултати да се докаже правосъдието при обжалване. Но има алтернативен, по-разумен вариант на поведение. Включете в решението изчисленията за всеки отвъзможни варианти. Един от тях недвусмислено ще съвпадне с варианта на правилния отговор на инспекторите и вие гарантирате най-висок резултат за тази задача. Тук представяме вариант на решение, предполагащ изгаряне на амоняк.
Алгоритъмът може да бъде представен със следната схема:
1. Определете масата на чист KMnO4:
2. Съгласно първото уравнение на реакцията, ние определяме количеството на веществото на образувания кислород:
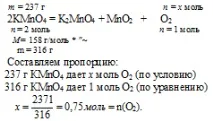
3. Тъй като целият кислород, освободен при 1 реакция, отиде в реакцията на изгаряне на амоняк, можем да изчислим обема на образувания азот и масата на изгорения амоняк.

Отговор: m(NH3)=17g; V(N2) = 11,2 литра.
Коментари: 1 При излишък на кислород азотният оксид (II) лесно се окислява до азотен оксид (IV).