РЕАКЦИИ НА ЗАМЕСТВАНЕ В БЕНЗЕЛНИТЕ ЯДРА
Хомолозите на бензена влизат в реакции на заместване със същите реагенти като бензена.
Въпреки това, алкиловите радикали, присъстващи в молекулите на бензенови хомолози (-CH3, -C2H5, -C3H7 и т.н.), са донори на електронна плътност и проявяват положителен индуктивен ефект. Увеличаването на електронната плътност се случва главно в позиции 2, 4 и 6 по отношение на радикала.
Благодарение на това преразпределение на електронната плътност, бензеновото ядро става по-активно в реакциите на заместване (реакциите протичат по-лесно, при по-меки условия), а новопостъпилият заместител се насочва къморто- ипара-позиции спрямо алкиловия радикал.
Например, прихлориранена толуен се образува смес оторто- ипара- хлоротолуени:
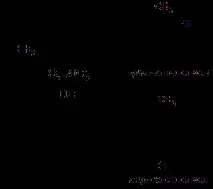
Нитриранена толуен с нитрираща смес при нагряване може да доведе до заместване на три водородни атома с нитро групи:

При по-меки условия се образува смес оторто- ипара-нитротолуени (вижте Приложение 1).
РЕАКЦИИ НА СТРАНИЧНАТА ВЕРИГА
Алкилните радикали могат, при подходящи условия, да проявяват същите химични свойства като алканите. По този начин взаимодействието на бензенови хомолози с хлор в присъствието на осветление без катализатор протича по радикален механизъм. В този случай водородните атоми се заменят в страничната верига, а не в ароматното ядро:

В случай на по-сложни въглеводородни радикали, заместването протича предимно при въглеродния атом, който е най-близо до бензеновия пръстен:
ОКСИДАЦИЯ
Под действието на калиев перманганат върху бензенови хомолози, страничните въглеводородни вериги се окисляват. При провеждане на реакцията в кисела среда продуктът от окисляването на толуен е бензоена киселина:

Когато калиевият перманганат действа върху толуен в неутрална среда, се образува сол на бензоена киселина - калиев бензоат:

По-сложните странични вериги "изгарят" под действието на окислители: въглеродният атом, който е най-близо до бензеновия пръстен, остава в карбоксилната група, а останалите въглеродни атоми се окисляват до въглероден диоксид:
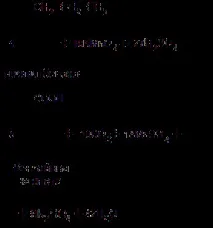
Бензенови хомолози, съдържащи две странични вериги, дават двуосновни киселини или техни соли при окисление:
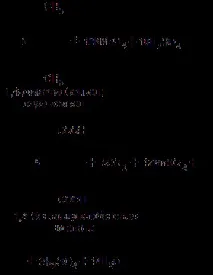
ПРОИЗВОДСТВО НА БЕНЗОЛ И НЕГОВИТЕ ХОМОЛОЗИ
ДЕХИДРОГЕНИРАНЕ И ДЕХИДРОЦИКЛИЗАЦИЯ НА АЛИФАТНИ ВЪГЛЕВОДОРОДИ
Процесът на превръщане наалкани в арени се нарича дехидроциклизация,защото включва едновременно две реакции: затваряне на цикъл на линеен въглеводород и елиминиране на водород. Бензолът се получава от хексан, толуен от хептан и смес от етилбензен и ксилени от октан:

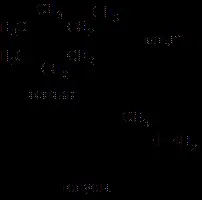
Като катализатори в тези процеси се използват платина, паладий или Cr2O3 върху алуминиев оксид.
Ароматни въглеводороди също се образуват по време надехидрогениране на циклохексан и неговите хомолози:
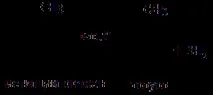
Промишленият процес, при който арени се получават от петролни въглеводороди чрез реакциите на дехидроциклизиране и дехидрогениране, описани по-горе, се нарича реформинг.
ТРИМЕРИЗАЦИЯ НА АЦЕТИЛЕН
Когато ацетиленът преминава през активен въглен при 400-600 ° C, тримеризацията на ацетилена се извършва с образуването на бензен:
СЛИВАНЕ НА БЕНЗОЕНА КИСЕЛИНА С АЛКАЛ
Когато солите на бензоената киселина се слеят с алкали, карбоксилната група се отцепва с образуването на бензен:
С тази реакция е възможно да се получи бензен от неговите хомолози чрез серия от стъпки, например чрезсхема
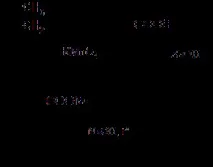
РЕАКЦИЯ НА WURZ-FITTIG
Когато ароматни халогенни производни реагират с халоалкани, се образуват бензенови хомолози, например:

Спомнете си, че неговите хомолози също могат да бъдат получени от бензен чрез реакции на алкилиране с халоалкани или алкени (вижте раздела „Химични свойства на ароматните въглеводороди“).
ЗАДАЧИ ЗА САМОСТОЯТЕЛНА РАБОТА
| а) | G) |
| б) | д) |
| V) | д) |
Дайте име на всяко от тези вещества в съответствие с правилата на номенклатурата на IUPAC. Дайте също тривиалните имена на тези вещества, за които се използват такива имена.
Напишете структурните формули на тези вещества.
3.Напишете структурните формули на всеки пет ароматни вещества от състав С9Н12. Дайте имена на тези вещества.
4.Напишете уравненията за следните реакции:
а) нитриране на бензен;
б) алкилиране на бензен с 2-хлоропропан;
в) алкилиране на бензен с пропилей.
Посочете условията на реакциите, назовете получените вещества.
5.Напишете уравненията за следните реакции:
а) взаимодействия на бензен с хлор в присъствието на алуминиев хлорид;
б) взаимодействието на бензен с хлор под действието на ултравиолетово лъчение;
в) взаимодействие на толуен с хлор в присъствието на алуминиев хлорид;
г) взаимодействие на толуен с хлор на светлина в отсъствие на катализатор.
По какъв механизъм - радикален или йонен - протичат реакциите в) и г)?
6.Напишете уравненията за следните реакции:
а) окисление на етилбензен с калиев перманганат в присъствието на сярна киселина;
б) окисляванепара-ксилен с воден разтвор на калиев перманганат.
7.Напишете уравненията за следните реакции:
а) дехидрогениране на циклохексан;
b) дехидрогениране на 1,2-диметилциклохексан;
в) дехидроциклизиране на октана.
Назовете получените ароматни въглеводороди.
8. Напишете уравненията на реакциите, от които може да се получи етилбензен
Посочете условията на реакцията.
9.Напишете уравненията на реакцията, които могат да се използват за получаване на бензен от калциев карбид в два етапа.
10.Напишете уравненията на реакцията, които могат да се използват за получаване на бензен от толуен в два етапа.
11. Дайте уравненията на реакцията, които ви позволяват да разграничите
а) бензен и хексен-1;
б) бензен и толуен;
в) толуен и стирен.
12.Напишете уравненията на реакциите, които могат да се използват за извършване на следните трансформации:
13.Напишете уравненията на реакцията, които могат да се използват за извършване на следните трансформации:
14.Напишете уравненията на реакцията, които могат да се използват за извършване на следните трансформации:
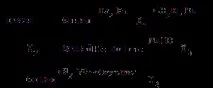
15. Напишете уравненията на реакцията, които могат да се използват за извършване на следните трансформации:

[1] Формално тази реакция може да се разглежда като добавяне на C6H5-H молекула бензен към пропилей, при което е изпълнено правилото на Марковников: Н атомът отива към по-хидрогениран въглероден атом при двойната връзка на пропилена, след което фенил C6H5- е свързан към втория въглероден атом на пропилена.