Технология за производство на лизин
1. Характеристики на крайния продукт на продукцията
2. Химична схема на производство
3. Технологична схема на производство
4. Характеристики на суровини, материали
.1 Подготовка на стерилна културална среда
4.2 Подготовка на семената
4.3 Условия на отглеждане
5. Приготвяне на лизинови препарати
5.1 Течен концентрат на лизин
5.2 Сух лизин концентрат
5.3 Кристален лизин
През последните години животновъдството в България рязко намаля и в резултат на това вносът на месни продукти се увеличи до недопустими нива.
Една от причините за намаляването на производството на месни продукти е влошаването на качеството на фуражите и повишаването на тяхната цена, което се дължи на почти пълното спиране на предприятията, произвеждащи фуражен протеин, поради тяхната неконкурентоспособност при променената ценова структура. Днес фуражният протеин е почти изцяло вносен.
И така, за зърнените култури и всички селскостопански животни и птици, ограничаващите аминокиселини са метионин, лизин, триптофан и треонин.
В момента в България птицевъдството е водещ отрасъл. При храненето на птиците първата лимитираща аминокиселина е лизинът, втората е метионинът, който се произвежда както у нас, така и в чужбина чрез химичен синтез и се доставя на българския пазар в достатъчни количества.
Ефектът от използването на незаменими аминокиселини, по-специално L-лизин, се основава на факта, че зърненият протеин, основният компонент на фуража за селскостопански животни и птици, има неблагоприятен състав на аминокиселините, които го образуват. Един от тях -L-lysine- е дефицитен и не може да бъдесинтезирани в животинския организъм.
Обикновено дефицитът се отстранява чрез добавяне към диетата на т.нар. "Протеинови" (протеинови) добавки, богати на L-лизин - като рибно и месокостно брашно, соев и слънчогледов шрот, хидролиза и фуражна мая. Въпреки това, дефицитът, както беше споменато по-горе, може също да бъде елиминиран просто чрез въвеждане на подходящо количество кристален L-лизин във фуража.
Напоследък потреблението на L-лизин интензивно расте в развитите страни - 12-15% ръст годишно - и днес се доближава до 500 хиляди тона / година. Преди началото на икономическите реформи СССР беше най-големият производител на L-лизин (до 1/3 от световното производство в средата на 80-те години).
1. Характеристики на крайния продукт от производството
Лизинът е незаменима аминокиселина, която е част от почти всеки протеин, необходима е за растежа, възстановяването на тъканите, производството на антитела, хормони, ензими, албумини.
Сега е установено, че лизинът в организма е не само структурен елемент на протеина, но също така изпълнява редица важни биохимични функции - той е предшественик на карнитин и оксилизин, подпомага транспорта на калций и стронций в клетките и др.
Доказано е, че лизинът подобрява апетита, насърчава секрецията на храносмилателни ензими и предотвратява зъбния кариес при децата.
L-лизинът се използва главно като фуражна добавка поради ниското количество на тази аминокиселина в растителните храни.
В растениевъдството могат да се използват препарати, съдържащи лизин. Използването на такива препарати, съдържащи освен аминокиселини и други биостимуланти, дава значително увеличение на добива на оранжерийни и полски култури.
Освен това беше предложено да се използват лизинови препарати като хранаатрактанти за дезориентация на ларви на телени червеи.
Лизин пантотенат може да се използва срещу левкопения. Солите на фитиновата киселина и лизин, оксилизин имат антианемичен и анаболен ефект. Лизин ацетиласпартат може да се използва за лечение на миокарда, интоксикации от ендогенен или екзогенен произход, чернодробни заболявания и др.
Клетките на микроорганизмите, образувани след ферментацията, заедно с маточните разтвори обикновено се използват в протеинов фуражен продукт съгласно технологията за производство на фуражни дрожди.
Лизин(2,6-диаминохексанова киселина) е алифатна аминокиселина с изразени основни свойства; есенциална аминокиселина. Лизинът е известен като две оптически активни D- и L-форми. Безцветни кристали. Естественият L-лизин (tpl 224-225°C, с разлагане) е лесно разтворим във вода, киселини и основи, слабо в алкохол. Изолиран през 1889 г. от казеинов хидролизат, синтезиран през 1902 г.; е част от почти всички протеини от животински и растителен произход (голямо количество лизин се намира в хистони и протамини, в малко количество - в протеини от зърнени култури. Липсата на лизин в храната забавя растежа при деца, при възрастни води до отрицателен азотен баланс и нарушаване на нормалното функциониране на тялото. Дневната нужда от лизин при възрастни е 23mg / kgтелесно тегло, при кърмачета - 170mg/kg
2. Химическа схема на производство
Химията на образуване на молекула лизин е показана на фиг. 1.
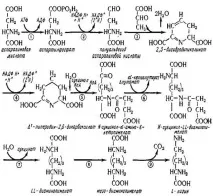
Фиг. 1.Химия на биосинтезата на лизин
При получаване на лизин е необходимо да се изключат нежелани странични процеси. Така че при недостатъчна аерация може да се получи образуването на аланин или млечна киселина вместо синтеза на лизин. Много важен фактор е концентрацията на оскъдниаминокиселини - хомосерин, метионин и треонин в средата. За нормален растеж и биосинтеза на лизин от Brevibacterium sp. 22, оптималната концентрация на треонин е 800 mg, метионин - 200 mg на литър хранителна среда. В допълнение, развитието на културата изисква тиамин в концентрация от 200 µg на 1 литър от средата. Биотинът е важен регулатор на процеса. Същата култура на Brevibacterium sp. 22 произвежда глутаминова киселина при концентрация на биотин в средата, равна на 1–4 μg/l, и лизин при концентрация 15–20 μg/l. Смята се, че биотинът променя пропускливостта на клетъчната мембрана. При концентрация на биотин 2,5 mg/l се стимулира и образуването на млечна киселина.
Важна роля играе треонинът, който е задължителен растежен фактор в началния етап на ферментацията. Концентрацията му обаче не трябва да бъде голяма, тъй като в следващите етапи на ферментация (по време на синтеза на лизин) той може да действа като инхибитор на ензима аспартат киназа. Наличието на лизин засилва инхибиторните свойства на треонина.
При производствени условия, ако добивът на лизин е 35,7% от използваните захари, общото превръщане на глюкоза, амоняк и кислород в лизин и клетъчна биомаса може да се опише с уравнението:
От дясната страна на това уравнение първият член показва количеството лизин, получено от глюкоза. От 1 молекула глюкоза се образуват 0,35 молекули лизин. Вторият термин характеризира образуването на биомаса. От уравнението може да се види, че за обработката на всяка молекула глюкоза са необходими 2,19 кислородни молекули. Това означава, че интензитетът на аериране по време на растежа на културата трябва да бъде 2-4 g 02 на час на 1 литър среда.
3. Технологична схема на производство
В зависимост от предназначението от културалната течност могат да се получат различни микробиологични препарати.(Фигура 1): течен лизин концентрат (LCL), сух фуражен лизин концентрат (DCL), кристален лизин.
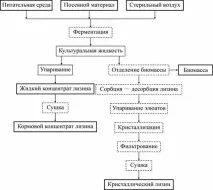
Фиг. 2.Технологична схема за производство на лизинови препарати
За биосинтезата на лизин се използват хомосерин-дефицитни мутанти на ауксотрофни бактерии от родоветеBrevibacterium,Micrococcus,Corynebacterium.
4. Характеристики на суровини, материали
В промишлени условия като източник на въглерод се използват фуражно зърно, меласа, хидрол, хидролизати от целулозни суровини, нишесте и оцетна киселина.
4.1 Приготвяне на стерилна културална среда
Всички производители на лизин са биотин-зависими микроорганизми. Количеството биотин в средата трябва да бъде значително по-високо (29 μg/L), отколкото е необходимо за нормален растеж и развитие на микробните клетки (4–5 μg/L). Ако количеството биотин се намали до 1-2 µg/l, биосинтезата на лизин се забавя, но в същото време се увеличава образуването на глутаминова киселина.
Източникът на биотин, витамини и редица аминокиселини обикновено са екстракт от царевица и меласа от цвекло. Максималната биосинтеза на лизин се наблюдава върху среда със захароза (Таблица 1).
Ефект на въглероден източник (концентрация 7,5%) върху биосинтезата на L-лизин от производителя Brevibacterium flavum
| Източник на въглерод | ASB *, g/l | Лизин, g/l | Усвояване на захар, % | YP/S |
| Глюкоза | 15.2 | 22.0 | 7.6 | 0,37 |
| захароза | 18.2 | 25,0 | 7.1 | 0,42 |
| Галактоза | 2.0 | 1.0 | 0,7 | 0,02 |
| Ксилоза | 5.2 | 3.5 | 2.5 | 0,06 |
| Маноза | 9.3 | 6.0 | 4.5 | 0,10 |
| Рамноза | 3.6 | 2.0 | 1.3 | 0,03 |
| арабиноза | 1.0 | Стъпки | 0,7 |
От съществено значение в процеса на усвояване на въглеродсъдържащи съединения е тяхната концентрация в хранителната среда. Най-голямото количество лизин се получава в среда, съдържаща 10–12% захароза. При по-високи концентрации на захароза, специфичната скорост на растеж на производителя намалява и скоростта на превръщане на захарта намалява (YP/S).