Тема №7 Производство на амоняк
Избройте основните методи за фиксиране на азот.
Фиксирането на азот се отнася до реакции, по време на които молекулният азот образува различни съединения, например реакцията на образуване на амоняк по време на взаимодействието на азот с водород.
Интересите на биолозите са насочени към конкретни научни области, от които могат да се разграничат следните:
1) търсене на нови микробни и растителни азотфиксиращи общности и определяне на тяхната роля в глобалната азотфиксираща система на планетата;
2) изследване на молекулярните механизми на връзката между растенията и азотфиксиращите микроорганизми;
3) изследване на физичните и физико-химичните основи на явлението азотфиксация;
4) изследване на генетиката на азотфиксацията и създаването на азотфиксиращи растения чрез генно инженерство;
5) разработване на комплекс от агробиологични технологии за повишаване на производителността на азотната фиксация в растениевъдството.
Как се промени структурата на ресурсната база с развитието на азотната промишленост? Какъв вид естествени суровини са намерили практическо приложение в началото за получаване на технологични суровини?
Какво е предимството на природния газ пред другите видове природни суровини?
Предимство на природния газ (CH4):
Изгарянето на метан е придружено от леко отделяне на замърсители, както твърди прахови, така и газообразни: азотни, серни и въглеродни оксиди.
Метанът може да служи като междинно гориво при постепенния преход към алтернативни енергийни източници като вятърна, слънчева, водноелектрическа, приливна и геотермална енергия.
Метанът е широко разпространен и наличен в повечето градове, в непосредствена близост до финалаконсуматори на електроенергия. Това означава, че за такива електроцентрали е по-лесно да се намери място и те не изискват дълги линии за пренос на високо напрежение.
Електроцентралите от смесен тип, работещи на метан, са доста ефективни.
Постоянното снабдяване с метан може да бъде организирано с помощта на подземни газопроводи, спестявайки консумацията на енергия от влакове и камиони, доставящи гориво от рафинерията до електроцентралата.
Захранващите с метан електроцентрали могат да бъдат преобразувани да използват водород като гориво, когато водородът е наличен в достатъчни количества на достъпни цени.
Съставете химическа и функционална схема за получаване на технологичен газ за синтез на амоняк от природен газ.
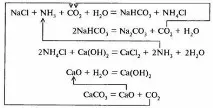
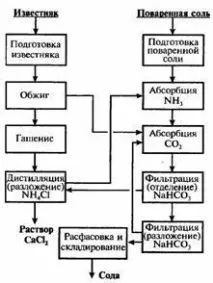
Функционална схема на синтез на амоняк: А – синтез на NH3; B – отделяне на NH3; B - компресия и рециркулация
Защо е необходимо природният газ да се почиства от серни съединения? Как и при какви условия се извършва?
Пречистване на природен газ от съдържащи сяра съединения чрез адсорбция на сероводород, което пречи на по-нататъшни трансформации:
H2S + ZnO = ZnS + H20
Конверсия на метан с пара. Както природният газ (CH4), така и водата (H2O) са суровини за получаване на един от компонентите за синтеза на амоняк - водород H2. При тази трансформация две реакции протичат едновременно:
CH4 + H2O = CO + ZH2;
CO + H2O = CO2 + H2.
Преобразуване на въглероден окис с пара (в предишния процес въглеродният окис CO не се превръща напълно в CO2 поради ограничения на равновесието):
CO + H2O = CO2 + H2.
След този процес се постига възможно най-голямото извличане на водород от суровината - метан CH4 и вода H2O.
Анализирайте химикала ифункционална схема на десулфуризация.
Какви съображения се ръководят при избора на технологичния режим на основните етапи на паровъздушния реформинг на природния газ?
Какви катализатори се използват при превръщането на метан и въглероден окис? Какви примеси в газа причиняват отравяне на катализаторите? Какъв е експлоатационният им живот?
Всички реакции протичат с участието на катализатори и при високи температури. По време на процеса на конвекция на CH4 природният газ се пречиства от серни съединения, които са каталитични отрови, а азотно-водородната смес се пречиства от въглеродни оксиди.
Конверсията на метана се извършва при температура 800-900 °C върху никелов катализатор.
Какви са отпадъчните газове от агрегатите за синтез на амоняк? Как се почистват?
Конвертираният газ, получен след преобразуване на метан, съдържа 20-40% въглероден окис.
За да се увеличи добивът на водород, газът след превръщането на метана се редуцира с пара.
Какви методи са намерили практическо приложение за пречистване на преработен газ от въглероден диоксид? Избройте техните предимства и недостатъци.
Напишете химичните реакции, които са в основата на пречистването на моноетаноламин. Какво е страничен продукт от процеса и какво практическо приложение намира?
Абсорбция на въглероден диоксид - отстраняване на CO2, получен при производството на водород. Абсорбира се с разтвор на моноетаноламин:
CO2 + 2RNH2 + H2O = (RNH3)2CO3.
Обосновете избора на технологичния режим на етапите на абсорбция на CO2 и регенерация на разтворителя в процеса на пречистване на технологичен газ с моноетаноламин.
Пречистване на MEA - ниска цена, стабилност на процеса, лесна регенерация, висок капацитет на абсорбция. При почистване на газ с 17-21% разтворIEA има 2 реакции:
Какви методи за пречистване от въглероден окис се използват в съвременните технологични агрегати за производство на синтезен газ?
Пречистване на газ от въглероден окис CO. След превръщането на CO остава малко количество CO, което пречи на по-нататъшните трансформации. Те се освобождават от него, превръщайки се в метан:
Как се извършва финото пречистване на преработен газ от въглеродни оксиди?
Катализаторите, съдържащи желязо-хром и мед, са селективни: първият осигурява достатъчна скорост на реакция при температура 450-500 ° C, вторият активно работи при 250-300 ° C. Остатъчната концентрация на CO е 0,3-0,5%.
След почистване на газа от въглеродни оксиди, той влиза в синтеза на амоняк.
Посочете най-важните области на приложение на амоняка.
Амонякът е един от най-важните продукти на химическата промишленост, годишното му световно производство достига 150 милиона тона. Използва се главно за производство на азотни торове (амониев нитрат и сулфат, урея), експлозиви и полимери, азотна киселина, сода (амонячен метод) и други химически продукти. Като разтворител се използва течен амоняк.
В хладилната техника се използва като хладилен агент (R717)
В медицината 10% разтвор на амоняк, често наричан амоняк, се използва при припадък (за възбуждане на дишането), за стимулиране на повръщане, както и външно - невралгия, миозит, ухапвания от насекоми и за лечение на ръцете на хирурга. Ако се използва неправилно, може да причини изгаряния на хранопровода и стомаха (в случай на приемане на неразреден разтвор), рефлекторно спиране на дишането (при вдишване във високи концентрации).
Прилага се локално, инхалация и вътре. За възбуждане на дишането и изваждане на пациента отпри припадък внимателно донесете малко парче марля или памучна вата, навлажнена с амоняк, към носа на пациента (за 0,5-1 s). Вътре (само в разплод) за предизвикване на повръщане; също като част от амонячно-анасонови капки - като муколитично (отхрачващо) средство. При ухапвания от насекоми - под формата на лосиони; с невралгия и миозит - триене с амонячен линимент. В хирургическата практика те се отглеждат в топла преварена вода и измиват ръцете си.
Тъй като амонякът е слаба основа, той неутрализира киселините при взаимодействие с тях.
Физиологичният ефект на амоняка се дължи на острата миризма на амоняк, която дразни специфични рецептори на носната лигавица и възбужда дихателните и вазомоторните центрове на мозъка, причинявайки учестено дишане и повишаване на кръвното налягане.
Антифризна добавка за сухи разтвори, свързани с ускорители. Препоръчителното дозиране е 2...8% от теглото на компонентите на сухата смес в зависимост от температурата на нанасяне. Амонячната вода е продукт (NH3*H2O), който е газообразен амоняк NH3, разтворен във вода.
Направете функционална схема на синтеза на амоняк.
Блок за синтез на амоняк (схема на процеса).
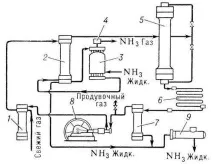
Какви са основните физикохимични характеристики на реакцията на синтез на амоняк от азот и водород, които влияят върху избора на технологичния режим на процеса? Като се имат предвид тези характеристики, обосновете избора на налягане, температурен режим на процеса, вида на технологичната схема.
Какви съображения управляват избора на пространствена скорост на газа в колоните за синтез на амоняк?
Обяснете механизма на хетерогенния каталитичен процес на синтез на амоняк. На какви етапи може да се опише?
Какви катализатори се използватв синтеза на амоняк?
При синтеза на амоняк от прости вещества - азот и водород - като катализатор се използва поресто желязо с примеси на Al2O3 и K2O
Какви методи за отделяне на амоняка от циркулиращия газ се използват в инсталации със средно налягане?
Циркулационният газ с температура 50°C постъпва във вторичната кондензационна система, която включва кондензационна колона и изпарители за течен амоняк. В кондензационната колона газът се охлажда до 18 ° C и в изпарителя поради кипене на амоняка в пръстена до -5 ° C. От тръбното пространство на изпарителите сместа от охладен циркулационен газ и кондензиран амоняк постъпва в разделителната част на кондензационната колона, където течният амоняк се отделя от газа и свежата азотно-водородна смес се смесва с циркулационния газ. След това газовата смес преминава през кошница с порцеланови пръстени на Рашиг, където се отделя от капки течен амоняк, издига се през топлообменните тръби и се изпраща към външен топлообменник и след това към колоната за синтез.
Какво представляват продухващите и резервоарните газове? Какво приложение намират?
Обяснете структурата на колоната за синтез. Анализирайте как работи.
Принципна технологична схема за синтез на амоняк в блок с капацитет 1360 тона / ден на местно оборудване.
Прясна азотно-водородна смес след пречистване чрез метаниране се компресира в центробежен компресор до налягане от 32 MPa и след охлаждане във въздушен охладител навлиза в долната част на кондензационната колона за пречистване от остатъчни примеси от CO3, H2O и следи от масло. Свеж газ мехурчета през слоя от кондензиран течен амоняк, освобождавайки се от водни пари и следи от CO2. и масла, наситени с амоняк до 3-5% и смесени сциркулационен газ. Получената смес преминава през тръбите на топлообменника на кондензационната колона и се изпраща в пръстеновидното пространство на отдалечения топлообменник, където се нагрява до 185-1950 ° C поради топлината на газа, напускащ колоната за синтез. Цикълният газ след това влиза в колоните за синтез.
Формулирайте основните изисквания към колоните за синтез на амоняк.
Какви технологични мерки допринасят за опазване на околната среда при производството на амоняк?
Голямотонажното производство на амоняк се характеризира със следните емисии в околната среда:
1) газ, съдържащ амоняк, азотни и въглеродни оксиди и други примеси
2) отпадъчни води, състоящи се от кондензат, продукти за измиване на реактори и охладителни системи;
3) ниска потенциална топлина.
Относителната концентрация на токсични примеси от производството на амоняк под формата на въглероден оксид и азотни оксиди в отработените газове е ниска, но когато азотните оксиди се редуцират до елементарен азот, се разработват специални мерки за елиминиране дори на незначителни емисии. Пълното елиминиране на токсичните емисии е възможно чрез каталитично пречистване в присъствието на редуциращ газ.