Уравнение на електролитна дисоциация, степен, константа, реакции
В следващите етапи от развитието на науката много учени продължиха изследванията и разработките в тази област, въз основа на наличната информация за структурата на атомите и природата на химичните връзки между тях. По-специално, I. A. Kablukov се занимава с въпроса за процесите на разтваряне, V. A. Kistyakovsky определя зависимостта на издигането на течен стълб в капиляр при условия на температура на кипене от молекулното тегло.
Съвременна интерпретация на теорията
Преди появата на това откритие много свойства и обстоятелства на процесите на разделяне не са били проучени, както и самите разтвори. Електролитната дисоциация е процесът на разпадане на вещество на съставните му йони във вода или други полярни течности, взаимодействието на частиците на съединението с молекулите на разтворителя, появата на подвижност на катиони и аниони във възлите на кристалната решетка поради топене. В резултат на това образуваните вещества придобиват ново свойство - електропроводимост.

Състав, класификация и имена на заредени частици в светлината на електролитната дисоциация
Йонът е атом или група атоми, които носят положителен или отрицателен заряд. Те се характеризират с условно разделение на прости (K (+) , Ca (2+) , H (+) - състоящи се от един химичен елемент), сложни и сложни (OH (-), SO4 (2-), HCO3 (-) - от няколко). Ако катион или анион е свързан с молекула на разтворителя, той се нарича солватиран, с дипол на молекулата на H2O - хидратиран.
При електролитна дисоциация на водата се образуват две заредени частици H (+) и OH (-). Водородният протон приема несподелена електронна двойка кислород от друга водна молекула в свободна орбитала, в резултаткойто образува хидрониевия йон H3O (+).
Основните положения на откриването на Арениус
Всички представители на класовете неорганични съединения, с изключение на оксидите, се разлагат в разтвори на ориентирани диполи на течности, в химичен план - те се дисоциират на съставните им йони в по-голяма или по-малка степен. Този процес не изисква наличието на електрически ток; уравнението на електролитната дисоциация е неговото схематично представяне.
Веднъж попаднали в разтвор или стопилка, йоните могат да бъдат изложени на електрически ток и да се движат в посока към катода (отрицателен електрод) и анода (положителен). Последните привличат противоположно заредени атомни агрегати. От тук частиците са получили имената си - катиони и аниони.

Паралелно и едновременно с разпадането на веществото протича обратният процес - асоциирането на йони в първоначалните молекули, следователно не настъпва сто процента разтваряне на веществото. Такова уравнение за реакцията на електролитна дисоциация съдържа знак за равенство между дясната и лявата част. Електролитната дисоциация, както всяка друга реакция, се подчинява на законите, управляващи химичното равновесие, и законът за масовото действие не е изключение. Той гласи, че скоростта на процеса на разлагане на йони е пропорционална на концентрацията на електролита.
Класификация на веществата по време на дисоциация
Химическата терминология разделя веществата на неразтворими, слабо разтворими и разтворими. Последните два са слаби и силни електролити. Информацията за разтворимостта на определени съединения е обобщена в таблица за разтворимост. Дисоциацията на силни електролити е необратим процес, те напълно се разпадат на йони. Слабите - само частично, те се характеризират с феномена на асоцииране и следователно равновесието на протичащите процеси.

Важно е да се отбележи, че няма пряка връзка между разтворимостта и силата на електролита. При силните може да е слабо изразен. Точно като слабите електролити, те могат да бъдат силно разтворими във вода.
Примери за съединения, чиито разтвори провеждат електричество
Класът на "силните електролити" включва всички добре дисоцииращи киселини, като азотна, солна, бромна, сярна, перхлорна и други. В същата степен алкалите са алкални хидроксиди и отделни представители на групата на “алкалоземните метали”. Електролитната дисоциация на солите е интензивна, с изключение на някои цианати и тиоцианати, както и на живачен (II) хлорид.
Класът на "слабите електролити" е представен от останалата част от минерала и почти всички органични киселини: въглеродна, сулфидна, борна, азотна, сярна, силициева, оцетна и др. Както и трудно разтворими и въглеводородни основи и амфотерни хидроксиди (хидроксиди на магнезий, берилий, желязо, цинк в степен на окисление (2+)). От своя страна водните молекули са много слаби електролити, но все пак се разлагат на йони.
Количествено описание на дисоцииращите процеси
Степента на електролитна дисоциация всъщност характеризира степента на процеса на разделяне. Може да се изчисли - броят на частиците, разделени на йони, трябва да се раздели на общия брой молекули на разтвореното вещество в системата. Тази стойност се обозначава с буквата "алфа".
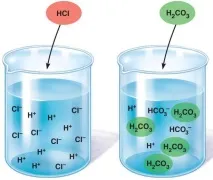
Логично е, че за силните електролити "α" е равно на единица или сто процента, тъй като броят на разпадналите се частици е равен на общия им брой. За слабите винаги е по-малко от едно. Пълното разлагане на изходните молекули на йони във водна среда не се случва, а протича обратният процес.
Основните фактори, влияещи върху пълнотата на гниене
на степенелектролитната дисоциация се влияе от редица неоспорими фактори. На първо място е важно естеството на разтворителя и веществото, което се разлага в него. Например, всички силни електролити имат ковалентен силно полярен или йонен тип връзка между съставните частици. Течностите са представени от диполи, по-специално водата, има разделяне на зарядите в молекулите и в резултат на тяхната специфична ориентация възниква електролитна дисоциация на разтвореното вещество.
Алфа стойността се влияе обратно от концентрацията. С увеличаването му стойността на степента на дисоциация намалява и обратно. Самият процес е изцяло ендотермичен, т.е. необходимо е определено количество топлина, за да започне. Влиянието на температурния фактор се обосновава по следния начин: колкото по-висок е той, толкова по-голяма е степента на дисоциация.
Вторични фактори
Многоосновните киселини, като фосфорната, и основите с няколко хидроксилни групи, например Fe (OH) 3, се разлагат на йони стъпаловидно. Определя се зависимост - всеки следващ етап на дисоциация се характеризира със степен, която е хиляди или десетки хиляди пъти по-малка от предходната.
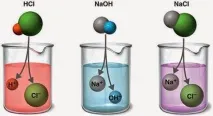
Степента на разлагане може да се промени и чрез добавяне на други електролити към системата, които променят концентрацията на един от йоните на основното разтворено вещество. Това води до изместване на равновесието встрани, което се определя от правилото на Le Chatelier-Brown - реакцията протича в посоката, в която се наблюдава неутрализиране на влиянието, оказвано върху системата отвън.
Класическа константа на процеса на равновесие
За характеризиране на процеса на разлагане на слаб електролит, в допълнение към неговата степен, се използва константата на електролитна дисоциация (Kd), която се изразява чрез съотношението на концентрациите на катиони и аниони към количественотосъдържание в системата от изходни молекули. Всъщност това е обичайната химическа равновесна константа за обратимата реакция на разделяне на разтворено вещество на йони.
Например, за процеса на разлагане на съединение на съставните му частици, константата на дисоциация (Kd) ще се определя от частното на постоянните концентрации на катиони и аниони в състава на разтвора, повишени до степените, съответстващи на числата пред тях в химическото уравнение, и общия брой на останалите недисоциирани формулни единици на разтвореното вещество. Има зависимост - колкото по-високо е (Kd), толкова по-голям е броят на катионите и анионите в системата.
Връзката между концентрацията на слабо разлагащо се съединение, степента на дисоциация и константата се определя с помощта на закона за разреждане на Оствалд по уравнението: Kd = α 2 s.
Водата като слабо дисоцииращо вещество
Диполните молекули се разпадат на заредени частици в изключително малка степен, тъй като това е енергийно неизгодно. Все пак има разделяне на водородни катиони и хидроксилни аниони. Като се вземат предвид процесите на хидратация, можем да говорим за образуването на хидрониев йон и ОН (-) от две водни молекули.
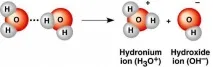
Постоянната дисоциация се определя от съотношението на произведението на водородните протони и хидроксидните групи, наречено йонен продукт на водата, към равновесната концентрация на неразпадналите се молекули в разтвора.
Електролитната дисоциация на водата обуславя наличието в системата на Н (+), които характеризират нейната киселинност, и наличието на ОН (-) - основност. Ако концентрациите на протона и хидроксилната група са равни, такава среда се нарича неутрална. Има така наречения pH индекс - това е отрицателен логаритъм от общото количествено съдържание на Н (+) в разтвор. pH по-малко от 7 показва, че околната средакиселинен, повече за неговата алкалност. Това е много важна стойност, според нейната експериментална стойност се анализират биологични, биохимични и химични реакции на различни водни системи - езера, езера, реки и морета. Уместността на водородния индикатор за промишлените процеси също е неоспорима.
Записване на реакции и нотиране
Уравнението на електролитната дисоциация с помощта на химични знаци описва процесите на разпадане на молекулите в съответните частици и се нарича йонна. Той е в пъти по-прост от стандартния молекулярен и има по-обща форма.
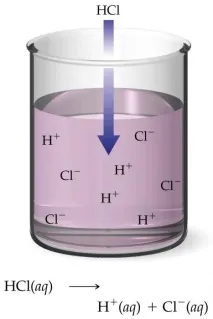
При съставянето на такова уравнение трябва да се има предвид, че веществата, които се утаяват или се отстраняват от реакционната смес като част от газовите пари по време на реакцията, трябва винаги да се записват само в молекулярна форма, за разлика от електролитните съединения, чиито силни представители само във формата, разделена на йони, са включени в състава на разтворите. Електролитната дисоциация за тях е необратим процес, тъй като свързването е невъзможно поради образуването на неделящи се вещества или газове. За този тип уравнения важат същите правила, както и за другите химични реакции - сумите на коефициентите на лявата и дясната част задължително трябва да са равни една на друга, за да се поддържа материалният баланс.
Електролитната дисоциация на киселини и основи може да протече на няколко етапа, ако веществата са многоосновни или многокиселинни. Всяка подреакция има свое собствено уравнение.
Роля в химическата наука и нейното развитие
Създаването на теорията на Сванте Арениус е от голямо значение за общия процес на формиране на физическата и в частност на електрохимичната наука. Въз основа на откриването на такова явление като електролитна дисоциация, електродните процеси са интензивно разработени, спецификата напреминаването на токове през различни среди, теорията на индукцията на потенциалите катод-анод. Освен това теорията на разтворите е напреднала значително. Безпрецедентни открития очакваха химическата кинетика, областта на корозията на метали и сплави, както и работата по намирането на нови средства за защита срещу нея.
В съвременния свят има толкова много нови и непознати неща. Всеки ден учените се придвижват все повече и повече в познанието за такава велика дисциплина като химията. Електролитната дисоциация, както и нейните създатели и последователи, завинаги са заемали почетно място в контекста на развитието на световната наука.