Биосинтеза на глицерол, мастни киселини, ацилглицероли, фосфоглицериди и холестерол
1. Биосинтеза на глицерол и мастни киселини.
2. Биосинтеза на ацилглицероли, фосфоглицериди и холестерол.
3. Патология на липидния метаболизъм.
Биосинтеза на мастни киселини (Линеен път)
Този процес протича в цитоплазмата на клетките. Същността му е постепенното удължаване на молекулата на мастната киселина с 2 въглеродни атома, дължащо се на молекулата на ацетил-КоА и четирите водородни йона, доставяни от NADP-H2. на първия етап въглеродният диоксид се свързва с ацетил-КоА с участието на ензима биотин.
рибоза-5-фосфат и NADP-H2, генерирани от глюкоза в реакциите на пентозния цикъл, както и кобаламин и фолиева киселина, произведени от микрофлората на търбуха.
рибоза-5-фосфат и NADP-H2, генерирани от глюкоза в реакциите на пентозния цикъл, както и кобаламин и фолиева киселина, произведени от микрофлората на търбуха.
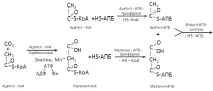
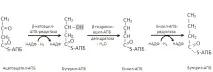
В получения малонил-CoA радикалът –S-CoA е заменен с радикал, носещ ацил протеин (-ACP). Успоредно с това радикалът -S-CoA се заменя с радикала -APB в молекулата на ацетил-CoA. След това малонил-APB се комбинира с ацетил-APB чрез отделяне на въглероден диоксид, за да образува ацетоацетил-APB. Последният се редуцира от водородни йони, разцепени от NADP-H2 до β-хидроксибутирил-APB. След отстраняването на водна молекула от това вещество се образува кротонил-APB, който допълнително се редуцира от водородни йони NADP-H2 до бутирил-APB. Тази реакция завършва първия цикъл на биосинтеза на мастни киселини.
Вторият цикъл започва с комбинирането на β-хидроксибутирил-APB с ацетил-APB с отстраняването на молекула въглероден диоксид. Полученият капронил-APB, по същия начин като ацетоацетил-APB, цикъл след цикъл, се превръща в синтезиран ацил-APBмастна киселина, последвано от разцепване от последния APB радикал.
Броят на молекулите АТФ, изразходвани за биосинтезата на една молекула мастна киселина (НАТР), се изчислява по формулата: HATP=n/2 - 1, където n е броят на въглеродните атоми, включително -COOH групата, а количеството NADP-H2 (ХNADP-Н) -по формулата: ХNADP-Н=n- 2.
Биосинтезата на глицерол-3-фосфатидва от 3-фосфоглицералдехид, образуван от глюкоза в реакциите на гликолиза:
В първия етап неговият глицерол-3-фосфат реагира с две активирани молекули на мастна киселина (напр. стеарил-КоА), за да образува фосфатидна киселина. Остатък от фосфорна киселина се отцепва от последния, последвано от добавяне на трети радикал на мастна киселина на негово място.
HO-CH + 2 стеарил-CoAАцил-CoA-C17H35–CO-O-CHФосфатидиофосфатаза
1 tтрансфераза1 + НОН
3-фосфоглицеролФосфатна киселина
Първо, както е описано по-горе, се синтезира фосфатидна киселина, в която остатък от арахидонова киселина е прикрепен към втория въглероден атом на глицерола.След това се активира молекулата на холина:
Холин-ADPФосфохолин
Фосфохолинът взаимодейства с цитидин трифосфат (CTP):
На първия етап от този процес ацетоацетил-КоА се образува от две молекули ацетил-КоА в резултат на реакция, катализирана от тиолаза. След като третата молекула ацетил-CoA се прикрепи към последната, катализирана от β-хидрокси-β-метил-глутатил-CoA синтаза, се образува β-хидрокси-β-метил-глутатил-CoA. (HMG-CoA). Този ензим е в състояние да инхибира някои лекарства, използвани за лечение на пациенти с атеросклероза, по-специално Zocor. HMG-CoA се редуцира допълнително от водородни йони, отцепени от NADP-H2 в резултат нареакция, катализирана от GMP-CoA редуктаза до мевалонат. Последният, в резултат на шест последователни реакции, се превръща в сквален, въглеводород с дълга отворена верига:
Березов – 312стр.
Впоследствие скваленът се циклизира до ланостерол в резултат на реакция, катализирана от сквален оксидоциклаза. Последният чрез няколко последователни реакции се превръща в холестерол.
Регулиране на липидния метаболизъм.
Този процес се изразява на етапа на приема на храна в тялото. Излишъкът от въглехидрати допринася за повишеното производство на инсулин, което не само подобрява биосинтезата на ацилглицероли от въглехидрати, но също така инхибира тяхното разграждане от липаза в мастните депа. Инсулинът също така подобрява биосинтезата на холестерола в черния дроб. Тироксинът и трийодтиронинът, произведени от щитовидната жлеза, стимулират окисляването на страничната верига на холестерола и освобождаването му в червата с жлъчката.
Мобилизирането на ацилглицероли от мастните депа се улеснява от хормоните адреналин, норепинефрин, глюкагон, тироксин, соматотропин, β-липотропин, кортикотропин и др., Които активират липазата, улеснявайки прехода на нейната неактивна форма в активна фосфорилирана.
Патология на липидния метаболизъм.
Прекомерният прием на въглехидрати и липиди с храната, както и недостатъчното производство на β-липотропин от предния дял на хипофизата води до развитие на затлъстяване. Прекомерната инкреция на този хормон води до развитие на хипофизна кахексия.
Хидролизата на липидите в органите на храносмилателната система може да бъде нарушена от недостатъчно производство на ензими от панкреаса, спиране на потока на жлъчни киселини в червата, които подобряват храносмилането и усвояването на липидите, възпаление на чревната стена и др. В тези случаи липидите се екскретират в изпражненията под формата на капки (стеаторея).
Ацилглицеролите, синтезирани в черния дроб, се екскретират от него, превръщайки се във фосфоглицериди. За биосинтеза на последния са необходими холин, метионин, витамин В12, цистеин, инозитол и други липотропни вещества. С техния дефицит в организма, свързан с недостатъчен прием или нарушение на биосинтезата от микроорганизми на храносмилателния тракт, патология на последния и др. екскрецията на ацилглицероли от черния дроб е нарушена и се развива мастна инфилтрация на този орган.
При хранене на преживни животни с високо концентрирани фуражи се нарушава производството на витамин В12 от микроорганизми на храносмилателния тракт, което също води до нарушаване на превръщането на пропионовата киселина, образувана от микроорганизми от фибри, и сукцинил-КоА и окисляването на последния в цикъла на Кребс. Това води до натрупване на кетонни тела в кръвта (хиперкетонемия) и в урината (кетонурия).
Кетонните тела се натрупват в тялото и при диабет. Дефицитът на въглехидрати в тъканите води до повишено β-окисление на мастни киселини до кетонови тела. Поради липсата на глюкоза последователно се нарушава и производството на оксалооцетна киселина, първият метаболит на цикъла на Кребс. Поради това окисляването на кетоновите тела в последните се инхибира, което също води до развитие на кетоацидоза. Повишената концентрация на глюкоза в кръвта на пациенти с диабет води до увреждане на ендотела на кръвоносните съдове, което допринася за развитието на атеросклероза, последвано от промяна в кръвното ниво на липидните показатели, отбелязани по-горе.