Физика Практическа работа № 7(в)
 |
Условие на проблема: Практика #7(c). Получаване на амоняк и изучаване на неговите свойства
Получаване на амоняк. Ще изпълним всички стъпки, описани в урока.
Сглобете инструмента, както е показано на фигура 50.
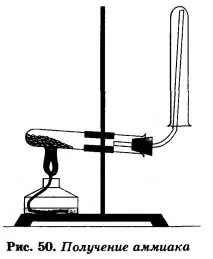
На лист хартия или в малка порцеланова чаша (може да използвате хаванче) изсипете по една лъжица амониев хлорид и калциев хидроксид (лъжица за горящи вещества).
Сместа се разбърква със стъклена пръчка и се изсипва в суха епруветка. Затворете го със запушалка с изходна тръба за газ и го фиксирайте в крака на статива.
Когато фиксирате устройството в крака на статива, обърнете внимание на наклона на епруветката спрямо нейния отвор. Поставете суха епруветка върху изходната тръба за газ, за да съберете амоняк.
Първо загрейте епруветка със смес от амониев хлорид и калциев хидроксид навсякъде (2-3 движения).
пламък) и след това загрейте мястото, където е сместа. За да откриете амоняк, поставете влажна фенолфталеинова хартия с главата надолу в епруветка. След като намерите амоняк, донесете стъклена пръчка, навлажнена с концентрирана солна киселина, до отвора на епруветката. какво наблюдаваш Напишете уравненията на реакцията.
Спрете нагряването на сместа. Внимателно извадете епруветката, в която се събира амоняк, от тръбата за изпускане на газ, като я държите с главата надолу (веднага след изваждането на епруветката с амоняка от нея, затворете края на тръбата за изход на газ с парче мокра памучна вата).
Веднага затворете отвора на извадената епруветка с палец и я спуснете в съд с вода. Извадете пръста си само под вода. какво наблюдаваш Защо водата се повишиепруветка? Отново затворете отвора на тръбата под вода с пръст и я извадете от съда.
1. Защо в този случай епруветката със смес от вещества трябва да бъде фиксирана в крака на статива, така че дъното му да е малко по-високо от отворения край? Написването на уравнението за реакцията между амониев хлорид и калциев хидроксид ще ви помогне да отговорите на въпроса.
2. Защо амонякът се събира в епруветка, обърната с главата надолу? Какви други газове могат да се събират по този начин?
3. Какво може да се наблюдава, ако вместо солна киселина пръчка, навлажнена с концентрирана азотна киселина, се донесе до отвора на епруветка с амоняк? Напишете уравнението на реакцията.
4. Как да докажем, че хидроксидните йони се съдържат във воден разтвор на амоняк?
Изучаване на свойствата на воден разтвор на амоняк
1. Изсипете 2-3 ml воден разтвор на амоняк в епруветка и добавете 2-3 капки разтвор на фенолфталеин. Какъв е цветът на разтвора? Загрейте този разтвор до кипене. Как ще се промени цветът на разтвора? Какво причини тази промяна?
2. Налейте 2-3 ml воден разтвор на амоняк в епруветка. Добавят се 2-3 капки разтвор на фенолфталеин и капка по капка се добавя разтвор на солна киселина, докато пурпурният цвят изчезне. Защо цветът е изчезнал? Напишете уравненията на йонната реакция (пълни и съкратени).
3. Изсипете 2-3 ml воден разтвор на алуминиев хлорид в епруветка и добавете същото количество воден разтвор на амоняк. какво наблюдаваш Напишете уравненията на йонната реакция (пълни и съкратени).