История на изобретяването на калориметъра
През 1780 г. френските учени Антоан Лавоазие (1743 1794) и Пиер Симон Лаплас (1749 1827) предлагат инструмент за измерване на специфичен топлинен капацитет, който те наричат калориметър.
Основата на калориметъра е топлоизолиран съд и калориметрично тяло, в което се поглъща или отделя топлина.
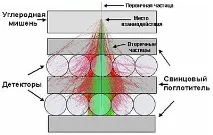
Обикновено калориметърът се използва за определяне на топлинния капацитет, топлината на изпаряване и топлината на изгаряне. Устройството се състои от въглеродна мишена, в която се генерират вторични частици неутрални пиони, които при разпадане образуват фотонен поток. Те се регистрират от слоеве детектори, разположени между абсорберите и оловото под целта. Чрез измерване на броя на вторичните частици може да се определи енергията на първичните. Колкото повече са слоевете детектори, толкова по-точна е измерената енергия.
През 1750 г. петербургският физик Георг Ричман (1711 1753), който работи в сътрудничество с М. В. Ломоносов, експериментално установи, че ако се смесят равни количества вода с различни температури, тогава температурата на сместа ще бъде равна на средноаритметичната стойност на температурите на частите. Тези експерименти са повторени през 1772 г. от Йохан Вилке в Германия. Уилке въвежда мерната единица за количеството топлина, калориите, като количеството топлина, необходимо за промяна на температурата на единица маса вода с един градус. Оцеляла е и до днес.
Концепцията за калории се конкурира с молекулярно-кинетичната теория в продължение на почти 100 години до средата на 19-ти век, а понятията "количество топлина", "топлинен капацитет", "калориметрия", "топлина на топене", "топлина на изпарение" все още са запазени (думата "скрит" едва наскоро изчезна от страницитеучебници). Тези концепции вече са адаптирани към молекулярно-кинетичната теория.
От средата на XIX век. развива теория, която се нарича механична теория за топлината. Откриването на закона за запазване на енергията и успехът на молекулярната теория доведоха до идеята за топлинните процеси като процеси на предаване на механично движение при сблъсък на молекули на тела. Налягането на газовете беше обяснено като предаване на импулс от газови частици към стените на съд. Температурата започва да се свързва с интензивността на движение на частиците. Молекулите се разглеждат като частици, чието движение се подчинява на законите на класическата механика. Оттук и терминологията "механична теория на топлината".
В същото време се разработват статистически представи. Болцман намира точна връзка между средната енергия на топлинното движение на частиците и температурата, въвеждайки нова световна константа, наречена на негово име.
Развитието на статистическата теория доведе до идеята за топлинното движение като специална форма на движение на материята, която не може да бъде сведена до механична. В природата съществуват специфични статистически модели, които имат точни математически изрази, като разпределенията на Максуел, Болцман, Ферми и др.
Развитието на квантовата механика доведе до усъвършенстване на нашите идеи за взаимодействията на частиците при топлинно движение.
За да се гарантира точността на разглежданите физически концепции, трябва да се подчертаят историческите връзки. Понятията количество топлина, топлинен капацитет и др. са неразривно свързани с калоричната хипотеза. Трябва да се обясни, че тази хипотеза е изоставена от науката и ние влагаме нов смисъл в традиционните концепции. Следователно, говорейки за количеството топлина, нямаме предвид количеството на нещо материално, а количеството енергия в определена форма. Тази специфична формаенергия енергията на колектив от хаотично движещи се частици. При нагряване преминава от тяло в тяло или се разпространява вътре в тялото, тогава говорим за топлопроводимост. Слънчевата топлина е енергията на електромагнитното излъчване, трансформирана в енергията на топлинното движение и т.н.
Съвременни калориметри
Съвременните калориметри работят в температурния диапазон от 0,1 до 3500 К и ви позволяват да измервате количеството топлина с точност от 10-2%. Конструкцията на калориметрите е много разнообразна и се определя от характера и продължителността на изследвания процес, температурния диапазон, при който се извършват измерванията, количеството измерена топлина и необходимата точност.