ОРБИТАЛ, Енциклопедия около света
ОРБИТАЛА– областта на най-вероятното местоположение на електрон в атом (атомна орбитала) или в молекула (молекулна орбитала).

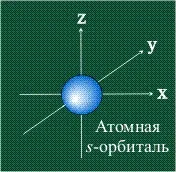
Електронът се движи в атома около ядрото не по фиксирана линия-орбита, а заема определена област от пространството. Например, електрон във водороден атом може с известна вероятност да бъде или много близо до ядрото, или на значително разстояние, но има определена област, където е най-вероятно да се появи. Графично орбиталата се изобразява като повърхност, която очертава областта, където вероятността за поява на електрон е най-голяма, с други думи, електронната плътност е максимална. При водородния атом електронната орбитала има сферична (сферична) форма:


Досега са описани пет вида орбитали:s,p,d, fиg. Имената на първите три са формирани исторически, след което е избран азбучният принцип. Орбиталните форми се изчисляват чрез методите на квантовата химия.
Орбиталите съществуват независимо от това дали върху тях има електрон (заети орбитали) или отсъства (свободни орбитали). Атомът на всеки елемент, започвайки с водорода и завършвайки с последния получен до момента елемент, има пълен набор от всички орбитали на всички електронни нива. Запълването им с електрони става с увеличаване на серийния номер, тоест зарядът на ядрото.
s-орбиталите, както е показано по-горе, имат сферична форма и следователно еднаква електронна плътност в посоката на всяка ос на триизмерни координати:
Има само еднаs-орбитала в първото електронно ниво на всеки атом. Започвайки от второто електронно ниво, в допълнение къмs-орбиталите се появяват и триp-орбитали. Те са във формата на обемни осморки, а именнотака изглежда областта на най-вероятното разположение наp-електрона в областта на атомното ядро. Всякаp-орбитала е разположена по една от трите взаимно перпендикулярни оси, в съответствие с това, в името наp-орбиталите, оста, по която е разположена нейната максимална електронна плътност, е посочена с помощта на съответния индекс:

В съвременната химия орбитала е определяща концепция, която позволява да се разгледат процесите на образуване на химични връзки и да се анализират техните свойства, докато вниманието се фокусира върху орбиталите на тези електрони, които участват в образуването на химични връзки, тоест валентни електрони, обикновено това са електроните от последното ниво.
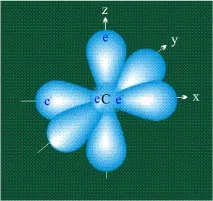
Въглеродният атом в първоначалното си състояние на второ (последно) електронно ниво има два електрона вs-орбиталите (маркирани в синьо) и по един електрон в двеp-орбитали (маркирани в червено и жълто), третата орбитала еpz-вакантна:
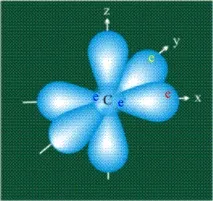
Хибридизация.
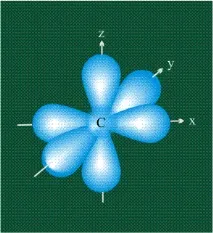
В случай, че въглероден атом участва в образуването на наситени съединения (несъдържащи множество връзки), еднаs-орбитала и триp-орбитали се комбинират, за да образуват нови орбитали, които са хибриди на оригиналните орбитали (процесът се нарича хибридизация). Броят на хибридните орбитали винаги е равен на броя на оригиналните, в този случай четири. Получените хибридни орбитали са еднакви по форма и външно приличат на асиметрични обемни осмици:
Цялата структура изглежда като вписана в правилен тетраедър - призма, събрана от правилни триъгълници. В този случай хибридните орбитали са разположени по осите на такъв тетраедър, ъгълът между които и да е две оси е 109 °. Четирите валентни електрона на въглерода са разположени върху тези хибридиорбитали:
Участие на орбиталите в образуването на прости химични връзки.
Свойствата на електроните, разположени в четири еднакви орбитали, са еквивалентни, съответно химическите връзки, образувани с участието на тези електрони при взаимодействие с атоми от същия тип, ще бъдат еквивалентни.
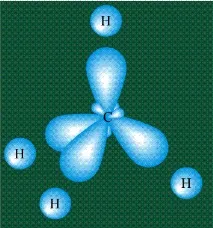
Взаимодействието на въглероден атом с четири водородни атома е придружено от взаимно припокриване на удължени хибридни въглеродни орбитали със сферични водородни орбитали. Всяка орбитала съдържа един електрон, в резултат на припокриване, всяка двойка електрони започва да се движи по комбинираната - молекулна орбитала.
Хибридизацията води само до промяна на формата на орбиталите в рамките на един атом, а припокриването на орбиталите на два атома (хибридни или обикновени) води до образуване на химична връзка между тях. В този случай (cm. фигурата по-долу) максималната електронна плътност е разположена по линията, свързваща два атома. Такава връзка се нарича s-връзка.
В традиционното изписване на структурата на получения метан, символът на валентната лента се използва вместо припокриващи се орбитали. За триизмерно изображение на структурата валентността, насочена от равнината на чертежа към зрителя, е показана като плътна клиновидна линия, а валентността, която излиза извън равнината на чертежа, е показана като пунктирана клиновидна линия:
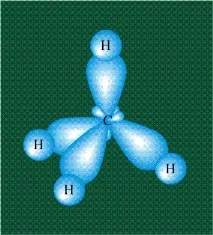
Така структурата на молекулата на метана се определя от геометрията на въглеродните хибридни орбитали:
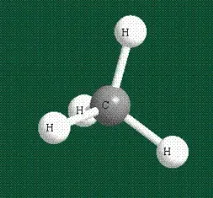
Образуването на молекула етан е подобно на процеса, показан по-горе, разликата е, че когато хибридните орбитали на два въглеродни атома се припокриват, се образува С-С връзка:
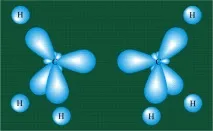
Геометрията на молекулата на етана прилича на метана, валентносттаъгли от 109°, което се определя от пространственото разположение на хибридни въглеродни орбитали:
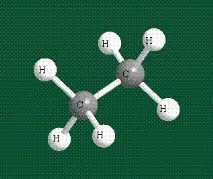
Участие на орбиталите в образуването на множествени химични връзки.
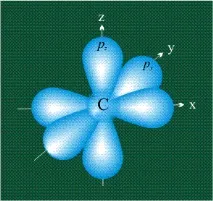
Етиленовата молекула също се образува с участието на хибридни орбитали, но еднаs-орбитала и само двеp-орбитали (pxиpy) участват в хибридизацията, третата орбитала -pz, насочена по остаz, не участва в образуването на хибриди. От първоначалните три орбитали възникват три хибридни орбитали, които са разположени в една и съща равнина, образувайки звезда с три лъча, ъглите между осите са 120 °:
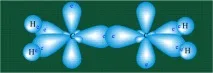
Два въглеродни атома свързват четири водородни атома и също се свързват един с друг, образувайки C-C s-връзка:

Двеpzорбитали, които не са участвали в хибридизацията, се припокриват взаимно, тяхната геометрия е такава, че припокриването се случва не по протежение на C-C линията на връзката, а над и под нея. В резултат на това се образуват две области с повишена електронна плътност, където се разполагат два електрона (маркирани в синьо и червено), участващи в образуването на тази връзка. Така се образува една молекулярна орбитала, състояща се от две области, разделени в пространството. Връзка, при която максималната електронна плътност е разположена извън линията, свързваща два атома, се нарича р-връзка:
Втората валентна линия в обозначението на двойна връзка, която е била широко използвана за изобразяване на ненаситени съединения в продължение на повече от един век, в съвременния смисъл предполага наличието на две области с повишена електронна плътност, разположени от противоположните страни на C-C линията на връзката.
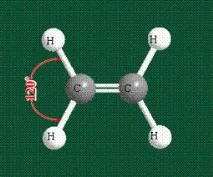
Структурата на етиленовата молекула се определя от геометрията на хибридните орбитали, ъгълът на връзката H-C-H е 120°:
При образуването на ацетилен участва хибридизацияеднаs-орбитала и еднарx-орбитала (орбиталитеpyиpzне участват в образуването на хибриди). Двете получени хибридни орбитали са разположени на една и съща линия по остаx:
Взаимното припокриване на хибридни орбитали една с друга и с орбиталите на водородните атоми води до образуването на s-връзки C-C и C-H, изобразени с помощта на проста валентна линия:

Двете двойки оставащи орбиталиpyиpzсе припокриват. На фигурата по-долу цветните стрелки показват, че от чисто пространствени съображения припокриването на орбитали с еднакви индексиx-xиy-yе най-вероятно. В резултат на това се образуват две p-връзки, обграждащи проста s-връзка C-C:
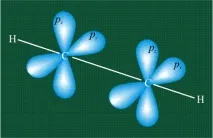
В резултат на това молекулата на ацетилена има пръчковидна форма:
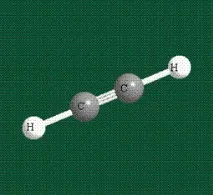
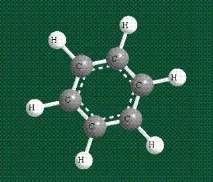
В бензена гръбнакът на молекулата е съставен от въглеродни атоми, които имат хибридни орбитали, съставени от еднаs- и двеp-орбитали, подредени под формата на трилъчева звезда (като в етилена),p-орбиталите, които не участват в хибридизацията, са показани като полупрозрачни:
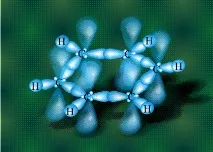
Шестте останалиp-орбитали се припокриват, образувайки молекулна орбитала под формата на две пръстенни области, над и под равнината на бензеновия пръстен:
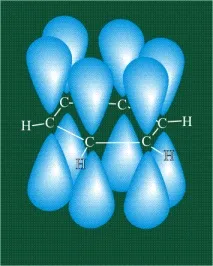
Появява се една затворена електронна система (вижте същоАРОМАТНОСТ).
Молекулата на бензена е плоска, което се дължи на плоската конфигурация на "звездите с три лъча", от които е сглобена. Молекулярна орбитала, образувана от припокриването на шест атомниpорбитали, се обозначава като символ на пръстен вътре в бензеновия пръстен:
Свободните места, тоест орбиталите, които не съдържат електрони, също могат да участват в образуването на химични връзки (виж.Вижте същоТРИЦЕНТРОВИ ВРЪЗКИ).
орбитали на високо ниво.
Започвайки от четвъртото електронно ниво, в атомите се появяват петd-орбитали, запълването им с електрони се случва в преходни елементи, като се започне от скандий. Четириd-орбитали имат формата на обемни четирилистници, понякога наричани "лист на детелина", те се различават само по своята ориентация в пространството, петатаd-орбитала е обемна осмица, навита в пръстен:
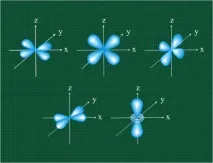
d-орбиталите могат да образуват хибриди сs-иp-орбитали. Параметрите наdорбиталите обикновено се използват при анализа на структурата и спектралните свойства в комплексите на преходните метали.
Започвайки от шестото електронно ниво, атомите имат седемf-орбитали, запълването им с електрони се случва в атомите на лантанидите и актинидите.f-орбиталите имат доста сложна конфигурация, фигурата по-долу показва формата на три от седемте такива орбитали, които имат еднаква форма и са ориентирани в пространството по различни начини:
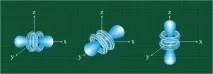
f-орбиталите се използват много рядко, когато се обсъждат свойствата на различни съединения, тъй като електроните, разположени върху тях, практически не участват в химични трансформации.
Перспективи.
На осмото електронно ниво има деветg-орбитали. Елементите, съдържащи електрони в тези орбитали, трябва да се появят в осмия период, докато те не са налични (елемент № 118, последният елемент от седмия период на Периодичната система, се очаква да бъде получен в близко бъдеще, неговият синтез се извършва в Обединения институт за ядрени изследвания в Дубна).
Формата наg-орбиталите, изчислена чрез методите на квантовата химия, е дори по-сложна от тази наf-орбиталите, областта на най-вероятнияместоположението на електрона в този случай изглежда много странно. По-долу е представена една от деветте такива орбитали:
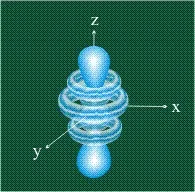
В съвременната химия понятията за атомни и молекулни орбитали се използват широко при описване на структурата и реакционните свойства на съединенията, както и при анализиране на спектрите на различни молекули и в някои случаи за прогнозиране на възможността за протичане на реакции.