Структурата на атома и молекулата на азота
Терминът "азот" е въведен от Лавоазие. Това означава "безжизнен". Въздухът съдържа 75,6% азот по маса и около 23% кислород. Но азотът не поддържа горенето или дишането. Молекулярният азот не се свързва с кислорода и това спасява целия живот на Земята от образуването на киселини във въздушната и водната среда.
Азотът е седмият елемент в периодичната таблица на химичните елементи, разположен в нейната пета група. Структурата на ядрото му е показана на фиг. 104, а. Той е близък по форма до структурата на ядрото на въглеродния атом. Тъй като повечето от ядрата на азотните атоми имат седем протона и седем неутрона, това мнозинство има плоски ядра, показани на фиг. 104, а.
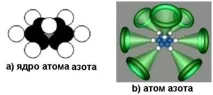
Ориз. 104. Диаграми на ядрото и азотния атом
Диаграма на азотен атом с такова ядро е показана на фиг. 104б и т. Азотният атом има само един активен (валентен) аксиален електрон. Именно тази характеристика създава условията за образуване на молекула от два атома с толкова висока енергия на свързване, че химиците са измислили името тройна връзка за нея. Не, молекулата на азота има една връзка, но с висока енергия на свързване. Жалко е, че спектърът на азотния атом се смесва със спектъра на неговата молекула. Енергията на йонизацияна азотен атом, дадена в справочниците по спектроскопия, равна на 14,534 eV, най-вероятно е енергията на дисоциация на азотна молекула, а не енергията на йонизация на нейния атом. Това е доста голяма енергия на свързване.
А сега нека си представим процеса на преход на шест пръстенни електрона на азотния атом към по-ниските енергийни нива. Неговата особеност се състои в това, че тези електрони преминават едновременно към по-ниските енергийни нива, като същевременно излъчват фотони, чиито размери са с няколко порядъка по-големи от размера на азотния атом. Когато този процес включва целия набор от азотни атоми - веществото, в което той влиза, и когаТой включва въглеродни и кислородни атоми, които също имат пръстен набор от електрони, след което общият брой излъчени фотони незабавно увеличава обема, зает от тях в пространството, което формира явлението експлозия. Разбира се, съществуващата идея, че експлозията е разширяване на газове, е дълбоко погрешна. Налягането се формира от едновременно излъчени фотони поради факта, че техните размери са с 5-7 порядъка по-големи от размерите на атомите. Оттук веднага следват непознати за специалистите изисквания към взривни вещества и ракетно гориво и методи за тяхното прилагане, но няма да развиваме тази тема по добре известни причини.
Молекулата на азота (фиг. 105) се образува от електронни връзки на аксиални електрони 1 и 2 на неговите атоми. Връзката изглежда доста силна. Всички останали 12 електрона са на същото разстояние от ядрата на своите атоми и следователно не могат да бъдат активни, когато азотът е в молекулярно състояние. Няма електрони отляво и отдясно на пръстенните електрони на атомите по протежение на оста на симетрия на молекулата. Това е основната причина за ниската химическа активност на азотната молекула.
Когато анализираме структурата на водната молекула, ще видим причината за увеличаването на нейния размер при замръзване. Този процес също така включва пръстенните електрони на кислородните атоми и фотоните, излъчени и погълнати от тях, и ние ясно ще видим как те осъществяват процеса на увеличаване на размера на водната молекула, когато тя замръзне.
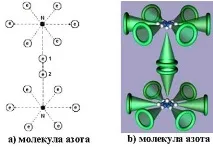
Ориз. 105. Азотна молекула
Цялата енергия на свързване се разпределя по оста на симетрия на молекулата само между два електрона 1 и 2 (фиг. 105, а), поради което се нарича от химиците тройна връзка. Сега трябва да изоставим противоречивите идеи за молекулярните връзки и да свикнем с факта, че един електрон - електронна връзка в различни молекули има различна стойност на енергията на свързване,което определя активността на молекулата при образуването на различни съединения.