Съвременни методи за лечение на рецидивираща хемофталмия и диабетен макулен едем при
Статии. Работа със съдържание
Преглед на минали събития
Съвременни методи за лечение на рецидивираща хемофталмия и диабетен оток на макулата при пролиферативна диабетна ретинопатия на примера на клиничен случай
Всички терапии, използвани при лечението на пациента, до известна степен влияят на нивото на VEGF фактор в очната кухина: панретинална лазерна коагулация поради блокиране на производството на неоваскуларен фактор в неперфузирани области, субтотална витректомия поради механично отстраняване на VEGF, приложение на ранибизумаб (Lucentis) поради свързването на неговите молекули със специфичен антиген. Само комбинираното използване на няколко анти-VEGF техники показва ефективност в случаите на напреднала пролиферативна диабетна ретинопатия.
Съвременни подходи за лечение на рецидивиращ хемофталм и диабетен макулен едем в очите с пролиферативна диабетна ретинопатия: доклад за случай
Всички подходи, приложени към практиката в хода на лечението на пациента, влияят в различна степен на вътреочното ниво на VEGF: панретинална лазеркоагулация - поради потискане на продукцията на неоваскуларен фактор в области на неперфузия, субтотална витректомия - благодарение на механично отстраняване на VEGF, инжектиране на ранибизумаб (Lucentis) - поради свързване на неговите молекули със специфичен антиген. Беше разкрито, че само многостранното приложение на няколко техники е най-ефективно в случаи на напреднала пролиферативна диабетна ретинопатия.
Броят на пациентите с диабет в световен мащаб непрекъснато нараства и в момента наброява около 130 милиона души, а до 2025 г. според прогнозите на СЗО ще достигне 350 милиона души [1-3]. Пролиферативната диабетна ретинопатия (PDR) е съдово усложнениезахарен диабет, който е основната причина за слепота и слабо зрение при хората в трудоспособна възраст. Развиващата се тъканна хипоксия е стимул за растежа на новообразуваните съдове и нарушената съдова пропускливост, което води до развитие на диабетен макулен едем (DME) и рецидивиращ хемофталм [3–9]. Каскадата от патофизиологични реакции, инициирани от хипергликемия и хипоксия, се реализира в компенсаторната хиперпродукция на антиисхемичния ензим васкуларен ендотелен растежен фактор (VEGF) в пигментния епител и външните слоеве на ретината [10-15].
Клиничните проучвания показват значително повишаване на нивото на VEGF в стъкловидното тяло и влажността на предната камера на пациенти с диабетна ретинопатия [4]. VEGF факторът стимулира ретиналната, ретиновитреалната неоваскулогенеза, повишава пропускливостта на съдовата стена, повишава риска от хемофталмия.
Хемофталмът е често срещано усложнение на PDR. Кръвоизливът в стъкловидното тяло рязко намалява зрителната острота, увеличава вероятността от витреоретинална адхезия. Биологично активните продукти, освободени по време на резорбцията на кръвта, могат да служат като катализатори за по-нататъшна фиброваскуларна пролиферация.
Класическият "златен" стандарт за лечение на PDR и DME е лазерната коагулация на ретината, която чрез "изключване" на исхемичните зони спомага за намаляване на концентрацията на VEGF фактор във вътрешните структури на окото. Напоследък интравитреалното приложение на VEGF инхибитора ранибизумаб (Lucentis) се използва широко за предотвратяване на диабетна ретинална неоваскулогенеза и лечение на DME [7, 9].
Lucentis свързва всички VEGF изоформи, инхибирайки тяхната биологична активност, което води до намаляване на неоваскуларизацията, намаляване на екстравазацията,обратното развитие на оток на макулата.
Последните проучвания показват ефективността на интравитреалното приложение на lucentis при рецидивираща хемофталмия на фона на PDR като подготвителен етап преди панретинална лазерна коагулация [5, 16].
При лечението на напредналите стадии на PDR основната роля принадлежи на витреоретиналните интервенции - субтотална витректомия с тампонада на витреалната кухина и ендолазерна коагулация (ELK). Въпреки това, витреоретиналната хирургия, извършена до максимален обем, доста често не гарантира срещу прогресирането на неоваскуларизацията и рецидивиращия хемофталм.
Целта на работата: да се оцени ефикасността и безопасността на комбинираното многоетапно лечение на PDR и DME с рецидивиращ хемофталм при пациент с инсулинозависим захарен диабет.
Методи на изследване. Офталмология: визометрия, тонометрия, биомикроскопия, биомикроофталмоскопия, В-сканиране, оптична кохерентна томография. Обща клиника: мониториране на артериалното налягане, глюкоземия, глюкозурия, микроалбуминурия, електрокардиография. Ефективността се оценява по следните критерии: динамика на зрителната острота, дебелина на невроепителия във фовеоларната област, състояние на стъкловидното тяло (B-сканиране), модел на фундуса.
Безопасността се оценява чрез отсъствието или наличието на офталмологични (хипертония, увеална реакция, хеморагични усложнения) и общи соматични (артериална хипертония, протеинурия, ЕКГ аномалии) странични ефекти.
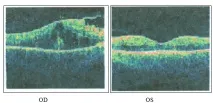
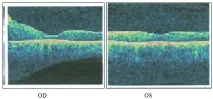
Кръвното налягане се нормализира стабилно чрез приемане на АСЕ инхибитори на ниво 110/70-130/80 mm Hg. Изкуство. Гликемичен профил - 5,7-7,2 mmol / l. Протеинурия - до 0,072 g / l.
В края на етапа на хирургичното лечение Vis OD = 0,1 n/corr.Vis OS = 0,05 sph - 4,0 D = 0,6. Отбелязана е частична регресия на фиброваскуларната пролиферация.
Обективно: OD — IOL в капсулен сак. Фиброзни промени в долните части на витреалната кухина. Очно дъно: ретината е прикрепена във всички отдели, няма пресни кръвоизливи. Останки от глиална тъкан върху оптичния диск и в екваториалната зона. В макулата - дистрофични промени, фокална атрофия на пигментния епител. Дебелината на невроепителия е 255 µm.
OS - първоначално помътняване на лещата. Преретинална фиброза в долните сегменти. Офталмоскопски: дискът на зрителния нерв е бледорозов, границите са ясни. По хода на темпоралните съдови аркади фиброваскуларната пролиферация е намалена и няма пресни кръвоизливи. Архитектониката на централния район е запазена. Дебелината на невроепителия е 247 микрона.
Дискусия
Този клиничен случай, според нас, представлява интерес по няколко причини.
1. Всички терапии, използвани при лечението на пациента, влияят до известна степен на нивото на VEGF фактор в очната кухина: панретинална лазерна коагулация поради блокиране на производството на неоваскуларен фактор в неперфузирани области, субтотална витректомия поради механично отстраняване на VEGF, въвеждане на lucentis поради свързването на неговите молекули със специфичен антиген. Въпреки това, само комбинираното използване на няколко анти-VEGF техники е доказано ефективно в случаите на напреднал PDR.
2. В литературата са описани потенциалните рискове от системни странични ефекти от интравитреалното приложение на инхибитори на VEGF-фактора, а именно артериална хипертония, протеинурия, стомашно-чревно кървене, нарушено зарастване на рани, което е особено неблагоприятно при пациенти със захарен диабет.
При нашето клинично наблюдение общиятприложената доза Lucentis е 5 mg (10 инжекции по 0,5 mg всяка). Общата продължителност на приема е 8 месеца. По време на периода на наблюдение не са отбелязани системни нежелани реакции при пациента.
3. Прогресията на неоваскуларизацията, епиретиналната глиоза, развитието на кистичен оток на макулата в лявото око на пациент с първоначално по-слабо изразена форма на PDR успя да бъде спряна чрез навременно продължително, масивно интравитреално приложение на Lucentis, което гарантира запазването на продуктивното централно зрение.
Изход
Примерът на клиничен случай показва, че само комбинираното използване на няколко анти-VEGF метода показва ефективността на лечението на напреднала пролиферативна диабетна ретинопатия, усложнена от DME и рецидивиращ хемофталм.
L.N. Борискин, В.Н. Потапова
Волгоградски клон на MNTK "Микрохирургия на очите" на името на A.I. акад. С.Н. Федоров» Министерството на здравеопазването на Руската федерация
Борискина Людмила Николаевна — кандидат на медицинските науки, заместник-директор по медицинска работа и медицински контрол
1. Балашевич Л.И. Очни прояви на диабет. - Санкт Петербург: Издателство SPbMAPO, 2004. - 282 с.
2. Дедов И.М., Липатов Д.В. Съвременно състояние и перспективи за развитие на офталмологичната хирургия при ендокринни заболявания // Захарен диабет. - 2006. - № 3. - С. 28.
3. Кузмин А.Г., Липатов Д.В., Смирнова О.М. и др. // Анти-VEGF лекарства за лечение на диабетна ретинопатия // Офталмохирургия. - 2009. - № 3. - С. 53-57.
4. Aiello L.P., Avery R.L., Arrig P.G. и др. Васкуларен ендотелен растежен фактор в очната течност на пациенти с диабетна ретинопатия и други заболявания на ретината // N. Engl. J. Med. - 1994. - V. 331. - P. 1480-1487.
5. Arevalo J.F. Wu L., Sanchez J.G. и др.Интравитреален бевацизумаб (Avastin) за пролиферативна диабетна ретинопатия // Eye. — 2009. — Т. 23. — С. 117-123.
6. Кънингам Е.Т., Адамис А.Р., Алтауеел М. и др. Фаза II рандомизирано двойно маскирано проучване на пегаптаниб, аптамер на антиваскуларен ендителен растежен фактор, за диабетен макулен едем // Офталмология. — 2005. — №. 112. — С. 1747-1757.
7. Massin P., Bandello F., Garweg J. et al. Безопасност и ефикасност на ранибизумаб при диабетен оток на макулата (проучване RESOLVE): 12-месечно, рандомизирано, контролирано, двойномаскирано, многоцентрово проучване фаза II // Diabetes Care. — 2010. — Т. 33. — С. 2399-2405.
8. Moshfeghi A.A., Rosenfeld P.J., Puliajito С. A. et al. Системна терапия с бевацизумаб (Avastin) за неоваскуларна макулна дегенерация, свързана с възрастта: двадесет и четири седмични резултати от неконтролирано отворено клинично проучване // Офталмология. — 2006. — № 113. — С. 2002-2011.
9. Nguyen Q.D., Shah S.M., Khwaja A.A. и др. READ-2 Study Grup. Двугодишни резултати от проучването Ranibizumab за оток на макулата при диабет (READ-2) // Офталмология. — 2010. — Т. 117. — С. 2146-2151.
10. Inan U.U., Avei В., Kusbeci T. et al. Предклинична оценка на безопасността на интравитреално инжектиране на хуманизирано антитяло на васкуларен ендотелен растежен фактор с пълна дължина в очи на плъх // Invest Ophthalmol. Vis. Sci. — 2007. — № 48. — С. 1773-1781.
11. Iriyama A., Chen Y.X., Tamaki Y. et al. Ефект на анти-VEGF антитяло върху ретиналната ганглийна клетка на плъх // Br. J. Ophthalmol. — 2007. — № 91. — С. 1230-1233.
12. Ишида С., Усуи Т., Ямаширо К. и др. VEGF165-медиирано възпаление е необходимо за патологична, но не физиологична, индуцирана от исхемия неоваскуларизация на ретината // J. Exp. Med. — 2003. — № 198. — С. 483-489.
13. Ишида С., Усуи Т.,Ямаширо К. и др. VEGF164 (165) като патофизиологична изоформа: диференциални левкоцитни и ендотелни отговори чрез VEGFR1 и VEGFR2 // Invest Ophthalmol. Vis. наука - 2004 - бр. 45. - С. 368-374.
14. Nishijima K., Yin-Shan N., Zhog L. et al. Васкуларен ендотелен растежен фактор А е фактор за оцеляване за неврози на ретината и критичен невропротектор по време на адаптивния отговор към исхемично увреждане // Am. J Phatol. - 2007. - бр. 171. - С. 53-67.