Валентност на берилий (Be), формули и примери
Общи сведения за валентността на берилия
Берилият под формата на просто вещество е метал (точка на топене 1287 o C, точка на кипене 2507 o C) стоманеносив на цвят, има плътна шестоъгълна кристална решетка, доста твърд и крехък (фиг. 1).

Ориз. 1. Берилий. Външен вид.
Във въздуха се покрива с оксиден филм, който му придава матов оттенък и причинява намалена химическа активност. При нагряване берилият гори в кислород и във въздуха.
Валентност на берилий в съединения
Берилият е четвъртият елемент в периодичната таблица на D.I. Менделеев. Той е във втори период в IIA група. Ядрото на атома на берилий съдържа 4 протона и 5 неутрона (масовото число е 9). В атома на берилия има две енергийни нива, на които има 4 електрона (фиг. 2).
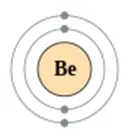
Ориз. 2. Структури на берилиевия атом.
Електронната формула на берилиевия атом в основно състояние е следната:
И енергийната диаграма (построена само за електрони от външното енергийно ниво, които иначе се наричат валентност):
Берилиевият атом има 3 свободни орбитали от подниво 2p. Поради тяхното присъствие електроните от поднивото 2s могат да се разпарят, като един от тях извършва преход и заема една от свободните 2p орбитали, т.е. берилият се характеризира с възбудено състояние.
Наличието на два несдвоени електрона показва, че берилият в неговите съединения (Be II O, Be II (OH) 2, Be II CO3 и др.) Проявява валентност, равна на II, подобно на други химични елементи от група IIA. Валентността на берилия е постоянна.
Примери за решаване на проблеми
| Упражнение | Определете валентността на елементите в следните съединения: а) NH3;б) SO2; в) CO2; d) H2S; д) P2O5. |
| Решение | Определянето на валентността на елементите в химично съединение трябва да започне с посочване на валентността на известен елемент. Във вариант "а" - това е водород, тъй като неговата валентност винаги е равна на I: |
След това определяме общия брой валентни единици на атомите на този елемент:
Поставяме получената стойност вдясно от химическия знак на този елемент, обозначавайки го с арабски цифри:
Сега разделяме общия брой единици на валентност на броя на атомите (индекс) на елемента, за който е известна валентността:
Поставяме полученото частно (3) с римска цифра върху желания елемент като негова валентност:
Това означава, че валентността на елементите в съединението NH3 е: за азота - III и за водорода - I.
По същия начин определяме валентностите на елементите в други съединения: б) S IV O II 2; в) C IV O II 2; г) H I 2S II; д) P V 2O II 5.
| Упражнение | Напишете формулите на кислородните съединения (оксиди) на следните елементи: а) берилий (II); б) силиций (IV); в) калий (I); г) арсен (V). |
| Отговор | Известно е, че валентността на кислорода в съединенията винаги е равна на II. За да съставите формулата на вещество (оксид), трябва да изпълните следната последователност от действия. Първо, записваме химичните знаци на елементите, които изграждат сложното вещество и поставяме валентност над знака на всеки елемент с римска цифра: |
Намерете най-малкото кратно на броя на валентните единици: а) (II × II) = 4; б) (IV × II) = 8; в) (I×II) = 2; г) (V × II) = 10.
Разделете най-малкото общо кратно на броя на валентните единици на всеки елемент вотделно (резултатните коефициенти ще бъдат индекси във формулата):
а) 4/2 \u003d 2 и 4/2 \u003d 2, следователно, формулата на оксида BeO;
б) 8/4 = 2 и 8/2 = 4, оттук и формулата на оксида SiO2;
в) 2/1 \u003d 2 и 2/2 \u003d 1, следователно формулата на оксида е K2O;
г) 10/5 = 2 и 10/2 = 5, следователно формулата на оксида е As2O5.