Вихрови модели на берилиеви атоми
В берилия само един изотоп Be9 е стабилен. Нека разгледаме няколко теоретично най-възможни конфигурации на атоми на този изотоп. Всяка конфигурация е придружена от съответна формула на модерно математическо описание.
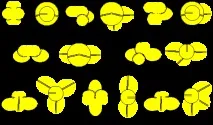
Фигура 1. Най-вероятните конфигурации на берилиевия атом
Ядрата, съответстващи на тези атоми, са показани на фигурата по-долу. Овал обгражда протоните, въртящи се около неутронната ос.
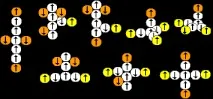
Фигура 2. Ядра на берилиеви атоми
Най-стабилните конфигурации на атомите трябва да бъдат тези, в които алфа-частицата е неразделна част от ядрото. Тези конфигурации са втора, трета и четвърта. Но само втората конфигурация може да бъде претендент за основното състояние на атома, тъй като изчислената стойност на ядрения спин (3/2) съответства на експерименталните данни. В химичните реакции берилият най-често е двувалентен. От атомите с алфа частица в ядрото третата и четвъртата конфигурация са двувалентни. Третата конфигурация ще бъде центърът на молекулите, в които ъгълът между крайните атоми е близо до 90 градуса. Четвъртата конфигурация ще бъде центърът на молекулите, в които ъгълът между крайните атоми е близо до 180 градуса. Според експериментални данни в молекулите F - Be - F, Cl - Be - Cl, Br - Be - Br ъгълът е 180 градуса. Следователно основното възбудено състояние най-вероятно е четвъртата конфигурация. Останалите конфигурации са временно възбудени състояния. В атомите на четвъртата конфигурация вече има две нуклонни двойки, а не една, както при лития, под въздействието на външни сили, те могат да се въртят около неутронната ос. Това свойство може да обясни забележителната способност на берилия да бъде добър модератор на неутрони. Всъщност сблъсъкът на неутрон с който и да е отот две нуклонни двойки практически във всеки случай трябва да доведе не до улавяне на неутрон от ядрото, а до въртене на нуклонната двойка около неутронната ос. Неутронът, от друга страна, трябва да отскочи от нуклонната двойка с промяна на посоката на движение и със загуба на част от кинетичната енергия.
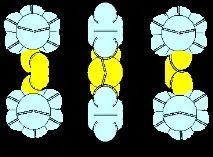
Фигура 3. F - Be - F молекула с берилиев атом от четвъртата конфигурация
Берилият не реагира директно с водорода. Причината може да е трудността да се създадат условия за съвместно съществуване на атомен водород и свободни атоми на берилий.
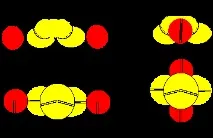
Фигура 4. Две форми на молекулата H - Be - H с берилиев атом от четвъртата конфигурация
Линеен берилиев хидрид може да се получи само чрез разлагане на по-сложни съединения. Тоест в една молекула водородните атоми трябва да са от противоположни страни. Но теоретично водородните атоми могат да се придържат към екваториалната форма на берилиевия атом по два различни начина. При първия метод водородните атоми се придържат към краищата на електронните листа. При втория метод водородните атоми се изтеглят в пролуките между венчелистчетата на берилий, така че размерите на молекула от три атома трябва да се различават малко от размерите на един берилиев атом, което е напълно невъзможно при сферично представяне на формата на атомите. От експериментите е известно, че разстоянията между ядрата на атомите в молекулите варират в зависимост от средата. За свободните молекули в газообразно състояние разстоянията между центровете на атомите обикновено са по-малки от разстоянията между центровете на атомите за молекули в свързано кристално състояние. Може да се предположи, че този факт е свързан със съществуването на два начина за свързване на атомите. В газообразно състояние, при условия на чести сблъсъци с други молекули с висока кинетична енергия, компактната форма е преобладаващо разпространена.молекули. В кристалната форма няма сблъсъци. Там се появява още един фактор - привличане към съседни молекули. Тъй като съседните молекули присъстват от всички страни, атомите в молекулата са максимално разтегнати.
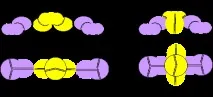
Фигура 5. Две форми на молекулата Li - Be - Li с берилиев атом от четвъртата конфигурация
Металурзите получават сплави на берилий с литий, но няма информация за съединения на берилий с литий. Въпреки че такава молекула не е трудна за изобразяване. Съединение с берилиев атом от четвъртата конфигурация също може да има две форми.
Фигура 6. Молекули H - Be - H с берилиев атом от третата конфигурация
Берилиевият атом от третата конфигурация също е двувалентен. Нека да видим какво се случва, ако атом с такава конфигурация има време да стане част от молекула по време на своето съществуване.
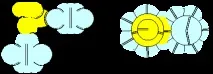
Фигура 7. Молекули F - Be - F с берилиев атом от третата конфигурация
С тази конфигурация може да се образува само една форма на молекулата, където ъгълът между крайните атоми е близък до ъгъла от 90 градуса. За да разберем как се държи един атом в молекулите, достатъчно е да разгледаме химичните съединения с водород като най-прост химичен елемент и флуор като най-химически активен елемент.
Берилиевият атом от първата конфигурация също е двувалентен.
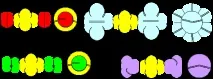
Фигура 8. Конструкция на молекули с берилиев атом от първата конфигурация
Сега остава да разгледаме поведението на атомите с екзотични валентности. В същото време ще направим предположението, че времето на съществуване на атомите в екзотични конфигурации е достатъчно, за да имат време да станат част от молекулата.
Берилиевият атом от втората конфигурация е едновалентен.
Фигура 9. Примери за молекули с берилиев атом от втората конфигурация
Атомът на берилий от петата конфигурация е тривалентен.
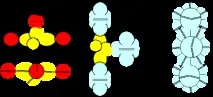
Фигура 10. Примери за молекули с берилиев атом от петата конфигурация.
Берилиевият атом от шестата конфигурация е четиривалентен. Комбинацията от водородни атоми с берилиевия атом от шестата конфигурация може отново да се случи по два различни начина. При първия метод молекулата има форма на свободен лъч. Стабилизирането на лъчите може да се случи в кристална форма, когато водородните атоми привличат електронните лобове на съседни атоми от различни страни. При втория метод водородните атоми се изтеглят в пролуките между венчелистчетата на берилий, така че размерите на молекула от пет атома трябва да се различават малко от размерите на един берилиев атом, което е напълно невъзможно при сферично представяне на формата на атомите. Компактната форма трябва да е присъща на свободните молекули на газовата фаза.
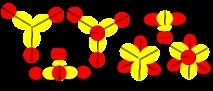
Фигура 11. Пример за молекули с берилиев атом от шестата конфигурация.
Атомът на берилий от седмата конфигурация е четиривалентен.
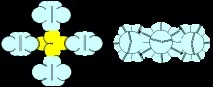
Фигура 12. Пример за молекула с берилиев атом от седма конфигурация.
От особен интерес е берилиевият атом от осмата конфигурация, в който три електронни листа се слепват и не могат да взаимодействат с лобовете на други атоми. Само един електронен лоб на полюс остава химически активен.
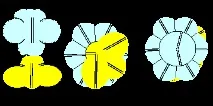
Фигура 13. Be - F молекула с берилиев атом от осма конфигурация.
В това състояние атомът напълно губи своите метални свойства и става аналогичен на разглеждания по-рано литиев атом от втората конфигурация. Ако беше възможно да се създадат условия за увеличаване на живота на възбудените състояния на атомите и техния контакт при ниски кинетични енергии, тогава те биха могли да образуват молекули с възбудените състояния на други атоми, както е показано на фигурата по-долу. Атоми такиваконфигурациите са разделени на десни и леви. Слепването в Be - Be молекула, показана на фигурата, е възможно само от атоми с противоположна ориентация.

Фигура 14. Примери за други молекули с берилиев атом от осма конфигурация.
Адхезията е възможна и за атоми със същата ориентация, само че по напълно различен начин. При слепване се образува симетрична молекула с напълно запълнен електронен слой с шест листа на екватора и по един аксиален дял на всеки полюс.

Фигура 15. Слепване на атоми от осмата конфигурация с еднаква ориентация
За разлика от предишната химически инертна берилиева молекула, тази берилиева молекула е реактивна и може да се комбинира с други атоми.

Фигура 16. Примери за химическата активност на берилиевите молекули