Железен (III) хлорид е

Железен(III) хлорид, железен хлорид FeCl3 е средна сол на фери желязо и солна киселина.
Съдържание
Физични свойства

Блестящи, черно-кафяви или тъмночервени или лилави в пропускаща светлина, зелени в отразена светлина, листа с метален блясък. Той е силно хигроскопичен, във въздуха се превръща в хидрат FeCl3 6H2O - хигроскопични жълти, според други източници, жълто-кафяви кристали, силно разтворими във вода (при 20 ° C, 91,9 g безводна сол се разтваря в 100 g вода).Tpl 309 °C.
Методи за придобиване
- Най-простият метод за получаване на железен трихлорид е действието на хлорен газ върху железни стружки. В този случай, за разлика от действието на солната киселина, се образува железна сол:
- Също така трихлоридът се получава чрез окисляване на железен (II) хлорид с хлор:
- Има и доста интересен метод за окисление със серен оксид (IV):
Химични свойства
- При нагряване при атмосферно налягане до точката на топене започва бавното разлагане на железния трихлорид с образуването на дихлорид и молекулярен хлор:
- Поради факта, че железният трихлорид е силна киселина на Луис, той взаимодейства с някои други хлориди и се образуват комплексни соли на тетрахлоржелязна киселина:
- При нагряване до 350 °C с железен (III) оксид се образува железен оксохлорид:
- Железните соли са слаби окислители, по-специално железният трихлорид окислява добре металната мед, превръщайки я в разтворими хлориди:
Приложение
- Железен (III) хлоридизползва се за ецване на печатни платки (радиотехника, системотехника).
- Използва се за ецване на печатни форми (ецване, цинкография), като алтернатива на азотната киселина, реакцията с която е съпроводена с отделяне на силно токсични изпарения ("лисича опашка").
- Използва се като стъргач при боядисване на тъкани.
- В индустриален мащаб се използва като коагулант за пречистване на вода.
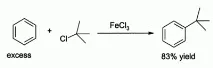
- Поради изразените си киселинни свойства се използва широко като катализатор в органичния синтез. Например за реакцията на електрофилно заместване в ароматни въглеводороди.
Безопасност
Железен (III) хлорид е токсично, силно корозивно съединение. Безводната сол служи като десикант.
Фондация Уикимедия. 2010 г.
Вижте какво е "железен (III) хлорид" в други речници:
Железен (III) хлорид - Железен (III) хлорид Общо систематично наименование Железен (III) хлорид Химия ... Wikipedia
железен (III) хлорид - железен трихлорид, железен (III) хлорид ... Речник на химичните синоними I
Хром (III) хлорид - Хром (III) хлорид ... Уикипедия
Хексааминхромиев(III) хлорид - Общо систематично наименование Хексааминхромий(III) хлорид Традиционни имена хексааминхромиев хлорид Химична формула [Cr(NH3)6]Cl3 Физични свойства ... Wikipedia
Златен(III) хлорид е златен трихлорид AuCl3. Външен вид червени моноклинни кристали. Моларна маса 303,33 g/mol. В безводно състояние е най-добре да се получи чрез действието на хлор върху златно фолио или върху сух златен прах, получен чрез редукция със сулфат ... ... Wikipedia
Хром(III) хлорид - Хром(III) хлорид CrCl3. Свойства Виолетови кристали; плътност 2,76 g/cm3; т.т. 1152°С. При 600°Cсублимира в поток от хлор и се разлага в негово отсъствие на хлор и CrCl2. Разтворим във вода в присъствието на редуциращи агенти (Cr2+, Fe2+). Влизане в ... ... Wikipedia
Златен(III) хлорид - Този термин има и други значения, вижте Златен хлорид. Златен(III) хлорид ... Уикипедия
Железен (II, III) хлорид - Общо систематично наименование Железен (II, III) хлорид Традиционни наименования Железен хлорид Химична формула Fe3Cl8 Физични свойства ... Wikipedia
Железен(II) хлорид - Железен(II) хлорид (железен хлорид) FeCl2 сол. Съдържание 1 Свойства 2 Получаване 3 Приложение 4 Вижте също // ... Wikipedia
Железен(II) хлорид - Този термин има и други значения, вижте железен хлорид. Железен(II) хлорид ... Уикипедия