§ 6. Циановодородна киселина
нискотемпературни фризери с температурен режим -24С, -55С, -85С
Циановодородната киселина (циановодородна киселина) е газ или безцветна течност (т.к. 25,6 ° C, т.т. - 13,3 ° C, плътност 0,699), има миризма на горчиви бадеми, лесно се смесва със свод и с редица органични разтворители. При -13,3 ° C циановодородната киселина се втвърдява, образувайки влакнеста кристална маса.Циановодородната киселина е слаба киселина. Той се измества от солите дори от въглеродна киселина и слаби органични киселини.
Циановодородната киселина не се среща в природата в свободно състояние. Намира се под формата на химични съединения, които включват гликозиди (амигдалин, пруназин, дур-рин и др.) Амигдалин се намира в семената на горчиви бадеми, семена от праскови, кайсии, сливи, череши, в листата на лаврови череши и др. се съставя в глюкоза, бензалдехид дихидроцианова киселина. Пруназин се намира в пенсилванската череша, а дурин в просото.При изгаряне на целулоид може да се образува синила киселина. Следи от тази киселина се намират в тютюневия дим.
Солициновата киселина (цианиди) лесно се хидролизира във вода. При съхранение на водни разтвори на цианиди с достъп до въглероден диоксид те се разлагат:
Във водни разтвори се разлагат не само цианидите, но и самациновата киселина:
Приложение. Ефект върху тялотоЦиановодородната киселина и нейните соли се използват за синтеза на редица органични съединения, при извличането на злато, за дезинфекция и дезинсекция, за борба с вредителите по растенията и др.
Циановодородната киселина и нейните соли са много отровни. Токсичността на циановодородната киселина надминава много известни отрови. Следователно синилната киселинас неговите соли трябва да се работи много внимателно. Трябва да се помни, че добавянето на силни киселини към цианидите незабавно освобождава циановодородна киселина, която може да причини тежко и понякога фатално отравяне. Отравяне може да бъде причинено и от различни съединения на циановодородната киселина (цианоген хлорид, цианоген бромид и др.). Има случаи на отравяне на хора с бадемови семена. Подадена от М. Д. Швайкова (1975), смърт при възрастни може да настъпи при изяждане на 40-60 броя, а при деца - 10-12 броя бадемови семки. Когато се вдишат високи концентрации на циановодородна киселина, смъртта може да настъпи незабавно от спиране на дишането и сърцето. Като се има предвид високата токсичност на циановодородната киселина и нейните соли, е възможно да се работи с тях в лабораторията само в аспиратор с добра вентилация.
Циановодородната киселина инхибира вътреклетъчните дихателни ензими, съдържащи желязо. Когато цитохромоксидазата се инхибира от циановодородна киселина, клетките на тялото не абсорбират кислород от кръвта. В резултат на това настъпва клетъчен кислороден глад, въпреки факта, че кръвта е наситена с кислород.Цианидите също могат да блокират кръвния хемоглобин, нарушавайки неговите функции.
Циановодородната киселина може да навлезе в тялото с вдишвания въздух и частично през непокътната кожа, киселини през храносмилателния канал.
Метаболизъм , Метаболитът на циановодородната киселина е тиоцианат (роданид), който се образува в тялото, когато цианидите се конюгират със сяра под въздействието на ензима роданаза.
Откриване на синила киселина и цианид
Изолирането на циановодородна киселина и цианиди от биологичен материал се извършва чрез парна дестилация. За тази цел вземете 3-5 ml от първия дестилат в епруветка,
съдържащ 2 ml 2% разтвор на натриев хидроксид. Тъй като циановодородната киселина бързо се разлага в организма, изследването на биологичен материал за наличието на товакиселина и нейните соли е за предпочитане да се извършват веднага след аутопсията на труповете.
При отравяне с циановодородна киселина и цианидамин се извършва химико-токсикологично изследване на стомаха със съдържанието му, черния дроб и бъбреците. Поради бързото разграждане на циановодородната киселина и цианидите в тъканите на тялото, тези отрови могат да бъдат открити в съдържанието на стомаха и да не се открият в паренхимните органи.
Когато се прави заключение за отравяне с циановодородна киселина и цианиди (въз основа на резултатите от химико-токсикологичен анализ на биологичен материал), трябва да се има предвид, че цианидите в малки количества (около 6 μg%) могат да бъдат в урината на хора, които не са били изложени на тези съединения. В урината на пушачите количеството цианид може да бъде почти 3 пъти повече, отколкото в кръвта на непушачите. В кръвта цианидите могат да се образуват и посмъртно.
За откриване на циановодородна киселина в дестилатите се използват няколко реакции, от които реакцията на образуване на пруско синьо е най-убедителната. Другите реакции, описани по-долу, се използват като спомагателни реакции, а също и за откриване на цианиди в прахове, течности и други предмети.
Реакциите на циановодородната киселина и нейните соли се провеждат в течение.
Реакцията на образуване на пруско синьоОт добавянето на железен (II) сулфат към алкален разтвор на цианиди се образува железен цианид (II), който при взаимодействие с излишък от цианиди и след това с железен (III) сулфат или хлорид образува пруско синьо:
По време на образуването на пруско синьо възникват странични реакции между железни соли и алкали (образуват се железни хидроксиди).
За разтваряне на железни хидроксиди и неутрализиране на излишните алкали се добавя киселина към кисела реакция. Голям излишък от добавена киселина може да забави образуването на пруско синьо.
Извършване на реакция.Към множествомилилитра дестилат, събран в алкален разтвор, добавете 1-4 капки разреден разтвор на железен (II) сулфат и същия обем разреден разтвор на железен (III) хлорид. Сместа се разклаща добре и се загрява на пламъка на газова горелка почти до кипене.
и след това се охлажда до стайна температура и се добавя 10% разтвор на солна киселина до леко кисела реакция на лакмус. Появата на синя утайка или син цвят показва наличието на циановодородна киселина (цианиди) в дестилата.
Граница на откриване: 20 μg циановодородна киселина в 1 ml разтвор. Пределната концентрация е 1: 100 000. При количества циановодородна киселина над 30 μg в 1 ml се образува синя утайка. При наличие на 20-30 микрограма циановодородна киселина в 1 ml се появява зелено или синкаво оцветяване. При малки количества циановодородна киселина в разтвори, син цвят се появява само след 24-48 часа.При липса на синя утайка или син цвят за дълго време към сместа се добавя 5% разтвор на бариев хлорид. В този случай се утаява бариев сулфат и се получава съутаяване на пруско синьо.
Утайката от пруско синьо може да бъде представена на съдебните и следствените органи като доказателство за наличието на циановодородна киселина или цианиди в изследваните обекти.
Реакцията на образуване на железен тиоцианат.Тази реакция се основава на факта, че когато цианидите се нагряват с разтвор на амониев полисулфид, се образува тиоцианат от добавянето на разтвор на железен (III) хлорид, към който се появява кървавочервен цвят:
Провеждане на реакцията.Към 2-3 ml от тестовия разтвор се добавят 3-5 капки 10-20% разтвор на амониев полисулфид и сместа се изпарява на водна баня до малък обем. Към изпарената течност се добавя на капки 8% разтвор на солна киселина до кисела реакция (според лакмус), след което се добавя 1 капка 10% разтвор на железен (III) хлорид. Външен видкървавочервен цвят показва наличието на цианиди в разтвора. Когато оцветеният разтвор се разклати с диетилов етер, цветът преминава в етерен слой.
Граница на откриване: 10 µg циановодородна киселина в 1 ml.
Реакцията на образуване на бензидиново синьо.Медните (II) соли с цианиди образуват цианид (CN)2, чието взаимодействие със свода освобождава кислород, който окислява бензидина. Продуктът на окисление на бензидина е бензидиново синьо:
Извършване на реакцията.За извършване на тази реакция използвайте индикаторна хартия, навлажнена със смес от разтвори на меден бензидин ацетат.
В колбата се добавят 2-3 ml от тестовия разтвор, към който се добавя 1 ml 10% винена киселина. Колбата веднага се затваря със запушалка, към която е прикрепена мокра индикаторна хартия. След това колбата се загрява няколко минути на водна баня. При наличие на циановодородна киселина или нейни соли в пробата хартията посинява.
Подготовка на индикаторна хартия(вижте Приложение 1, реактив 6).
Реакция с пикринова киселина.Добавянето на пикринова киселина към цианиди произвежда сол на изопурпурова киселина с червен цвят:
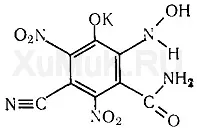
Провеждане на реакцията.Към 1 ml алкален дестилат се добавя 1 ml 0,5% разтвор на апикринова киселина и се загрява леко на водна баня. В присъствието на цианиди разтворът придобива червен цвят. Подобен цвят със спикриновата киселина дават и някои други вещества (алдехиди, ацетон, сулфити и др.). Следователно реакцията на спикринова киселина с нацианиди е значима само при липса на цианиди в дестилата.
Откриване на цианид чрез микродифузия.Циановодородната киселина и нейните соли могат да бъдат открити чрез микродифузия, която се основава на реакцията със спиридинобарбитурова киселина. Методът за откриване на цианиди чрез микродифузия е описан по-горе (виж гл.III, § 3).