Cheat Sheet - Аминокиселини
Всяко съединение, което съдържа както карбоксилна, така и амино група, еаминокиселина. Въпреки това, по-често този термин се използва за обозначаване на карбоксилни киселини, чиято аминогрупа е в a-позиция спрямо карбоксилната група.
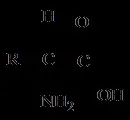
Аминокиселините, като правило, са част от полимери -протеини. В природата се срещат над 70 аминокиселини, но само 20 играят важна роля в живите организми.Есенциалнитеса аминокиселини, които не могат да бъдат синтезирани от организма от вещества, набавени с храната в количества, достатъчни за задоволяване на физиологичните нужди на организма. Есенциалните аминокиселини са дадени в табл. 1. За пациентите с фенилкетонуриятирозинътсъщо е незаменима аминокиселина (вижте Таблица 1).
Есенциални аминокиселиниR-CHNH2 COOH
Аминокиселините обикновено се наричат като заместени съответстващи карбоксилни киселини, обозначаващи позицията на аминогрупата с буквите от гръцката азбука. За най-простите аминокиселини обикновено се използват тривиални имена (глицин, аланин, изолевцин и др.). Изомерията на аминокиселините е свързана с подреждането на функционалните групи и със структурата на въглеводородния скелет. Една аминокиселинна молекула може да съдържа една или повече карбоксилни групи и съответно аминокиселините се различават по основност. Освен това една аминокиселинна молекула може да съдържа различен брой аминогрупи.
МЕТОДИ ЗА ПОЛУЧАВАНЕ НА АМИНОКИСЕЛИНИ
1. Около 25 аминокиселини могат да бъдат получени чрез хидролиза на протеини, но получената смес е трудна за разделяне. Обикновено една или две киселини се получават в много по-големи количества от останалите и тези киселини могат да бъдат изолирани доста лесно - с помощта найонообменни смоли.
2. От халогенирани киселини. Един от най-разпространените методи за синтез наa-аминокиселини е амонолизата наa-халогенирана киселина, която обикновено се получава чрез реакцията на Гел-Фолхард-Зелински:
Този метод може да бъде модифициран, за да се получи a-бромо киселина чрез малонов естер:

Аминогрупа може да бъде въведена в естера на а-халогенирана киселина с помощта на калиев фталимид (синтез на Габриел):

3. От карбонилни съединения (Синтез на Strecker). Синтезът на а-аминокиселини според Strecker се състои в реакцията на карбонилно съединение със смес от амониев хлорид и натриев цианид (това подобрение на метода е предложено от N.D. Zelinsky и G.L. Stadnikov).
Реакциите на присъединително разцепване, включващи амоняк и карбонилно съединение, дават имин, който реагира с циановодород, за да образува а-аминонитрил. В резултат на хидролизата му се образува a-аминокиселина.

Химични свойства на аминокиселините
Всички а-аминокиселини, с изключение на глицин, съдържат хирален а-въглероден атом и могат да се появят катоенантиомери:

Доказано е, че почти всички естествени a-аминокиселини имат една и съща относителна конфигурация при a-въглеродния атом. На а-въглеродния атом на (-)-серина условно е определенаL-конфигурация, а на а-въглеродния атом на (+)-серин е определенаD-конфигурация. Освен това, ако проекцията на Фишер на а-аминокиселина е написана така, че карбоксилната група е разположена отгоре, а R е отдолу, аминогрупата ще бъде отляво наL-аминокиселината и отдясно наD-аминокиселината. Схемата на Фишер за определяне на конфигурацията на аминокиселина е приложима за всички а-аминокиселини, имащи хирален а-въглероден атом.
Фигурата показва, чеL-аминокиселината може да бъде дясновъртяща (+) или лявовъртяща (-) в зависимост от природата на радикала. По-голямата част от естествено срещащите се а-аминокиселини принадлежат към сериятаL. Технитеенантиоморфи, т.е.D-аминокиселините се синтезират само от микроорганизми и се наричат "неестествени" аминокиселини.
Според (R,S) номенклатурата повечето "естествени" или L-аминокиселини имат S-конфигурация.

L-изолевцин и L-треонин, съдържащи два хирални центъра на молекула, могат да бъдат произволни членове на двойка диастереомери, в зависимост от конфигурацията при b-въглеродния атом. Правилните абсолютни конфигурации на тези аминокиселини са дадени по-долу.

КИСЕЛИННО-ОСНОВНИ СВОЙСТВА НА АМИНОКИСЕЛИНИТЕ
Аминокиселините са амфотерни вещества, които могат да съществуват като катиони или аниони. Това свойство се обяснява с наличието както на киселинни (-COOH), така и на основни (-NH2) групи в една и съща молекула. В много киселинни разтвориNH2- групата на киселината се протонира и киселината се превръща в катион. В силно алкални разтвори карбоксилната група на аминокиселината се депротонира и киселината се превръща в анион.
В твърдо състояние аминокиселините съществуват катоцвитер йони(биполярни йони, вътрешни соли). В цвитерионните йони протонът се прехвърля от карбоксилната група към аминогрупата:
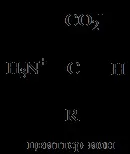
Ако аминокиселина се постави в проводяща среда и там се спусне двойка електроди, тогава в киселинни разтвори аминокиселината ще мигрира към катода, а в алкални разтвори към анода. При определена стойност на pH, характерна за дадена аминокиселина, тя няма да се придвижи нито към анода, нито към катода, тъй като всекимолекулата е под формата на цвитерион (носи както положителен, така и отрицателен заряд). Тази стойност на pH се наричаизоелектрична точка(pI) на тази аминокиселина.
Повечето от реакциите, в които аминокиселините влизат в лабораторията (invitro), са общи за всички амини или карбоксилни киселини.
1. образуване на амиди при карбоксилната група. Когато карбонилната група на аминокиселина реагира с аминогрупата на амина, реакцията на поликондензация на аминокиселината протича успоредно, което води до образуването на амиди. За да се предотврати полимеризацията, аминогрупата на киселината се блокира, така че реагира само аминогрупата на амина. За тази цел се използват карбобензоксихлорид (карбобензилоксихлорид, бензил хлороформат),tert-бутоксикарбоксазид и др.. За да реагира с амин, карбоксилната група се активира чрез третиране с етил хлороформат.Защитната групаслед това се отстранява чрез каталитична хидрогенолиза или чрез действието на студен разтвор на бромоводород в оцетна киселина.

2. образуване на амиди при аминогрупата. Когато аминогрупата на a-аминокиселина се ацилира, се образува амид.

Реакцията протича по-добре в основната среда, тъй като това осигурява висока концентрация на свободен амин.
3. образуване на естери. Карбоксилната група на аминокиселината лесно се естерифицира чрез конвенционални методи. Например, метиловите естери се получават чрез преминаване на сух газообразен хлороводород през разтвор на аминокиселина в метанол:
Аминокиселините са способни на поликондензация, което води до образуването на полиамид. Полиамидите, съставени от а-аминокиселини, се наричат пептидиилиполипептиди. Амидната връзка в такива полимери се наричапептиднавръзка. Полипептиди съсс молекулно тегло най-малко 5000 се наричат протеини. Протеините съдържат около 25 различни аминокиселини. При хидролизата на даден протеин всички тези аминокиселини или някои от тях могат да се образуват в определени пропорции, характерни за отделен протеин.
Уникалната последователност от аминокиселинни остатъци във веригата, присъща на даден протеин, се наричапървична структура на протеина. Характеристиките на усукване на вериги на протеинови молекули (взаимно разположение на фрагменти в пространството) се наричат вторична структура на протеини. Полипептидните вериги на протеините могат да бъдат свързани помежду си с образуването на амидни, дисулфидни, водородни и други връзки, дължащи се на страничните вериги на аминокиселините. В резултат на това спиралата се усуква на топка. Тази структурна характеристика се наричатретична структура на протеина. За да проявят биологична активност, някои протеини трябва първо да образуват макрокомплекс (олигопротеин), състоящ се от няколко пълни протеинови субединици.Кватернерната структураопределя степента на свързване на такива мономери в биологично активния материал.
Протеините се делят на две големи групи -фибриларни(съотношението на дължината на молекулата към ширината е по-голямо от 10) иглобуларни(съотношението е по-малко от 10). Фибриларните протеини включватколаген, най-разпространеният протеин в гръбначните животни; представлява почти 50% от сухото тегло на хрущяла и около 30% от твърдите кости. В повечето регулаторни системи на растения и животни катализата се извършва от глобуларни протеини, които се наричат ензими.