Фазови диаграми
Фазови диаграми. Тройна точка - раздел на апаратура, апаратура и информатика. Различни фази на едно и също вещество могат да бъдат в равновесие, съседни.
Различни фази на едно и също вещество могат да бъдат в равновесие, в контакт една с друга. Такова равновесие се наблюдава само в ограничен температурен диапазон и всяка температурна стойностTсъответства на собственото си наляганеP, при което равновесието е възможно. За визуално представяне на фазовите трансформации се използват фазови диаграми на състоянията, на които зависимостта между температурата на фазовия преход и налягането е посочена в координатите P, T. Такива диаграми се изграждат въз основа на експериментални данни.
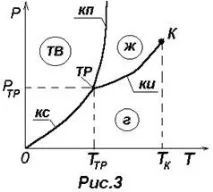
2) кривата на топене (KP ) определя условията на равновесие между твърдата и течната фази (например между лед и вода); 3) кривата на сублимация (KS ) определя условията на равновесие между твърдата и газообразната фаза (например между лед и водна пара). Всяко вещество има само една тройна точка. Тройната точка на водата имаTPP=273.16 K (илиtTP=0.01°C) иPTP=611 Pa, което съответства на 1/166 от физическата атмосфера. При тази температура и налягане водата, ледът и водните пари са в равновесие, т.е. може да остане в това състояние толкова дълго, колкото желае.
Уравнението на Клаузиус-Клапейрон изразява връзката между наклона на кривата на равновесието на две фази и топлината на фазовия преход q и промяната във фазовия обемV2-V1:
. (6)
Тази тема принадлежи към категорията:
Приборостроене и информатика
Министерство на образованието на Руската федерация.. Московска държавна академия.. Приборостроене и информатика..
Какво ще правим с получения материал:
Всички теми в този раздел:
Основните положения на молекулярно-кинетичната теория Според молекулярно-кинетичните концепции всяко тяло се състои от атоми и молекули. Тези частици са в произволно, хаотично движение, чиято интензивност зависи от температурата.
Уравнение на състоянието на идеален газ Най-простият обект, за който може да се получи уравнение на състоянието, е идеален газ. Идеален газ е този, чиито молекули имат пренебрежимо малък собствен обем.
Следователно уравнението на състоянието на един мол идеален газ е РV=RT. (4) За произволна маса m газ уравнение (4) може да се пренапише като РV=(m/M)RT или РV=nRT, (5) където n=m/M е броят на моловете. Очевидно з
Основното уравнение на молекулярно-кинетичната теория на идеален газ Нека има N молекули в съд под формата на куб със страна l. Помислете за движението на една от молекулите. Нека молекулата се движи от центъра на куба в една от 6 възможни посоки (фиг. 1), напр.
барометрична формула. Разпределение на Болцман При извеждането на уравнение (14) се приема, че външните сили не действат върху газовите молекули, следователно молекулите са равномерно разпределени в обема. Въпреки това, газовите молекули са в гравитационното поле на Земята,
Закон на Максуел за разпределението на молекулите на идеален газ по скорости В газ в равновесие ще се установи някакво стационарно (непроменящо се с времето) разпределение на молекулите по скорости, което се подчинява на добре дефинирана статия
Разпределение на Максуел-Болцман През 1866 г. Болцман (1844-1906) извежда по-общо разпределение, което включва разпределението на Максуел, наречено разпределение на Максуел-Болцман
Среден брой сблъсъци и средна дължинасвободен път на молекулите Газовите молекули, намиращи се в състояние на хаотично движение, непрекъснато се сблъскват една с друга. Молекулите изминават известно разстояние между два последователни сблъсъка.
Досега разглеждахме изключително равновесни системи, характеризиращи се при постоянни външни условия от инвариантността на параметрите (P, V, T, ) във времето и липсата на поток в системата
Дифузия Това е пренос на маса от места с по-голяма плътност
Топлопроводимост Това е преносът на топлина (вътрешна енергия) от по-горещи места към по-хладни места. Фурие (1822) установява, че количеството топлина
Вътрешно триене (вискозитет) Възниква между слоеве течност или газ, движещи се по подреден начин с различни скорости u. Благодарение на хаотичното топлинно движение, в резултат на това се извършва обмен на молекули между слоевете
Физически основи на термодинамиката Термодинамиката, подобно на молекулярната физика, се занимава с изучаването на физически процеси, протичащи в макроскопични системи, т.е. в тела, съдържащи огромен брой взаимодействащи микрочастици
Термодинамични системи. Равновесни състояния и равновесни процеси Термодинамична система ще наричаме всяко макроскопично тяло, което е в равновесие или близко до равновесие. Състоянията на всяка термодинамична система могат да бъдат
Вътрешна енергия на идеален газ. Броят на степените на свобода на една молекула. Законът за равномерното разпределение на енергията по степени на свобода Важна характеристика на термодинамичната система е нейната вътрешна енергия U - енергията на хаотичното (топлинно) движение на микрочастиците на системата (молекули, атоми, електрони, ядра и др.).
Работа и топлина Разгледайте термодинамикатасистема, при която механичната енергия не се променя, а се променя само нейната вътрешна енергия. Вътрешната енергия на затворена система (т.е. система, която не обменя
Първият закон на термодинамиката (LLT) Да приемем, че някаква термодинамична система (например газ, затворен в цилиндър под бутало), имаща вътрешна енергия U1, е получила определено количество топлина Q
Топлинен капацитет Специфичният топлинен капацитет на дадено вещество е стойност, равна на количеството топлина, необходимо за нагряване на 1 kg вещество с 1 K:
Изохоричен процес За него V=const. Диаграма на този процес (изохора)
Изобарен процес За него P=const. Диаграма на този процес (изобара)
Изотермичен процес За него Т-конст. Например, процесите на кипене, кондензация, топене и кристализация на химически чисти вещества протичат при постоянна температура, ако външното налягане е постоянно.
Адиабатен процес Това е процес, при който няма топлообмен () между системата и околната среда. К адиабатен
Кръгови процеси (цикли) Процесът, при който системата след преминаване през поредица от състояния се връща в първоначалното си състояние, се нарича кръгов процес или цикъл. На диаграмата на процеса цикълът е изобразен като затворена крива
Ентропия 4.10.1. Ентропия в термодинамиката При изучаване на PNT() беше отбелязано, че dU е полето
Вторият закон на термодинамиката (VNT) Изразявайки универсалния закон за запазване и преобразуване на енергията, първият закон на термодинамиката (PNT) не позволява да се определи посоката на процесите. Всъщност процесът на спонтанно предаване
Сили и потенциална енергия на междумолекулни взаимодействия В лекции 1-2 се изучават идеални газове, чиито молекули иматнезначителен собствен обем и не взаимодействат помежду си на разстояние. Свойства на реалните газове при високо налягане и
Уравнение на Ван дер Ваалс (VdV) В научната литература има повече от 150 уравнения на състоянието на реален газ, които се различават едно от друго. Нито едно от тях не е наистина вярно и универсално. Нека се спрем на уравнението
Изотерми на Ван дер Ваалс За фиксирани стойности на P и T уравнение (2) е уравнение от трета степен по отношение на обема на газа V и следователно може да има или три реални корена (V
Фази и фазови преходи Фазата е набор от части на система, които са идентични във всички физични, химични свойства и структурен състав. Например има твърди, течни и газообразни фази (наречени
Кристална клетка. Видове връзки между решетъчните частици Основната характеристика на кристалите, която ги отличава от течностите и аморфните твърди тела, е периодичността на пространственото разположение на частиците (атоми, молекули или йони), които изграждат вика.
Елементи на квантовата статистика Дуализмът (двойствеността) на вълните и частиците е една от основните концепции на съвременната физика. Има много полета в кристалите, които проявяват и двата аспекта - вълна и корпускула.
Фермиони и бозони. Разпределение на Ферми-Дирак и Бозе-Айнщайн Според съвременната квантова теория всички елементарни и сложни частици, както и квазичастиците се разделят на два класа - фермиони и бозони. Фермионите включват електрони, прото
Концепцията за изроденост на система от частици Система от частици се нарича изродена, ако нейните свойства се различават от свойствата на класическите системи поради квантови ефекти. Нека намерим критериите за израждане на частиците. Разпределения на ФермиДирак и Боуз-Хей
Концепцията на квантовата теория за електрическата проводимост на металите Според квантовата теория електрон в метал няма точна траектория, той може да бъде представен от вълнов пакет с групова скорост, равна на скоростта на електрона. Квантовата теория взема предвид движението
Елементи на лентовата теория на кристалите Миналия семестър бяха разгледани енергийните нива на електрон във водороден атом [вж. бележки от лекции, част III, формула (11. 14)]. Там беше показано, че енергийните стойности, които могат и
Разделяне на кристалите на диелектрици, метали и полупроводници Всички кристали се делят на диелектрици, метали и полупроводници. Разглеждане
Вътрешна проводимост на полупроводници Електрическата проводимост на химически чист полупроводник (например чист Ge или чист Si
Полупроводници с примеси 9.6.1. Донорни примеси, n-тип полупроводници Въвеждането на примеси в полупроводника силно влияе върху неговите електрически свойства. Нека разгледаме например какво се случва, ако в решетката
P-n преход В много области на съвременната електроника контактът на два полупроводника с n- и p-типове играе важна роля
Структурата на атомните ядра Ядрото е централната част на атома, в която е концентрирана почти цялата маса на атома и неговия положителен заряд. Размерът на атома е единици ангстрьоми (1A = 10-10m), а ядрата
Дефект на масата и енергия на свързване на ядрото Когато се образува ядро, неговата маса намалява: масата на ядрото Mn е по-малка от сумата от масите на съставните му нуклони с Dm - дефектът на масата на ядрото: Dm=Zmp
Ядрени сили и техните свойства В допълнение към неутроните, ядрото включва положително заредени протони и те трябва да се отблъскват, т.е. ядрото на атома трябва да бъде унищожено, но това не се случва. Оказва се, че на малки
Радиоактивност Радиоактивността е спонтанна промяна в състава на ядрото, която настъпва за време, много по-дълго от характерното ядрено време (10-22 s). Съгласихме се да обмислим това
Законът за радиоактивното разпадане Радиоактивното разпадане е статистически феномен, така че всички прогнози са вероятностни. Спонтанният разпад на голям брой атомни ядра се подчинява на закона за радиоактивния разпад
Ядрени реакции Ядрените реакции са процеси на трансформация на атомни ядра, причинени от взаимодействието им едно с друго или с елементарни частици. По правило в ядрените реакции участват две ядра.
Елементарните частици и съвременната физическа картина на света При въвеждането на понятието елементарни частици първоначално се приемаше, че има първични, а след това неделими частици, които изграждат цялата материя. До началото на 20 век, с
Взаимно преобразуване на частици Характерна особеност на елементарните частици е тяхната способност за взаимни трансформации. Общо, заедно с античастиците, са открити повече от 350 елементарни частици, като броят им продължава да расте. Голям
Античастици В микрокосмоса всяка частица съответства на античастица. Например, първата античастица - позитронът (антиелектронът) е открит през 1935 г., зарядът му е + e. Във вакуум позитронът е също толкова