Формула на живак в химията
Определение и формула на живака
Много топим метал. Плътност 13,55 g/cm 3 . Точка на топене - 38,9 o C, точка на кипене 357 o C.

Ориз. 1. Живак. Външен вид.
Химическа формула на живака
Химическият символ на живака е Hg, произлизащ от латинската дума hydrargyrum. Този химичен елемент се намира в шестия период на II група от вторичната (B) подгрупа на периодичната система. Отнася се за елементи от d-семейството. Метал. Относителната атомна маса на живака е 200,59 amu.
Електронна формула на живак
Атомът на живака се състои от положително заредено ядро (+80), вътре в което има 80 протона и 120 неутрона, а 80 електрона се движат в шест орбити.
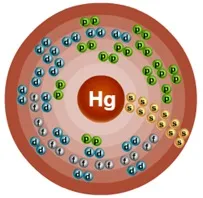
Ориз. 2. Схематична структура на атома на живака.
Разпределението на електроните в орбиталите е както следва:
Примери за решаване на проблеми
| Упражнение | Елементният състав на веществото е следният: масовата част на железния елемент е 0,7241 (или 72,41%), масовата част на кислорода е 0,2759 (или 27,59%). Изведете химичната формула. |
| Решение | Масовата част на елемента X в молекулата на състава HX се изчислява по следната формула: |
ω (X) = n × Ar (X) / M (HX) × 100%
Нека обозначим броя на железните атоми в молекулата с "x", броя на кислородните атоми с "y".
Нека намерим съответните относителни атомни маси на елементите желязо и кислород (стойностите на относителните атомни маси, взети от периодичната таблица на Д. И. Менделеев, ще бъдат закръглени до цели числа).
Ar(Fe) = 56; Ar(O) = 16
x:y = 72,41/56 : 27,59/16;
Нека приемем най-малкото число като едно (т.е. да разделим всички числа на най-малкото число 1,29):
Следователно, най-простата формула за комбиниране на желязо скислородът има формата Fe2O3.
| Упражнение | Намерете химичната формула на вещество, което съдържа 9 масови части алуминий и 8 масови части кислород. |
| Решение | За да разберете в каква връзка са химичните елементи в състава на една молекула, е необходимо да намерите тяхното количество вещество. Известно е, че за да се намери количеството на дадено вещество, трябва да се използва формулата: |
Нека намерим моларните маси на алуминия и кислорода (стойностите на относителните атомни маси, взети от периодичната таблица на Д. И. Менделеев, ще бъдат закръглени до цели числа). Известно е, че M = Mr, което означава M(Al) = 27 g/mol и M(O) = 16 g/mol.
Тогава количеството вещество на тези елементи е равно на:
n (Al) = m (Al) / M (Al);
n (Al) \u003d 9 / 27 \u003d 0,33 mol
n(O) = 8/16 = 0,5 mol
Намерете моларното съотношение:
n(Al) :n(O) = 0,33 : 0,5 = 1 : 1,5 = 2 : 3,
тези. формулата за свързване на алуминий с кислород е Al2O3.