I клас
Този клас включва ензими, които катализират редокс реакции. По време на окисляването може да настъпи или отстраняване на водород от окисленото вещество, или добавяне на кислород към окисленото вещество. В зависимост от начина на окисление се разграничават следните подкласове оксидоредуктази:
1) ДЕХИДРОГЕНАЗИ. Катализира реакции, при които водородът се отстранява от окисленото вещество. Пример:
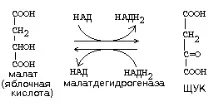
2) ОКСИГЕНАЗИ. Ензимите от този подклас катализират включването на кислород в окисленото вещество.
а)Монооксигенази- включват един кислороден атом в окисленото вещество.
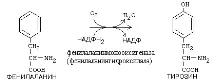
б) Диоксигенази – включват 2 кислородни атома в окисленото вещество. Често това е придружено от прекъсване на цикличната структура. На мястото на прекъсване на връзката (обозначено със стрелка на фигурата) се прикрепват кислородни атоми.
Клас II - трансферази
Те катализират преноса на химични групи от молекула на едно вещество към молекула на друго вещество.
IIIклас - ХИДРОЛАЗИ
Те катализират реакции на разкъсване на химични връзки, включващи вода.
Те катализират реакции на разкъсване на химични връзки без участието на вода.
Катализира реакциите на изомерни трансформации.
VIклас - ЛИГАЗИ (СИНТАЗИ, СИНТЕТАЗИ)
Катализира реакциите на синтез.
ОСНОВНИ СТЪПКИ НА ЕНЗИМНАТА КАТАЛИЗА
Всяка ензимна реакция протича през серия от междинни етапи. Има три основни стъпки в ензимната катализа:
Етап 1. ОРИЕНТИРАНА СУБСТРАТНА СОРБЦИЯ ВЪРХУ ЕНЗИМНО АКТИВНО МЯСТО С ОБРАЗУВАНЕ НА ОБРАТИМ E-S КОМПЛЕКС (ЕНЗИМ-СУБСТРАТ). На този етап взаимодействието на мястото на адсорбция на ензима ссубстратна молекула. В същото време субстратът претърпява конформационно пренареждане. Всичко това се дължи на появата на слаби видове връзки между субстрата и адсорбционния център на ензима. В резултат на това молекулата на субстрата се подава към каталитичния център в най-удобната за него позиция. Тази стъпка е лесно обратима, тъй като са включени само слаби видове връзки. Кинетичната характеристика на първия етап на ензимната катализа е константата на Михаелис (Km).
Етап 2. ХИМИЧНИ ТРАНСФОРМАЦИИ НА СУБСТРАТНАТА МОЛЕКУЛА В СЪСТАВА НА ЕНЗИМНО-СУБСТРАТНИЯ КОМПЛЕКС С ОБРАЗУВАНЕТО НА ЕНЗИМНИЯ КОМПЛЕКС С ХИМИЧЕСКИ ТРАНСФОРМИРАНИЯ СУБСТРАТ. На този етап някои ковалентни връзки се разкъсват и се образуват нови. Следователно този етап протича много по-бавно от 1-ви и 3-ти етапи. Скоростта на втория етап определя скоростта на цялата ензимна реакция като цяло. Това означава, че скоростта на ензимния процес като цяло се характеризира със стойността k + 2, която почти винаги е най-малката от всички конкретни константи на скоростта. Кинетичната характеристика на 2-ри етап е максималната скорост (Vmax).
Етап 3. ДЕЗОРБЦИЯ НА ГОТОВ ПРОДУКТ ОТ КОМПЛЕКСА МУ С ЕНЗИМА. Тази стъпка е по-лесна от стъпка 2. Той, подобно на 2-ри етап, също е необратим. Изключение правят обратимите ензимни реакции.