История на квантовата механика
Около осем години по-късно Нилс Бор разшири квантовата теория до атома и обясни честотите на вълните, излъчвани от атоми, възбудени в пламък или в електрически разряд. Ърнест Ръдърфорд показа, че масата на атома е почти изцяло концентрирана в централното ядро, което носи положителен електрически заряд и е заобиколено на относително големи разстояния от електрони, които носят отрицателен заряд, в резултат на което атомът като цяло е електрически неутрален.
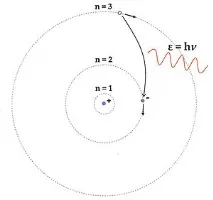
Бор предполага, че електроните могат да бъдат само в определени дискретни орбити, съответстващи на различни енергийни нива, и че "скокът" на електрона от една орбита в друга, с по-ниска енергия, е придружен от излъчване на фотон, чиято енергия е равна на енергийната разлика между двете орбити. Честотата, според теорията на Планк, е пропорционална на енергията на фотона. По този начин моделът на атома на Бор установява връзка между различните спектрални линии, характерни за вещество, излъчващо радиация, и атомната структура. Въпреки първоначалния успех, моделът на атома на Бор скоро изисква модификации, за да се премахнат несъответствията между теорията и експеримента. В допълнение, квантовата теория на този етап все още не е предоставила систематична процедура за решаване на много квантови проблеми. Стана обаче ясно, че класическата физика не е в състояние да обясни факта, че електрон, движещ се с ускорение, не пада върху ядрото, губейки енергия при излъчване на електромагнитни вълни.
Нова съществена характеристика на квантовата теория се появява през 1924 г., когато Луис дьо Бройл излага радикална хипотеза за вълновата природа на материята: ако електромагнитните вълни, като светлината, понякога се държат като частици (както показа Айнщайн), тогава частици, като електрон, при определени обстоятелства могат да се държат като вълни. Така вВ микрокосмоса границата между класическите частици и класическите вълни е изтрита. Във формулировката на де Бройл честотата, съответстваща на дадена частица, е свързана с нейната енергия, както в случая на фотон (частица светлина), но математическият израз, предложен от де Бройл, е еквивалентна връзка между дължината на вълната, масата на частицата и нейната скорост (импулс). Съществуването на електронни вълни е експериментално доказано през 1927 г. от Клинтън Дж. Дейвисън и Лестър Х. Гермър в Съединените щати и Джордж Паджет Томсън в Англия.
На свой ред това откритие води до създаването през 1933 г. от Ернст Руска на електронния микроскоп.
Една от причините за провала на Шрьодингер е, че той не е взел предвид наличието на специфично свойство на електрона, сега известно като спин (въртене на електрона около собствената си ос като връх, но такова сравнение не е напълно правилно), което по това време е било малко известно. Следващият опит е направен от Шрьодингер през 1926 г. Този път скоростите на електроните са избрани от него да бъдат толкова малки, че необходимостта от включването на теорията на относителността изчезва от само себе си. Вторият опит беше увенчан с извеждането на вълновото уравнение на Шрьодингер, което дава математическо описание на материята от гледна точка на вълновата функция. Шрьодингер нарича своята теория вълнова механика. Решенията на вълновото уравнение бяха в съгласие с експерименталните наблюдения и имаха дълбок ефект върху последващото развитие на квантовата теория. В момента вълновата функция е в основата на квантовомеханичното описание на микросистемите, подобно на уравненията на Хамилтън в класическата механика.
Шрьодингер показа, че вълновата механика и матричната механика са математически еквивалентни. Познати сега под общото наименование квантова механика, тези две теории дадоха дългоочакванообща основа за описание на квантовите явления. Много физици предпочитаха вълновата механика, защото нейният математически апарат им беше по-познат и концепциите й изглеждаха по-"физически"; операциите с матрици са по-тромави.
Малко след като Хайзенберг и Шрьодингер разработват квантовата механика, Пол Дирак предлага по-обща теория, която комбинира елементи от специалната теория на относителността на Айнщайн с вълновото уравнение. Уравнението на Дирак е приложимо за частици, движещи се с произволни скорости. Спиновите и магнитните свойства на електрона следват от теорията на Дирак без никакви допълнителни предположения. В допълнение, теорията на Дирак предсказва съществуването на античастици, като позитрон и антипротон, близнаци на частици с противоположни електрически заряди.