Как протеините против замръзване предпазват водата от замръзване, Nanotechnology Nanonewsnet

Много животни, живеещи в Далечния север, иматспециални антифризни протеини, които предотвратяват превръщането на кръвта в лед. Като се свързват с ледени кристали,молекулите на тези протеини не им позволяват да растат.
Видовете арктическа риба живеят при температури под нулата, но нито кръвта, нито други телесни течности се превръщат в лед. Рибите са студенокръвни същества, не могат да се затоплят отвътре, но имат специални протеини против замръзване. Тяхната функция е да се свързват с ледените кристали и да предотвратяват растежа им. Дълго време оставаше неясно как тези протеинови молекули различават замразената вода от течната вода.
Всекипротеин е уникална последователност от аминокиселини. Освен това всички аминокиселини могат да бъдат разделени на две големи групи: *хидрофилни** ихидрофобни. В разтвора (а по-голямата част от протеините функционират във водни разтвори), протеиновата молекула отново придобива уникална пространствена конфигурация, свивайки се на топка, превръщайки хидрофилните аминокиселини във водата и криейки хидрофобните вътре в топката.
В случай на антифризни протеини се наблюдава донякъде необичайна ситуация: те излагат много хидрофобни аминокиселини навън. В тази връзка са изказани хипотези, че тези външни хидрофобни зони отличават леда от течната вода. Но дълго време нямаше експериментално потвърждение как го правят.
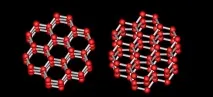
Изследователи от Института по генетика и молекулярна и клетъчна биология вСтрасбург (Франция) изследва взаимодействието наантифриз протеини с лед с помощта на методаразсейване на неутрони под малък ъгъл. Технологията направи възможно определянето на пространственото разположение на водородните атоми, което беше критично за изграждането на 3D модел "протеин върху лед". Оказа се, че групи от хидрофобни аминокиселини на повърхността на протеиновите молекули имитират подобните на лед тетраедрични структури, които водните молекули образуват, когато замръзнат. Окончателният модел, който беше построен въз основа на резултатите от експеримента, изглеждаше като шест ледени пръстена от вода, в които бяха вмъкнати протеинови молекули. Такива пръстени се образуват само в замръзнала вода и само с такива пръстени може да взаимодейства антифризният протеин.
Изграждането на пространствен модел даде отговор на въпроса как протеините на арктическите риби предотвратяват замръзването на кръвта: те просто прекъсват растежа на кристала, взаимодействайки с едната страна на молекулата с „ледената“ структура, а с другата, просто НЕ взаимодействайки с течна вода.
Има много практически приложения на антифризните протеини. Те могат да служат като опора за криохирурзите и трансплантолозите, като помагат да се запазят трансплантираните тъкани и органи в безопасност и здрави, осигурявайки им течна вода при температури под нулата. Същите протеини са полезни в хранително-вкусовата промишленост: те могат да се използват за удължаване на срока на годност на продуктите, без да се прибягва до потенциално токсични консерванти.