Калиев хидрид
 |
| калиев хидрид |
| KH |
| HK |
| бяло твърдо вещество |
| 40,1062 g/mol |
| 1,47 g/cm³ |
| 400°C |
| 37,91 J/(mol K) |
| -57,82 kJ/mol |
етанол: реагира [1]
Съдържание
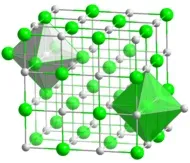
Калиевият хидрид образува безцветни йонни кристали от кубична система с NaCl тип решетка (a= 0,57 nm). Нека добре да разтворим в разтопения калий, той не се разтваря в органични разтворители. Има висока топлопроводимост.
Калиевият хидрид е йонно съединение K + H − . Неговата стопилка провежда електрически ток, при електролиза на анода се отделя водород.
Веществото е нестабилно и при нагряване се разпада на компоненти:
Калиевият хидрид има висока химична активност и е силен редуциращ агент. Окислява се от кислород:
Взаимодейства с вода:
и газообразен амоняк:
Реагира с халогени:
Образува калиев формиат с въглеродна киселина:
Взаимодейства със силициев оксид:
Калиевият хидрид се получава чрез директна реакция на разтопен калий с водород под налягане:
Тази реакция е открита от Хъмфри Дейви малко след неговото откриване на калия през 1807 г., когато той отбелязва, че металът ще се изпари в поток от водород, когато се нагрее точно под точката на кипене.
Корозивен, разяжда органичните вещества. Запалим.