Ненаситени алдехиди и кетони
Ненаситени алдехиди и кетони
Ненаситените алдехиди и кетони, в зависимост от взаимното разположение на двойните и карбонилните групи в молекулата, могат да бъдат разделени на три групи: с конюгирани (CH = CH2 -coch3 -methylivinylkeleton, Buten -3 -Ou; CH2 = chcho -акролеин, пропенел), кумулирани (ketemes CH2 = O) и изолирани и изолирани nym (CH2 = chch2 CH2 CH2 CO CH3) връзки. От тях най-голям интерес представляват съединения с конюгирани връзки, особено акролеин и кротоналдехид.
За някои ненаситени алдехиди и кетони са запазени емпирични (акролеин) или рационални (метил винил кетон) имена. Съгласно номенклатурата на IUPAC позицията на двойната връзка и карбонилната група се обозначава с цифри.
Най-важните представители на ненаситените алдехиди са акролеинът CH2=CH-CHO и кротоналдехидът CH3-CH=CH-CHO.
Има няколко начина за получаване на акролеин:
1.Алдолна кондензация на формалдехид с ацеталдехид
Хидроксипропионалдехидът допълнително претърпява дехидратация:
2.Директно каталитично окисляване на пропилен
3.Дехидратация на глицерол
Акролеинът се използва за производството на пластмаси, които са много твърди. Когато акролеинът се кондензира с пентаеритритол, се получават полимери, които приличат на стъкло. Акролеинът се използва като изходен материал за синтеза на глицерол.
Кротоналдехидът се получава чрез кротонна кондензация на ацеталдехид (виж Лекция No 24). Използва се за получаване на маслен алдехид, бутанол, маслена киселина, както и малеинов анхидрид.
Акролеин, кротоналдехид и други ненаситени съединения с конюгирани двойни и карбонилни връзки се характеризират с реакциихарактеристика на алкени и алдехиди. Взаимното влияние на двойната връзка и карбонилната група се отразява в някои характеристики, например:
1. Редът на свързване на HBr не съответства на правилото на Марковников

2. Циановодородната киселина е прикрепена към акролеина при карбонилната група:
3. Натриевият хидросулфит е свързан не само към карбонилната група, но и към двойната връзка:
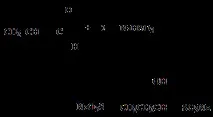
Метилвинилкетонът е най-простият представител на ненаситените кетони. Съществува под формата на два изомера:
Метил винил кетон се произвежда основно по два начина:
1. Хидратиране на винилацетилен.
2. Кондензация на формалдехид с ацетон:
Метилвинилкетонът проявява свойствата както на кетони, така и на алкени. Лесно полимеризира до прозрачна, безцветна стъкловидна маса, използвана в производството на пластмаси.
Кетените са съединения, съдържащи групата >C=C=O. По структура те наподобяват ненаситените кетони. Най-простият кетен CH2 =C=O може да се получи от бромид на бромооцетна киселина под действието на цинков прах:
В промишлеността кетенът се получава чрез пиролиза на ацетон.
и дехидратация на оцетна киселина в присъствието на киселинен тип катализатори:
CH3 COOH + H + ® CH3COO + H2 ® CH3 C + =O ® CH2 =C=O + H +
Кетените реагират изключително лесно с вода:
В промишлеността от кетен се получават оцетна киселина, оцетен анхидрид, етилацетат, дикетен и други вещества, които са междинни продукти при производството на багрила и лекарства.
Кетенът лесно полимеризира до образуване на дикетен:
Дикетенът реагира с вода, алкохоли, амини:
Ароматни алдехиди и кетони
Ароматните алдехиди и кетони се характеризират с наличиетокарбонилна група, свързана с въглерода на бензеновото ядро или странична верига. Алдехидите с карбонилна група от първия тип се наричат според съответните ароматни киселини, а с карбонилна група в страничната верига - като арил-заместени мастни алдехиди.
Кетоните са чисто ароматни (дифенилкетон или бензофенон) и мастно-ароматни (метилфенилкетон или ацетофенон).
Методи за получаване на ароматни алдехиди
Много ароматни алдехиди могат да бъдат получени по методите, описани за мастните алдехиди (лекция № 23): окисление на първични алкохоли, суха дестилация на калциеви соли на ароматни и мравчени киселини, синтези с реактиви на Гриняр и др.
1. Окисляване на ароматни въглеводороди.
Важен метод за синтез на ароматни алдехиди (по-специално бензалдехид) е окисляването на въглеводороди с атмосферен кислород върху катализатор (V2 O5, MnO2):
Методът има както лабораторно, така и индустриално значение.
2. Формилиране на ароматни въглеводороди.
За ароматните серии са известни реакции на директно въвеждане на алдехидната група, които нямат аналози в мастната серия (реакция на Гутерман-Кох):
Реакцията се катализира от медни и алуминиеви хлориди. Предполага се, че формил хлорид HCOCl, който не съществува в свободна форма, се образува като междинен продукт. Бензолът влиза в тази реакция много слабо, неговите хомолози дават добри добиви (50-60%).
3. Хидролиза на гем-дихалогенопроизводни.
Има начин за получаване на бензалдехид чрез бензилиден хлорид C6 H5 CHCl2:
толуен хлорид бензилиден бензалдехид
Хидролизата се извършва в присъствието на катализатор (Fe).
Методи за получаване на ароматни кетони
За да получите ароматкетони, приложими са много методи за получаване на мастни кетони (окисление на вторични алкохоли, дестилация на калциеви соли на ароматна и всяка друга киселина, с изключение на мравчена киселина - виж Лекция № 23).
Реакция на Фридел-Крафтс. Като изходни материали могат да се използват ароматни въглеводороди, фенолни етери:
бензоил бензофенон хлорид
Реакцията се катализира от алуминиев хлорид.
Химични свойства на ароматните алдехиди
Ароматните алдехиди влизат в повечето от реакциите, присъщи на мастните алдехиди. Специфичните реакции на ароматните алдехиди са както следва:
1. Реакция на Cannizzaro.
В присъствието на воден или алкохолен разтвор на основа (50%) ароматните алдехиди могат да диспропорционират, образувайки съответния алкохол и киселинна сол (реакция на Канизаро):
бензалдехид калиев бензоат бензилов алкохол
Повечето мастни алдехиди се подлагат на осмоляване при условията на реакцията на Cannizzaro, но ако алдехидът няма водороден атом в a-позиция, тогава реакцията протича доста гладко. Механизмът на реакцията е както следва:
2. Бензоинова кондензация. Под действието на цианиден йон две молекули ароматен алдехид могат да кондензират, за да образуват а-хидроксикетон. Тъй като най-простото съединение, образувано от кондензацията на бензалдехид, се нарича бензоин, тази последователност от реакции се нарича бензоинова кондензация:
Реактивоспособността на ароматните алдехиди и кетони зависи от заместителите в ароматното ядро. По този начин наличието на електрон-оттеглящи групи (NO2 -) повишава реактивността на карбонилната група. Пространственият фактор също е от голямо значение: заместителят (tert-С4 H9 -, SO3 H-) в орто позицияароматното ядро намалява реактивността.
Повечето ароматни кетони реагират с производни на хидроксиламин и хидразин по обичайния начин:
От всички азотни производни на кетоните най-голям интерес представляват оксимите. Оксимите на чисто ароматни несиметрични кетони съществуват в две геометрични изомерни форми, син- и анти-:
От всички азотни производни на кетоните най-голям интерес представляват оксимите. Оксимите на чисто ароматни несиметрични кетони съществуват като две геометрични изомерни форми, син- и анти-. Син-формата се счита за изомер, съдържащ по-малък радикал в цис-позиция с хидроксилната група на оксима. По-устойчива е анти-формата. Получава се от син формата чрез действието на киселини. Подобно явление е известно и за ароматните алдехидни оксими: