НЕНАСИТЕНИ ВЪГЛЕВОДОРОДИ ОТ АЦЕТИЛЕНОВИЯ РЕД
Алкините са алифатни ненаситени въглеводороди, в молекулите на които има една тройна връзка между въглеродните атоми.
Въглеводородите от ацетиленовата серия са дори по-ненаситени съединения от съответните им алкени (със същия брой въглеродни атоми). Това може да се види от сравнение на броя на водородните атоми в серията:
C2H6 C2H4 C2H2
етан етилен ацетилен
Алкините образуват своите хомоложни серии с общата формула, както при диеновите въглеводороди СnH2n-2
4.1. СТРУКТУРА НА АЛКИНИ
Първият и основен представител на хомоложната серия от алкини е ацетилен (етин) C2H2. Структурата на неговата молекула се изразява с формулите:
N—CêC—N или N:C.C:N
структурна електроника
формула формула
По името на първия представител на тази серия - ацетилен - тези ненаситени въглеводороди се наричат ацетилен.
В алкините въглеродните атоми са в трето валентно състояние (spхибридизация). В този случай между въглеродните атоми възниква тройна връзка, състояща се от една s- и две p-връзки. Дължината на тройната връзка е 0,12 nm, а енергията на нейното образуване е 830 kJ/mol. Моделите на пространствената структура на ацетилена са показани на фиг. 1.
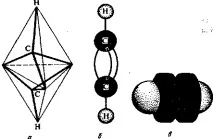
Фиг. 1. Модели на пространствената структура на ацетиленовата молекула:
а - тетраедърен;b -топка и стик; в – според Бриглеб
4.2. НОМЕНКЛАТУРА И ИЗОМЕРИЯ
Номенклатура. Според систематичната номенклатура ацетиленовите въглеводороди се наименуват чрез заместване на наставката-anв алканите с наставката-yn. Съставът на основната верига трябва да включва тройна връзка, която определя началото на номерирането. Ако една молекула съдържа както двойна, така и тройна връзка, тогава предпочитанието за номериране се дава на двойната връзка:
Според рационалната номенклатура алкиновите съединения се наричат ацетиленови производни.
Ненаситените (алкинови) радикали имат тривиални или систематични имена:
Изомерия. Изомерията на алкиновите въглеводороди (както и на алкеновите въглеводороди) се определя от структурата на веригата и позицията на кратната (тройна) връзка в нея:
Ацетиленът в промишлеността и в лабораторията може да се получи по следните начини:
1. Високотемпературно разлагане (крекинг) на природен газ - метан:
2. Водно разлагане на калциев карбид CaC2, който се получава чрез синтероване на негасена вар CaO с кокс:
CaO + 3C2500°C® CaC2 + CO
3. В лабораторията ацитиленовите производни могат да бъдат синтезирани от дихалогенирани производни, съдържащи два халогенни атома при един или съседни въглеродни атоми чрез действието на алкохолен разтвор на основа:
4.4. ФИЗИЧНИ И ХИМИЧНИ СВОЙСТВА
физични свойства. Ацетиленовите въглеводороди, съдържащи от два до четири въглеродни атома в молекула (при нормални условия), са газове, започвайки с C5H8 - течности и висши алкини (с C16H30 и по-високи) - твърди вещества. Физичните свойства на някои алкини са показани в табл. 1.
Таблица 1. Физични свойства на някои алкини
| Име | Формула | tpl,°С | tkip,°С | d 20 4 |
| Ацетилен (етан) | HCєCH | - 81,8 | -84,0 | 0,6181* |
| Метилацетилен (пропин) | HCєІ—CH3 | -101,5 | -23.2 | 0,7062** |
| Етилацетилен (бутин-1) | HCєС—С2Н5 | -125,7 | +8,1 | 0,6784 |
| Symm-Диметилацетилен |
(бутин-2)
*При -32 °C,
**При температура - 50 °С.
Химични свойства. Химичните свойства на алкините се определят от тройната връзка, характеристиките на нейната структура. Алкините са способни да влизат в реакции на добавяне, заместване, полимеризация и окисление.
Реакции на присъединяване. Като ненаситени съединения, алкините участват предимно в реакции на присъединяване. Тези реакции протичат на стъпки: с добавянето на една молекула от реагента, тройната връзка първо се превръща в двойна връзка, а след това, докато добавянето продължава, в единична връзка. Изглежда, че алкините, имащи две p-връзки, трябва да бъдат много по-активни в реакциите на електрофилно присъединяване. Но не е така. Въглеродните атоми в алкините са по-близо един до друг, отколкото в алкените и са по-електроотрицателни. Това се дължи на факта, че електроотрицателността на въглеродния атом зависи от неговото валентно състояние. Следователно p-електроните, които са по-близо до въглеродните ядра, проявяват малко по-малка активност в реакциите на електрофилно присъединяване. В допълнение, близостта на положително заредените атомни ядра, които могат да отблъснат приближаващите се електрофилни реагенти (катиони), засяга. В същото време алкините могат да влизат в реакции на нуклеофилно присъединяване (с алкохоли, амоняк и др.).
1.Хидрогениране.Реакцията протича при същите условия катокакто в случая на алкени (катализатори Pt, Pd, Ni). Когато алкините се редуцират, първо се образуват алкени, а след това алкани:
2.Халогениране.Тази реакция протича с по-бавна скорост, отколкото в серията етиленови въглеводороди. Реакцията също протича на стъпки:
Br2 Br2 HCєCH —®CHBr=CHBr —®CHBr2—CHBr2 1,2-дибромоетан 1,1,2,2-тетрабромоетан
3.Хидрохалогениране.Реакциите на присъединяване на халогеноводороди, подобно на халогени, протичат главно според механизма на електрофилно присъединяване:
HCl HCєCH + HCl —® H2C=CHCl —® H3C—CHCl2 хлороетен 1,1-дихлороетан (винил хлорид)
Втората молекула халогеноводород се добавя в съответствие с правилото на Марковников.
4.Присъединяване на вода (реакция на M.G.Kucherov,.1881). Катализатор с живачна сол:
HgSO4 y HCєCH + HOH ——® ъ H2C=CH—OHъ ® H3C—C=O l s \ H винилоцетен алкохол алдехид (междинен нестабилен продукт)
Нестабилен междинен продукт, винилов алкохол, се пренарежда, за да образува ацеталдехид.
5.Добавяне на синила киселина:
HCєCH + HCNкат.® H2C=CH—CN акрилонитрил
Акрилонитрилът е ценен продукт. Използва се като мономер за производството на синтетично влакно -нитрон.
6.Добавяне на алкохолВ резултат на тази реакция се образуват винилови етери(реакция на А. Е. Фаворски):
Добавянето на алкохоли в присъствието на алкохолати е типична реакция на нуклеофилно присъединяване.
реакции на заместване. Водородните атоми в ацетилена могат да бъдат заменени с метали (реакция на металиране). В резултат на това се образуват метални производни на ацетилена -ацетилениди.Тази способност на ацетилена може да бъде обясненапо следния начин. Известно е, че въглеродните атоми на ацетилена, намиращи се в състояние на sp-хибридизация, се отличават с повишена електроотрицателност (в сравнение с въглеродите в други хибридни състояния). Следователно електронната плътност на C–H връзката е донякъде изместена към въглерода и водородният атом придобива известна подвижност:
Но тази „мобилност“, разбира се, е несравнима със „свободата“ на протона в реалните киселини: солната киселина, например, е почти 1033 пъти по-силна в киселинността от ацетилена. Но дори такава подвижност на водорода е достатъчна, за да бъде заменен от метал в алкална среда. И така, под действието на амонячен разтвор на сребърен оксид върху ацетилен се образува сребърен ацетиленид:
HCєCH + 2[Ag(NH3)2]OH ® Ag—CєC—Ag + 4NH3 + 2H2O сребърен ацетиленид
Със сухите ацетилиди трябва да се работи много внимателно: те са силно експлозивни.
реакция на изомеризация. Ацетиленовите въглеводороди, като алкани и алкени, са способни на изомеризация с изместване на тройна връзка:
полимеризационни реакции. Ацетиленът, в зависимост от условията на реакция, може да образува различни продукти на полимеризация - линейни или циклични:
Cu2Cl2 HCєCH + HCєCH —®HCєCH—CH=CH2 80°C винилацетилен (бутен-1-в-3)
Тези вещества са от голям интерес. Например, когато към винилацетилена се добави хлороводород, се образува хлоропрен, който се използва като мономер при производството на хлоропренов каучук:
Окислителна реакция. Ацетилените лесно се окисляват. В този случай молекулата се разпада на мястото на тройната връзка. Ако ацетиленът премине през окислител (воден разтвор на калиев перманганат), тогава разтворът бързо става безцветен. Тази реакция е качествена за множествени (двойни и тройни) връзки:
На пъленИзгарянето на ацетилен във въздуха произвежда два продукта, въглероден оксид (IV) и вода:
При непълно изгаряне се образува въглерод (сажди):
4.5. ИНДИВИДУАЛНИ ПРЕДСТАВИТЕЛИ
Ацетиленът е ценен продукт за химическата промишленост. От него се получават синтетичен каучук, ацеталдехид и оцетна киселина, етилов алкохол и много други вещества.
Винилацетилен (бутен-1-в-3) HCєC-CH=CH2 е газ с неприятна миризма. При редукция образува бутадиен-1,3, а при добавяне на хлороводород - 2-хлорбутадиен-1,3 (хлоропрен).