Осмотично налягане и неговото измерване
Инструментът, използван за количествено изследване на осмозата, се наричаосмометър. Най-простият осмометър е съд 1, чието дъно е полупропусклива преграда. Към съда е заварена тънка капилярка. Съд 1 съдържа разреден захарен разтвор. Полупропускливата преграда (дъното на съд 1) може да пропуска само водни молекули (но не и захарни молекули!). Ако съд 1 се спусне в чаша 2, пълна с вода, тогава водните молекули ще дифундират в съд 1, където концентрацията на водни молекули е по-малка, отколкото в чаша 2.
С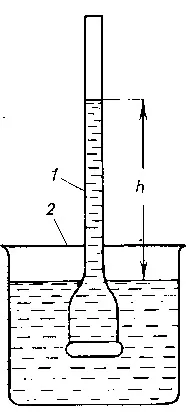
Фигура 1. Най-простото устройство за измерване на осмотично налягане: 1 - вътрешно стъкло; 2 - външно стъкло.
Благодарение на осмозата, нивото на разтвора в съд 1 се повишава, създавайки допълнително налягане, което предотвратява осмозата. При определена височина h на стълба течност в съд 1 допълнителното налягане достига стойност, при която осмозата спира. Равновесието се установява между разтвор с дадена концентрация и чист разтворител, разделени от полупропусклива преграда. Чрез увеличаване на налягането в съд 1 отвън водата може да бъде принудена да премине от съд 1 към външен съд 2. В този случай концентрацията на разтвора в съд 1 ще се увеличи, докато достигне стойност, съответстваща на повишеното налягане; се установява ново равновесие между разтвора и разтворителя.
Равновесието между разтвор с дадена концентрация и чист разтворител, отделен от полупропусклива преграда, съответства на определено хидростатично налягане в съд с разтвор.
Хидростатичното налягане, равно на височината h, което предотвратява еднопосочната дифузия на разтворителя, е числено равно на осмотичното налягане πosm на разтвора.
През 1887 г. ботаникът Пфефер експериментално установи два модела, които управляват осмотичното налягане на неелектролит.
1. В разредени разтвори на неелектролит при дадена температура осмотичното налягане е право пропорционално на концентрацията
2. При същата концентрация C (mol / l), осмотичното налягане на разреден разтвор е право пропорционално на абсолютната температура
Вант Хоф обърна внимание на аналогията между законите на Пфефер и газовите закони на Гей-Лусак и Бойл-Мариот. Анализирайки цифровите данни, той стигна до извода, че стойността на осмотичното налягане може да се изчисли по следната формула:
където C е концентрацията на вещество в разтвор, R е универсалната газова константа, T е абсолютната температура.
Този израз се нарича закон на Вант Хоф за осмотичното налягане. Ето формулировката на закона, дадена от van't Hoff:
Осмотичното налягане на разреден неелектролитен разтвор е равно на налягането, което би произвело разтвореното вещество, ако беше в газообразно състояние при същата температура и заемаше обем, равен на обема на разтвора.
Но въпреки сходството с уравнението на състоянието на идеалните газове, аналогията между осмотичното и газовото налягане е случайна.
Биологичните течности (урина, плазма, слюнка, мляко и др.) съдържат големи количества неорганични и органични вещества под формата на молекули, йони и колоидни частици. Тяхната обща концентрация се наричаосмотична концентрация (или осмоларност).и именно тази стойност трябва да се използва в уравнението на Вант Хоф.
Осмоларната концентрация е общото моларно количество на всички кинетично активни, т.е. способни на независимо движение, частици, съдържащи се в 1 литър разтвор, независимо от тяхната форма, размер и природа.
Осмоларната концентрация на разтвор е свързана с неговата моларна концентрация чрез изотоничния коефициент cosm =ic(x). Това е много важно да се има предвид при приготвянето на физиологични разтвори. Осмотичните свойства на тъканите също трябва да се вземат предвид в медицината при интравенозни инфузии на лекарства. Инжектираният разтвор не трябва да бъде токсичен и освен това е необходимо осмотичното му налягане да е същото като това на кръвната плазма, с други думи инжектираният разтвор трябва да има същото осмотично налягане. Например, така нареченият физиологичен разтвор, който може да се прилага интравенозно на човек в големи количества, е изотоничен разтвор на натриев хлорид. При приготвянето на солеви разтвори трябва да се вземат предвид техните осмотични свойства.
Ролята на осмотичните явления в различни физиологични процеси е изключително голяма. Постоянността на осмотичното налягане (изоосмия) на определени физиологични среди (плазма, вътреклетъчна течност, урина и др.) е основно физикохимично изискване на хомеостазата. Осмотичното налягане на човешката кръвна плазма е около 8 атмосфери, при рибите е ≈ 15, при някои растения може да достигне 100, а при покълващите семена до 400 атмосфери. Такива високи стойности на осмотичното налягане се постигат поради общия ефект на разтворените неорганични вещества. В плазмата най-важният компонент е NaCl.
Делът на ВМС - протеини - представлява малка част от общото налягане, нареченоонкотично налягане. Стойност на онкотичното наляганекръв, причинена от албумини и глобулини, е 0,03 - 0,04 atm. Въпреки това, този незначителен компонент на общото осмотично налягане играе основна роля в някои физиологични процеси.
Осмотичният метод е приложим и за определяне на молекулното тегло на високомолекулни съединения. Зависимостта на осмотичното налягане на разтвореното вещество от неговата концентрация се описва със съотношението
където g е масата на веществото в грамове, M е моларната маса на полимера.
За електролити, в чиито разтвори броят на частиците се увеличава по време на дисоциацията на молекулите, Вант Хоф предложи да се използва изотоничен коефициент i, който отчита промяната в броя на частиците в разтвора. Физическото значение на този коефициент е следното:
i = брой на всички частици в разтвора/брой на първоначалните частици
За неелектролитни разтвори, i = 1, а за електролитни разтвори, поради дисоциацията на техните молекули, i>gt; 1:
Ако има процес на асоцииране на частици в разтвора, тогава i Извън; πlook(int.) > виж (външен).
В резултат на ендосмозата водата дифундира в клетката, настъпва подуване на клетката с появата на стресово състояние на клетката, наречено тургор. В растителния свят тургорът помага на растението да поддържа изправено положение и определена форма.
Ако разликата в концентрациите на външния и вътрешния разтвор е достатъчно голяма и силата на клетъчната мембрана е малка, тогава ендосмозата води до разрушаване на клетъчната мембрана и клетъчен лизис. (Припомнете си, че лизисът е унищожаване, разпадане, разтваряне на клетки).
Ендосмозата е причина за хемолиза (хематолиза) - разрушаване на червените кръвни клетки с освобождаване на хемоглобин в околната среда. Обикновено хемолизата завършва жизнения цикъл на еритроцитите (приблизително 125 дни) и се появява в тялотохора и животни непрекъснато. Патологичната хемолиза възниква под въздействието на хемолитични отрови, студ, някои лекарствени вещества и други фактори.
В допълнение към ендосмозата е възможна екзосмоза:
Екзосмозата е движението на разтворител от осмотична клетка в околната среда.
В резултат на екзосмозата водата дифундира от клетката в плазмата и настъпва компресия и набръчкване на клетъчната мембрана, наречена плазмолиза. Екзосмоза възниква, когато клетката е в хипертонична среда. Феноменът на екзосмозата се наблюдава например, когато горските плодове или плодовете се поръсват със захар, а зеленчуците, месото, рибата - със сол. В този случай консервирането на храната възниква поради унищожаването на микроорганизмите поради тяхната плазмолиза.
Всяко нарушение на осмотичното налягане в тъканите причинява различни заболявания (например, отокът е свързан с нарушение на осморегулацията).
Основната задача на осморегулацията се изпълнява от бъбреците. Осмотичното налягане на урината обикновено е много по-високо от това на кръвната плазма, което осигурява активен транспорт от кръвта до бъбреците. Осморегулацията се осъществява под контрола на ензимни системи. Нарушаването на тяхната дейност води до патологични процеси. Така например при нефрит осмотичното налягане на урината може да бъде по-ниско от това на кръвта, което ще доведе до обратен транспорт на вещества.