Осмотично налягане на биополимерни разтвори
Осмотичното налягане на разредените разтвори на IUD се подчинява на закона на van't Hoff. С увеличаване на концентрацията на HMS се наблюдават отклонения от този закон: реалното осмотично налягане става по-високо от теоретичното, изчислено по уравнението (фиг. 5).
Това явление се дължи на факта, че в HMS разтворите не само самите макромолекули са кинетично независими единици, но и техните отделни сегменти, които имат относителна подвижност. Топлинното движение на сегменти от макромолекули се наричаМикро-Брауново движение.Броят на подвижните сегменти се увеличава нелинейно с увеличаване на концентрацията на ВМС. За изчисляване на осмотичното налягане на разтворите на HMS се използва уравнението на Халер: (2), където γ е масовата концентрация на полимера;Mе средната моларна маса на полимера, g/mol;bе вирусен коефициент, който взема предвид формата на молекулата и степента на нейната асиметрия.
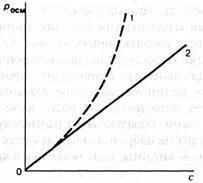
Ориз. Фиг. 5. Зависимост на осмотичното налягане от концентрацията на разтвора: 1 — разтвор на IUD; 2 - разтвор на неелектролит с ниско молекулно тегло
В сложните биологични системи общото осмотично налягане се създава както от нискомолекулни електролити и неелектролити, така и от биополимери. Компонентът на общото осмотично налягане, което се дължи на наличието на протеини и други колоидни частици, се наричаонкотично налягане.Делът на онкотичното налягане е сравнително малък: той е приблизително 0,5% от общото осмотично налягане (около 3,1 kPa), но отклонението на тази стойност от нормата води до сериозни нарушения във функционирането на тялото. Известно е, че в артериалната част на капилярите хидростатичното налягане е по-голямо от онкотичното, докато във венозната част е по-малко. Това осигурява движението на свободната от протеини част от плазмата в първия случай в междуклетъчната течност,а във втория – в обратна посока (фиг. 6).

Ориз. 6. Осмотично равновесие между плазма и междуклетъчна течност
Мембранен баланс
Теорията за мембранното равновесие е създадена през 1911 г. от английския физикохимик Ф. Донан. Селективната пропускливост на клетъчните мембрани причинява специално преразпределение на електролитите от различните й страни, известно каторавновесие на Донан.То се описва със следното уравнение: (3)
къдетоx- броят на йоните, които са преминали вътре, когато мембраната контактува с междуклетъчната течност; ceh - концентрация на йони в междуклетъчната течност (от английскивъншен —външен);stе концентрацията на йон във вътреклетъчната течност (от английскиinternal- вътрешен).
Ако преди контакт на мембраната с външния разтвор cex>gt; cin, тогава уравнение (3) може да се трансформира, както следва:
Анализът на този израз показва, че при това условие електролитът ще бъде разпределен равномерно от различните страни на мембраната. За cex = cin уравнение (3) се трансформира по различен начин:
В този случай 1/3 от йоните се движат вътре в клетката, докато в отсъствието на протеин във вътреклетъчната течност, при cex =cxn, няма да се наблюдава насочен трансфер на йони. Дори и с всички