Приложения на реакциите в синтеза на лекарствени вещества
1) Добавяне на бромкъм двойната връзка на натриев 2-пропенесулфонат във вода (синтезунитиол):
Използването наелектрохимичен метод, при който бромът реагира с алкен в момента на утаяване на анода по време на електролиза на неговите соли, позволява да се намали консумацията на бром, да се реши проблемът с неговото съхранение и натоварване и да се увеличи добивът на целевия продукт до 94%.
2) Добавяне на бромкъм двойната връзка на стероиди в бензенов разтвор в присъствието на алкохолен разтвор на НС1 (синтезпреднизолон).
3) Бромиране на холестерол-бензоат(синтез на витамин D3)N-бромо сукцинимидпри осветяване с кварцова лампа и нагряване:
Вместо N-бромосукцинимид могат да се използват rидантоин(гликолил урея) и 5,5-диметилхидантоинпод формата на дибромо-заместен.
4) Хлориране на 1,1,2-три-р-анизил-етилен(синтез на хлортрианизен) с разтвор на хлор в тетрахлорметан (SR-бензилхалогениране):
5) Хетеролитично присъединяване на бромоводородкъм двойната връзка:
6) ДобавянеHIв среда на оцетна киселина към ненаситени висши киселини, получени от синапено масло (препарат с калций):
7) Хомолитично добавяне на бромоводородкъм алил бромид или алил хлорид (синтез на инхалационен анестезиолог - циклопропан):
Активирането се извършва с бензоил пероксид и UV светлина.
8)Хипохлориране на винилхлоридвъв водна среда (cсинтез на хлороацеталдехид припроизводство нанорсулфазол):
9) Хипохлорирането на стирен(получаване на хлорхидрин при производството на левомицетин) е един от малкото примери за синтез на органично съединение в химическата промишленостчрезнепрекъснат метод:
10) Метоксихлориране на стирен(синтезлевомицетин) с хлор в метанол (стирен хлорохидрин метилов естер):
V. Халогениране на карбонилни съединения
1. Радикално халогениранена алдехиди и кетони почти винаги давасмес отпродукти. За повишаване населективносттана реакцията се използват специфични халогенни носители (сулфурилхлорид, N-бромосукцинимид и др.):
В ароматните алдехидипонякога водородният атом на алдехидната група е заменен.
2. Хетеролитното халогениранена алдехиди и кетони (с изключение на флуориране) в присъствието на киселини и основи преминава в -позиция по отношение на карбонилната група:
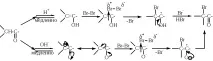
Доказателствоза изложения механизъм е следното: а) реакцията има първи ред по отношение на субстрата и нулев ред по отношение на халогена (т.е. първият етап ограничава скоростта на процеса); б) при същите условия скоростта на реакцията е еднаква за хлориране, бромиране и йодиране; в) скоростта на реакцията зависи от киселинността на средата.
При условията накиселинна катализа, реакцията може да бъде спряна след заместване на един водороден атом с халоген. В присъствието наоснови, всички водородни атоми при един от -въглеродните атоми се заместват с халоген. Ако метилов радикал е прикрепен към карбонилната група, протичахалоформна реакция.
Халоформната реакция–е реакция на халогениране на метилкарбонилни съединения в алкална среда, при която всички водородни атоми в метиловата група се заместват с халоген, последвано от разцепване на С-С връзката и образуване на халоформа.
Причината за полихалогенирането е повишената способност на α-халокарбонилните съединения даенолизация и, следователно, до реакцията на халогениране.
1) Бромиране на пропиофенон и подобни вещества (3,4-дихидроксиацетофенон и др.)при синтеза на ефедрин, адреналин и др.:
-Бромирането на m- и p-нитроацетофенон(получаване на мезатон и хлорамфеникол) се извършва в дихлороетан при 30-40 ° C:
3)Хлороформътсе получава от ацетон или етанол и белина. В този случай алкохолът първо се окислява до ацеталдехид, превръща се в хлорал и след това се разделя с калциев хидроксид до хлороформ и калциев формиат:
Хлоралът, образуван като междинен продукт, е ценен реагент в органичния синтез, а неговият хидрат (хлоралхидрат) е хипнотично лекарство.
Електрохимичният методза получаване на хлороформ е най-модерният. Алкохолът или ацетонът се смесват с разтвор на калиев или натриев хлорид и се подлагат на електролиза. Полученият натриев хипохлорит окислява и халогенира субстрата:
-Йодоформният тесте пример за използване на халоформната реакция за аналитични цели за откриване на CH3CO и CH3CHOH групи. Реагентът е разтвор на йод в основа, който едновременно окислява първични и вторични алкохоли и йодира карбонилното съединение. Полученият йодоформ има специфична миризма: