Проблемен урок на тема - Електролитна дисоциация - (8 клас)
Раздели: Химия
Въпросът за електролитната дисоциация на веществата се изучава в 8 клас в темата "Разтваряне. Разтвори. Свойства на електролитни разтвори."
Електролитната дисоциация се изучава на примера на вещества с йонни и ковалентни полярни връзки. Обикновено се демонстрират експерименти, свързани само с електропроводимостта на електролитни разтвори и стопилки. Тези експерименти пораждат погрешното схващане сред учениците, че разтворите на вещества във всякакви разтворители провеждат електрически ток. Това означава, че електролитната дисоциация на веществата се наблюдава, когато веществата се разтварят във всякакви разтворители.
За да предотвратим такава грешка, можем да започнем да разглеждаме въпроса за електролитната дисоциация на вещества с йонни и ковалентни полярни връзки, без да демонстрираме експерименти с електрически ток. Първо, с помощта на химични експерименти убедете учениците, че съединенията с йонни и ковалентни полярни връзки се разлагат на йони във воден разтвор. И трябва да се провеждат експерименти с електрически ток като доказателство за наличието на йони във водни разтвори на електролити.
Следователно в този случай е възможно да се създаде проблемна ситуация на конфликт между практически постигнатия резултат и липсата на знания за неговата теоретична обосновка.
Това поражда интерес у учениците към изучавания въпрос и желание за обяснение на наблюдаваните явления, както и желание за придобиване на нови знания.
Цели на урока:
- Дайте концепцията за електролити и неелектролити; разгледайте механизма на дисоциация на вещества с различни видове връзки; посочете ролята на водните молекули в дисоциацията на веществата; въведе понятието "степен на дисоциация" и класификацията на електролитите.
Оборудване и реактиви:
- Концентрирана H2SO4; H2O; Ca(OH)2 кристален; метилоранж върху ацетон; кристален фенолфталеин; ацетон; дехидратиран CuSO4; железни пирони; епруветки; устройство за определяне на електропроводимостта на разтвори с електрическа крушка; кристален NaCl и разтвор; Разтвори на Ca(OH)2 и H2SO4.
Урокът започва с организационен момент: взаимно поздравление на ученици и учители; фиксиране отсъства; проверка на готовността на учениците за урока; организация на вниманието.
Това е последвано отcсъздаване на основни знания: учителят задава въпроси на учениците, отговорите на които ще бъдат използвани в процеса на изучаване на нов материал:
1) Какви вещества принадлежат към класа на киселините?
2) Дайте формулите на известните ви киселини?
3) Разберете какво е общото в състава на всички киселини, как можете да откриете киселина в разтвор?
4) Какви вещества принадлежат към класа на основите и как се класифицират според тяхната разтворимост във вода?
5) Дайте формулите на известни алкали и отговорете на въпросите:
а) Какво е общото между тях?
б) как може да се открие алкал в разтвор?
6) Какви вещества се наричат соли?
След като запомни необходимата информация, учителят продължава да представя новия материал.
Учителят отново насочва вниманието на учениците към темата на урока: в него и двете думи са нови и следователно неразбираеми. Тези термини ще трябва да бъдат дешифрирани по време на урока. Това послание насочва учениците към възприемане на нов материал.
След това учителят формулира учебна задача-1 под формата на проблемен въпрос:Ще се промени ли цветът на индикатора в киселина, ако се разтвори не във вода, а в друг разтворител (например в ацетон)?се затруднява да отговори.
За да провери хипотезите, изложени от учениците, учителят демонстрира експерименти:
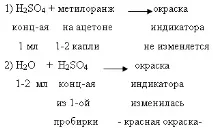
Т.Б. Внимателно добавете концентрирана H2SO4, като настъпва интензивно нагряване.
По време на експеримента учениците отбелязват, че в първия случай цветът на индикатора не се е променил, а във втория се е променил, станал червен.
Заедно с учителя учениците заключават:
Киселините променят цвета на индикатора самовъв воденразтвор.
Следващата стъпка: формулирането на образователен проблем-2 под формата на проблемен въпрос:Ще промени ли сухата основа цвета на индикатора?Мненията на учениците са различни: да, не, трудно е да се отговори.
За да разреши противоречията в отговорите, учителят демонстрира експерименти:
Изсипете малко кристален калциев хидроксид в две сухи епруветки и добавете кристали фенолфталеин в двете епруветки. Клатя. Налейте малко вода в една от епруветките.
Т.Б. Тръбите трябва да са абсолютно сухи.
Учениците отбелязват, че в първата епруветка не са настъпили промени, а във втората - цветът на фенолфталеина се променя на пурпурен.
Заедно с учителя учениците заключават:
Индикаторът променя цвета самовъв воденалкален разтвор.
Учителят информира учениците, че някои метали, като желязото, реагират с водни разтвори на определени соли, като меден (II) сулфат. Учителят формулира задача-3 под формата на въпрос:Ще взаимодейства ли желязото с разтвор на меден сулфат(II), ако солта се разтвори не във вода, а в ацетон?
Въз основа на резултатите от първия експеримент по-силните ученици предполагат, че вероятно не. За да потвърди правилността на хипотезата, учителят демонстрираопит:
Изсипете безводен меден (II) сулфат в две епруветки. В една от епруветките се налива 1 ml ацетон, а в другата - 1 ml вода. Разклатете двете епруветки. Потопете почистени железни пирони в разтворите.
Първо учениците наблюдават разтварянето на солта и в двата случая, след това наблюдават отделянето на мед само върху пирон във воден разтвор на сол, а солта, разтворена в ацетон, не взаимодейства с желязото.
Заедно с учителя учениците заключават:
Желязото само измества медтаот воденразтвор на сол.
Учителят прави общо заключение: киселини, основи, соли, т.е. вещества с йонни и ковалентни полярни връзки показват своите свойства самовъв водниразтвори.
Това означава, че нещо се случва с вещества във водни разтвори. Учителят насочва вниманието на учениците към ролята на водните молекули в тези процеси и въвежда понятието "електролитна дисоциация". Определението е написано на черната дъска. Учениците записват определението в тетрадката си.
След това структурата на водната молекула се разглежда подробно:
Връзката в молекулата е ковалентна полярна.
Диаграмата се рисува от учителя на дъската.
Механизмът на електролитна дисоциация се разглежда като се използва като пример дисоциацията на натриев хлорид. Едновременно с обяснението учителят рисува схема на дъската. Учениците рисуват в тетрадки и слушат внимателно и записват етапите на дисоциация в тетрадка.
Механизъм на електролитна дисоциация:
а) Първоначално произволно движещите се водни молекули в близост до йоните на кристала са ориентирани към тях с противоположно заредени полюси - възниква ориентация.
б) Тогава водните диполи се привличат, взаимодействат с йоните на повърхностния слой на кристала - настъпва хидратация.
в) Молекулите на водата, преминавайки в разтвор, се улавят отхидратирани йони – настъпва дисоциация.
Учителят обяснява как протича дисоциацията на вещества с ковалентна полярна връзка: дисоциацията на вещества с ковалентна полярна връзка продължава още една стъпка - ориентация -> хидратация -> йонизация (т.е. трансформация на ковалентна полярна връзка в молекула в йонна връзка) -> дисоциация.
Студентите задълбочават знанията си за механизма на електролитната дисоциация; задайте знания, запишете етапите на дисоциация в тетрадка.
След това учителят задава въпроса:Възможно ли е експериментално да се потвърди фактът, че има йони във водни разтвори на киселини, основи, соли?Учениците се затрудняват да отговорят. За да разреши затруднението, учителят демонстрира експерименти за изпитване на кристални вещества и техните разтвори за електропроводимост. Учениците правят наблюдения и ги записват на дъската и в тетрадка.
Писане на дъската.
NaCl е кристален - крушката не свети, не провежда ток.
Разтвор на NaCl - крушката свети, провежда ток.
Ca (OH) 2 кристален - крушката не свети, не провежда електрически ток.
Разтвор на Ca (OH) 2 - крушката свети, провежда ток.
Разтвор H2SO4 - крушката свети, провежда електричество.
Въз основа на резултатите от експеримента се провежда разговор по следните въпроси:
Защо свети крушката?
Учениците отговарят, че при преминаване на електрически ток през разтвор йоните придобиват насочено движение: отрицателно заредените йони (аниони) се движат към положителния полюс, а положително заредените йони (катиони) се движат към отрицателния полюс. Веригата се затваря и светлината светва.
Защо кристалните вещества не провеждат електричество?
защотоВ кристалите йоните са свързани един с друг.
След това учителят описва накратко историята на развитието на теорията за електролитната дисоциация:
Автор на теорията за електролитната дисоциация е шведският учен Сванте Арениус. Като привърженик на физическата теория на разтворите, С. Арениус не можа да отговори на въпроса: защо се случва дисоциацията на соли и алкали във воден разтвор (в края на краищата сухите соли не провеждат електрически ток) и откъде идват йони в киселинни разтвори? Отговорът е даден от българските химици И. А. Каблуков и В. А. Кистяковски, които прилагат химическата теория на разтворите на Д. И. Менделеев за обяснение на електролитната дисоциация.
Учителят въвежда понятията "електролити" и "неелектролити", "степен на електролитна дисоциация":
Веществата, чиито разтвори провеждат електрически ток, се наричат електролити; Веществата, чиито разтвори не провеждат електрически ток, се наричат неелектролити.
Тъй като молекулите присъстват в електролитни разтвори заедно с йони, електролитните разтвори се характеризиратсъс степента на дисоциация,която се обозначава с гръцката буква a (алфа).
Степента на дисоциация е съотношението на броя на молекулите, разградени на йони (Nd) към общия брой разтворени молекули (Np): a = Nd / Np
Степента на електролитна дисоциация се определя емпирично и се изразява във фракции или проценти. Ако a \u003d 0, тогава няма дисоциация, ако a \u003d 1 или 100%, тогава електролитът напълно се разлага на йони.
Електролитите имат различна степен на дисоциация, т.е. степента на дисоциация зависи от природата на електролита. Зависи и от концентрацията: с разреждането на разтвора степента на дисоциация се увеличава
Учениците разширяват и задълбочават знанията по темата на урока, задават знания, записватнотация и формула в тетрадка.
Въз основа на концепцията за степента на електролитна дисоциация, учителят дава концепцията за силни и слаби електролити:
Силните електролити, когато се разтворят във вода, почти напълно се дисоциират на йони. За такива електролити стойността на степента на дисоциация клони към единица.
Силните електролити включват:
1) всички разтворими соли;
2) силни киселини, например: H2SO4, HCl, HNO3;
3) всички алкали, например: NaOH, KOH.
Слабите електролити, когато се разтварят във вода, почти не се дисоциират на йони. За такива електролити стойността на степента на дисоциация клони към нула.
Слабите електролити включват:
2) воден разтвор на амоняк NH3 * H2O.
Учениците разширяват понятието електролити, задават знания, записват примери в тетрадка.
След обяснението на материала по темата следва затвърдяване на знанията. Учителят кара учениците да изпълнят следните задачи:
1) Обяснете защо разтвор на калиев хидроксид провежда електричество, а разтвор на глюкоза C6H12O6 не.
2) Защо степента на неговата дисоциация се увеличава, когато разтворът на електролит се разрежда?
3) Как се различава електрическата проводимост на металите и електролитите по природа?
4) Как да обясним електрическата проводимост на водни разтвори на електролити?
Учениците прилагат наученото в клас, за да решават проблеми.
Те развиват способността да обясняват своите отговори, да анализират условията на задачите, способността да използват допълнителни справочници (таблица за разтворимост).
След затвърждаване на знанията се давадомашна работа:
Параграф 35, бележници, изх. 1-5, стр. 198.
Габриелян О.С. Химия. 8 клас: учебник. за общо образование институции / О.С. Габриелян. - 11-то изд., Рев. -М.: Bustard, 2005. - 267 с. : аз ще.