Структурата на атома на полоний (Po), схема и примери
Общи сведения за структурата на полониевия атом
Отнася се за елементи от p-семейството. Метал. Обозначение - По. Пореден номер - 84. Относителна атомна маса - [210] a.m.u.
Електронната структура на полониевия атом
Полониевият атом се състои от положително заредено ядро (+84), вътре в което има 84 протона и 126 неутрона, а 84 електрона се движат в шест орбити.
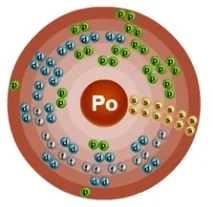
Фиг. 1. Схематична структура на полониевия атом.
Разпределението на електроните в орбиталите е както следва:
На външното електронно ниво на атома на бисмута има 6 електрона, които са валентни (разположени на 6s- и 6p-поднивата). Енергийната диаграма на основното състояние има следната форма:
Валентните електрони на полониевия атом могат да се характеризират с набор от четири квантови числа: n (основно квантово), l (орбитално), ml (магнитно) и s (спин):
Полоният се характеризира с наличието на възбудено състояние поради свободни орбитали на подниво 6d:
Примери за решаване на проблеми
209x + 208x(100x) = 208,9824x100%.
209x + 20800 - 208x = 20898,24;
Енергийната диаграма на основното състояние има следната форма:
Енергийната диаграма на основното състояние има следната форма:
Хлорът и манганът имат еднакъв брой електрони на външната електронна обвивка - 7, така че те са в една и съща група на периодичната таблица на D.I. Менделеев - VII. Най-високата валентност, както и степента на окисление, се определят от номера на групата, следователно те са равни съответно на VII и +7. Най-ниската валентност за хлорния атом е I, а степента на окисление е -1; манган - съответно II и +2.
Висшите оксиди имат формули Cl2O7 и Mn2O7, исъответните им хидроксиди HMnO4 и HClO4, те проявяват киселинни свойства.