Травматично увреждане на мозъка и инсулт
В произхода на черепно-мозъчната патология (фактори от първи ред) при травма или инсулт решаващо значение има механизмът на възникване на локално първично огнище на деполяризация (обемен процес - градиент на вътречерепно налягане в резултат на вибрация, ротация, шок на цереброспиналната течност, кръвоизлив). Реакцията на нараняване се проявява чрез локален реактивен оток (в рамките на 24 часа) и първична интракраниална хипертония.
Особено често се увреждат участъците на стъблото, съседни на твърдата мозъчна обвивка, която или просто покрива черепните кости, или образува свои собствени фиксирани образувания (сърп, церебеларна мантия). Преобладаването на определени признаци се осигурява от локалното развитие на съдовата мрежа; близостта на местоположението на ядрата; полисинаптичен характер на нервната тъкан, по-специално - ретикуларната формация. Неговото дезактивиране е особено забележимо, тъй като в същото време отпадат неговите активиращи и синхронизиращи влияния върху висшите и долните части на централната нервна система. Напротив, най-добри резултати се получават при ограничени инфаркти на ствола, когато симптомите се изразяват само в булбарна или псевдобулбарна парализа (до 47% от пациентите с изолирани респираторни нарушения оцеляват, т.е. без загуба на контрол върху други жизнени функции).
Увреждащите фактори са системни и локални хидродинамични нарушения (микроциркулация на кръвта, цереброспинална течност), водещи едновременно до нови механични увреждания на мозъчната тъкан (нарушение под церебеларния шип, в голямата тилна дупка или дупка), както и до метаболитни нарушения (хипоксия, ацидоза, прекомерно освобождаване на ацетилхолин, хистамин и други продукти на локалния катаболизъм).
Важна роля за възникването на тези състояния играятт.нар първичен централен холинергичен отговор. Същността му е, че дразненето на парасимпатиковите ядра води до масивна енергийно-тропна контрарегулация с "дистония", с локални (вазоконстрикция със застой и агрегация на кръвни клетки) и системни хидродинамични нарушения. На свой ред отклоненията в хидродинамиката и ендокринно-хуморалното състояние водят до влошаване на вътречерепните водни състояния и нарушения на водния обмен. Така че, с повишаване на вътречерепното налягане и паралелно затруднено кръвообращение, функциите на кората на главния мозък страдат и центровете на хипоталамуса изчезват от неговото влияние - диенцефален синдром. Придружава се от прилив на хиперкатаболизъм с хиперпнея, с мускулна и артериална хипертония, с хипергликемия, хипертермия и др. . На определен етап и в леки ситуации те имат компенсаторна стойност: благодарение на тях мозъкът, дори и при намален кръвен поток, е в състояние да извлече максималното възможно количество хранителни вещества и стимуланти. Но след това с повишаване на кръвното налягане, артериалния приток към мозъка и вътречерепното налягане се възбуждат механизмите за контрол на вътречерепната хидродинамика. По-специално, хипокапнията, която придружава повишената белодробна вентилация, действа в същата посока. Те причиняват стесняване на мозъчните артериални съдове, което поне по някакъв начин ограничава артериалния приток. Но с намаляване на pCO 2 под 19 mm Hg. Изкуство. това стесняване става прекомерно. Едновременното блокиране на образуваните елементи, поради тяхната деполяризация от увредените тъкани, изостря исхемичното увреждане на мозъка (и миокарда). Напротив, хиперкапнията (например при паралелна обструкция на дихателните пътища) е придружена от вазодилатация и увеличаване на притока на кръв към мозъка. Резултатът, както винаги, се определя от много фактори. Така че, когато се изразилокален първичен оток, който придружава тежки увреждания, когато собствените механизми за стабилизиране на ICH не се справят с функциите си, възниква нова вълна от вече вторичен генерализиран оток. Осигурява се както от хидродинамичен компонент (преобладаване на артериалния приток над венозния отток), така и от метаболитен (преобладаване на разпадането над синтеза).
В този случай всичко се случва, както в амортисьорите на автомобила, когато е претоварен - нови порции цереброспинална течност се изтласкват от вентрикулите на мозъка в гръбначното пространство. По същия начин нови порции венозна кръв се изстискват от церебралните вени през синусите в системата на горната празна вена. Тъй като се използват тези амортизиращи хидромеханични компенсаторни процеси и съдържанието на вентрикулите се изтласква от черепа, възможностите на анатомичните механизми за стабилизиране на ICH се изчерпват. В допълнение, трофичните нарушения, свързани със стагнация и оток, са придружени от катастрофално бързо увреждане на клетките с техния оток (подуване) и трансминерализация. В този случай вторичният трансудат без протеини импрегнира неклетъчното пространство на медулата (интоксикация с глиарна вода), откъсвайки клетките една от друга и от съдовете, разделяйки тези образувания анатомично и функционално (разединителна арефлексия). В тежки случаи трансминерализацията с клетъчен оток може да се развие в състояние на злокачествен декомпенсиран глиален оток, когато миелиновото покритие на невроните е унищожено; глията е фрагментирана; образуват се периглиарни "езера", в които плуват кръвни клетки и клетъчни фрагменти.
Най-забележимите нарушения както на трофизма, така и на функцията се появяват в местата, където мозъкът се придържа към твърди вътречерепни образувания - в мозъчната кора близо до вътрешната повърхност на черепакости; в мозъчните дръжки близо до острите предни ръбове на церебеларния шип; в предните части на сърпа; в маслините на малкия мозък във foramen magnum; в черепните нерви на туберозната основа на черепа. Скоростта на възникване на тези усложнения зависи от скоростта на развитие и локализация на обемния процес.
Веднага щом вътречерепното налягане се доближи до налягането в мозъчните капиляри (около 300 mm воден стълб), кръвотокът в тях спира. Съответно стволовите функции отпадат и кръвното налягане пада необратимо. Още преди това спадовете на вътречерепното налягане водят до измествания (размествания) на мозъчната маса и се съпровождат от появата на хернии (инкарцерирани церебрални хернии) в естествените отвори и пукнатини на черепа. В тяхното възникване участват два механични компонента. Едното се дължи на тежестта на самия мозък (гравитационно), а другото се дължи на градиенти на хидродинамично налягане (хидродинамично). Посоката на гравитацията е винаги постоянна - към центъра на Земята, а хидродинамичната - винаги в посока на най-малкото противоналягане - под шипа на малкия мозък, към голямата тилна дупка или дупка. При тези размествания се получава притискане и огъване на венозните съдове. В по-голяма степен това се отнася до мястото на сливане на вътрешните церебрални вени и долния сагитален синус в директния синус, преминаващ през церебеларната плака, както и сигмоидния синус във вътрешната югуларна вена.
На този етап ятрогенията, свързана с "непоправимото" желание на медицинските работници да положат жертвата по гръб, се присъединява към спонтанните увреждащи фактори от втори ред. В тази позиция посоката на гравитационните и хидродинамичните компоненти съвпадат, което осигурява катастрофално бързо нарастване на увреждането на мозъка. Тежест на мозъка върху острите ръбове на церебеларната плакадолно-външните части на краката на мозъка, окуломоторните, трохлеарните и тригеминалните нерви са "изтиснати". Успоредно с това, под тежестта на мозъка, се притиска Силвиевият акведукт, който отвежда цереброспиналната течност през четвъртата камера към гръбначното пространство. Това блокира ликвородинамиката и провокира бързо повишаване на ICP. Заедно с тежестта на мозъка, той "изстисква" ствола и церебеларните маслини във foramen magnum.
Нарушаващите зони, като правило, са отговорни за регулирането на важни и следователно лесно забележими функции. Компресията на краката на мозъка се дължи на бързо прогресиращия ступор, преминаващ в отсъствието на външни прояви на съзнанието. Но често пациентът е в състояние да чуе (слуховият нерв не е повреден) и да си спомни какво се случва около него. Диенцефалният отдел контролира производството на енергия. Продълговатият мозък е изцяло отговорен за контрола на респираторния автоматизъм, сърдечната честота и комуникацията мозък-гръбначен стълб. Грубите и необратими трофични нарушения, които се появяват в засегнатите части, бележат терминалния стадий на остра CMP.
Клетъчните структури са много уязвими. Тази уязвимост се определя от високата скорост на техния обмен. Освен това най-интензивно се обменят ензимните протеини, които определят посоката в изключително разклонени метаболитни пътища. Най-малко интензивните - нуклеиновите киселини на клетъчното ядро - вид клетки за съхранение на информация. Ориентацията на обмена (анаболен или катаболен) до голяма степен се определя от активността на вътреклетъчните лизозомни хидролази, която се увеличава с транслокацията и подкисляването (протонизирането) на вътреклетъчната среда.
Значението на свръхпротонизацията е описано по-горе в раздела за киселинно-базовия баланс. Припомняме само, че барикадата на метаболитните пътищапротоните водят клетката до смърт, която идва чрез добре познати и разбираеми явления:
- прекратяване на производството на енергия и в същото време енергийно зависими процеси на обновяване, неспецифични и специфични клетъчни функции;
- взаимно активиране на клетъчни хидролази (автолитични ензими), вътреклетъчен разпад, клетъчна хиперосмия и неустоим клетъчен трансфер.
И все пак, при тези условия, и аноксия, и кървене (исхемия), и стагнация, мозъчната тъкан за доста дълго време е в състояние да поддържа способността да генерира енергия и всъщност жизнеспособността. "Животяващата" роля се изпълнява от:
- първо, количественото превъзходство на концентрациите на субстрати (първоначалните продукти за веригата от метаболитни процеси) над крайните продукти (мозъкът няма значителни резерви) и
- второ, годността на механизмите за разтоварване на протони.
Естествено, за функционирането на тази многозвенна, конвейерна метаболитна система, трябва да има достатъчно обемен резерв от носещи субстрати, способни да приемат тези транспортирани протони и да ги задържат (депозират) до "по-добри времена". Подобна функция могат да изпълняват така наречените метаболитни шънтове и задънени краища (приложени към ситуацията, по-добре е да ги наречем протонни торби, дивертикули или капани, подобно на паркинги и капани, които се оборудват от пътни работници по магистрали и при остри завои на планински автосерпентини). Техните възможности могат да бъдат разширени чрез предварително обучение на съответните ензимни системи (Korostovtseva N.V., 1973).
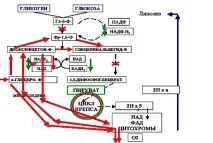
Първата връзка в протонната акцепторна система е системата NAD и NADP, която осигурява активен трансфер на протони между субстратите. Най-известен с тази ролялактатна задънена улица, чийто капацитет според A. Labori (1967) е около 7 mmol/l лактат. Малко лекари знаят за съществуването на глицерофосфат (Boxer G.E., Devlin T.M., 1961; Smith R.E., Holier D.J., 1962), глутамат, аспарагин, цис-аконит, глиоксилов и други шънтове. Междувременно те също участват активно в освобождаването на протони и в повторното активиране на NAD и NADP, които след това могат да се включат отново в процесите на производство на енергия.
Въпреки това, тъй като междинните продукти се натрупват, градиентът на концентрацията между субстратите и реакционните продукти неизбежно се изглажда. Темпото на последното се забавя. Вярно, консумацията на енергийни вещества също се забавя. По този начин, при потисната автолиза, колкото по-обратима е смъртта, толкова по-голям е енергийният резерв и капацитетът на протонните торби (концентрацията на съответните ензими). На първо място има превантивна стойност – да предпазва мозъка от последствията от ПРЕДСТОЯЩАТА хипоксия или исхемия.
В условията на вече приключила исхемия (ПОЗИШЕМИЧЕН период) и възстановена клетъчна иригация (включително кислород и налични субстрати) има нужда не от запазване, а от възможно най-бързо възстановяване на митохондриалното окислително фосфорилиране. Ясно е, че спряното „колело на Кребс“, възстановяващо естествената посока и скоростта на обмяна при „нулеви“ градиенти на концентрация и освен това в най-„протонизираната“ среда, е възможно само чрез енергичен „метаболитен тласък“ поради „резервиране“ на субстрата с едновременното активиране на следните два механизма:
- отваряне на портала (реоксидация на NAD и NADP);
- изхвърляне на "отпадъчни" субстрати от метаболитната магистрала и от протонните торби извън клетката.
Стойността на субстрата, тоест „лекотата“ на включване на субстрати в желаната реакция, е от първостепенно значение. Основно се определя от размера на техните молекули и независимостта от ензимите, които катализират реакциите в ключовите звена на метаболитния конвейер.
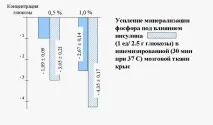
По време на хипоксия много ензими се разграждат под действието на активирани лизозомни протеази. Хексокиназата и фосфофруктокиназата, които катализират метаболизма на глюкозата, изглежда са сред най-чувствителните. В допълнение, клетъчните протеази могат да предотвратят свързването на хексокиназата с липопротеините на митохондриалната мембрана, да унищожат ензимите на дихателната верига, съдържащи флавинови или хем групи, и също да унищожат протеин, съдържащ нехем желязо. В резултат на това за „протонирания“ мозък окисляването дори на „обичайната“ глюкоза става непоносимо и много по-лесно (особено при паралелна „адекватна“ инсулинова терапия) се насочва „нагоре“ към превръщане в гликоген, отколкото „надолу“ към окисление в пируват.
Метаболитният тласък може да се осъществи чрез рязко увеличаване на концентрацията на субстрата, който има способността да дарява своите протони директно на компонентите на дихателната верига в нейните последни звена. Именно тези свойства имат GABA, ацетоацетат и глицерат-диоксиацетон-фосфатни системи по отношение на цитохромите и сукцинат - по отношение на FAD-връзката (Rappoport, 1964; Shumakov V.I. et al., 1975).
Оказва се, че намаляването на субстратната стойност на глюкозата по време на исхемия е относително лесно обратимо. Във всеки случай, в експеримента (Grushevsky V.E. и Grushevskaya O.A., 1973), мозъчната тъкан, дори след 30-минутна пълна исхемия, отново в присъствието на протеиназни инхибитори, възстановява способността да използва кислород инеорганичен фосфор.