МЕТАЛНИ РЕШЕТКИ
Всички метали са кристални вещества. Какво представляват кристалите?
Думата "crystallos" в древните гърци е означавала лед. Впоследствие тази дума започва да се нарича всички твърди тела, които имат естествена, строго определена геометрична форма. Кристалите са много разпространени в природата. По-голямата част от твърдите вещества имат кристална структура.
Желязото, когато се втвърди, образува кристали под формата на кубчета. Но на фигура 4 виждаме железни кристали с неправилна форма, кристалити, които приличат на зърна. Защо се случва това? Как растат кристалите?
Отговорът на тези въпроси беше даден от Д. К. Чернов. Впоследствие валидността на неговите възгледи беше потвърдена от работата на много съветски учени.
Прахови частици, въздушни мехурчета и други чужди включвания неизбежно попадат в разтопения метал. По правило именно около тези най-малки частици произволно разположените атоми в охлаждащия метал започват да се групират. В допълнение, комплекси от атоми, които спонтанно възникват в охладения метал, също служат като кристализационни центрове. Така се образуват ядрата на бъдещите кристали (фиг. 5, а). Когато металът се охлади, броят на ядрата се увеличава. Всеки ембрион израства в отделен кристал (Фиг. 5б). Растящите кристали в определен момент започват да се натискат един друг (фиг. 5, в) и правилната им форма се изкривява. Неравномерната температура на различни места на охлаждащия метал също допринася за нарушаването на формата на кристалите. Поради това в стопилката се появяват зърна (фиг. 5, г) и дървовидни образувания от отделни малки кристали, слети помежду си - дендрити. Кристалните зърна и дендритите във втвърдения метал могат да бъдат с различни форми и размери.
лица. Те са отделени един от друг с отделни слоеве, коитоясно видими под микроскоп (виж фиг. 4). Тези междинни слоеве се състоят от различни неметални включвания, които винаги присъстват в метала.
Вземете метал, който би се състоял само от един кристал - единичен кристал, при нормални условия

Ориз. Фиг. 5. Схема на растеж на кристали в втвърдяваща се стопилка: a - образуват се ядра, b кристали растат, c - кристалите започват да се тълпят един друг, d - отделни зърна се сливат.
не мога Това се обяснява с факта, че много кристали се генерират едновременно в стопилката. Въпреки това, за да се изследват определени свойства на металите, както ще видим по-късно, понякога е необходимо да имаме единичен кристал и сега са разработени методи за изкуствено отглеждане на монокристали (внимателно охлаждане на стопилката и други методи).
И в зърната, и в дендритите, и в единичен кристал от един и същи метал атомите са подредени в строго определен ред; те образуват тази или онази пространствена решетка.
Атомите не могат да се видят с никакъв микроскоп. Въпреки това, чрез осветяване на кристала с рентгенови лъчи и изучаване на рентгеновата картина, тоест картината, която се създава от тези лъчи, след като преминат през кристала върху фотографска плака, е възможно да се надникне дълбоко в света на кристалите. Възможно е да разберете как са разположени различните атоми в кристалната решетка и какви са разстоянията между тези най-малки частици материя, частици, които не можем да видим.
Рентгеновите изследвания показват, че сред металите най-често се срещат три типа пространствени решетки.
Първият тип е кубична тялоцентрирана решетка. Атомите в такава решетка са разположени във върховете и в центъра на куба (затова решетката се нарича тялоцентрирана). Всеки атом е заобиколен от осем най-близки съседни атома(фиг. 6, а). Литий, хром, ванадий, молибден, волфрам имат такава решетка.
Вторият тип решетка е кубична лицево-центрирана (фиг. 6b). Атомите са разположени във върховете и центровете на лицата на куба. Такава решетка притежават например алуминият, медта, оловото, никелът, златото, среброто и платината.
Третият тип е хексагонална (шестоъгълна) плътно опакована решетка (фиг. 6в). Среща се в магнезий, цинк, кадмий, берилий.
Манганът, бисмутът, белият калай и някои други метали имат по-сложни решетки.
Чрез изучаване на рентгенови дифракционни модели на различни кристали, учените стигнаха до извода, че атомите са "опаковани" в пространството по същия начин, по който могат да бъдат опаковани твърдите топки. Следователно на фигура 6 атомите са условно изобразени като топки (разстоянията между тях в лявата част на фигурата са умишлено увеличени, за да се представи по-ясно структурата на кристалната решетка).
Както в лицево-центрираната кубична, така и в шестоъгълната решетка, всеки метален atm е заобиколен от дванадесет най-близки съседни атома. Колкото повече съседи има един атом в кристалната решетка, толкова повече място в решетката се заема от самите атоми. Най-плътното "опаковане" на атомите е в лицево-центрирани и шестоъгълни решетки. Тук атомите притежават 74% от пространството, заето от кристали. В обемно центрирана кубична решетка атомите заемат само 68% от пространството.
Трябва да се каже, че в металните кристали няма неутрални атоми; пространствените решетки са изградени от положително заредени атоми, от йони.

Ориз. Фиг. 6. Видове кристални решетки на метали: a - кубична тялоцентрирана решетка, b - кубична лицевоцентрирана решетка, c - шестоъгълна решетка (плътна опаковка).
Всеки метален атом е винагигуби една или повече частици с отрицателно електричество - електрони, и се превръща в йон. Йоните са фиксирани във "възлите" на пространствената решетка - върховете и центъра на куба, в центровете на стените и т.н., в зависимост от вида на решетката. Електроните се скитат произволно между йоните.
Природата на кристалната решетка и разположението на атомите в нея оказват голямо влияние върху много свойства на веществата. Ще говорим за това подробно, но сега ще се запознаем с една интересна особеност на кристалите, която се нарича "анизотропия" и се обяснява с тяхната структура. Думата "анизотропия" на гръцки означава "неравностойно свойство". Анизотропията е нехомогенността на свойствата на кристала в различни посоки.
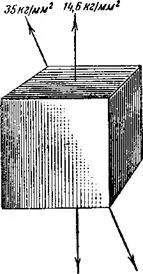
Ориз. 7. Сила на кристала 8. Стъклото провежда топлина от мед към мед в различни посоки и бързо във всички посоки.
различен. Калайът провежда топлина в някои
Дъските са по-лоши от другите.
Ако пробата е поставена по диагонала на куба, тогава за разкъсване е необходимо напрежение, равно на 35 kg/mm2 (фиг. 7). Това показва, че медните кристали са по-силни в една посока, отколкото в другата.
Топлопроводимостта на кристалите също не е еднаква в различни посоки. Този опит ни убеждава (фиг. 8). Да вземем кристал от бял калай и за сравнение - куб, изрязан от стъкло (стъклото е изотропен материал - свойствата му са еднакви във всички посоки). Ще покрием лицата им с парафин и след това ще ги приведемнего гореща игла. Разтопеният слой парафин върху стъкло ще има формата на кръг, а върху калай ще бъде овален. Това означава, че калайът провежда топлината по-лошо в някои посоки, отколкото в други, докато стъклото прави същото във всички посоки [48]).