Нови функции на чревната микрофлора
"Ние сме това, което ядем" (Хипократ).
Статия за конкурса "био/мол/текст": "Ние сме това, което ядем." Това е казал Хипократ. Но можеше ли да си представи колко прав е бил? Според най-новите научни данни, храната, която приемаме, има много силен ефект върху чревната ни микрофлора, което в крайна сметка се отразява на тялото ни. Освен това влияе доста осезаемо - например промяна на теглото ни! Получава се порочен кръг: човек - микрофлора - човек.

"Био/мол/текст" -2016г
Генерален спонсор на състезанието, според нашето групово финансиране, беше предприемачът Константин Синюшин, за което той изпитва огромно човешко уважение!
Спонсор на Наградата на публиката беше Атлас.
Ролята на чревната микрофлора в регулирането на много процеси в тялото е известна отдавна. Например, той образува защитна бариера на чревната лигавица, стимулира имунната система [1], неутрализира токсините, произвежда витамини, усвоява фибри и много други. Но науката, както знаете, не стои неподвижна и се появяват нови данни. Така например сега се разглежда връзката между състоянието на чревната микрофлора и затлъстяването, както и развитието на захарен диабет тип 2!
Какво е нормофлора и какви са нейните функции
Припомнете си какво представлява нормалната човешка микрофлора.Нормофлора (микрофлора в нормално състояние илиеубиоза ) е съвкупност от микробни популации на отделни органи и системи, характеризиращи се с определен качествен и количествен състав и поддържащи биохимичния и имунологичен баланс, необходим за поддържане на човешкото здраве.
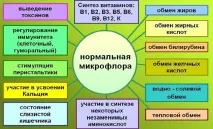
Фигура 1. Основни функции на нормалната микрофлора.
метаболитната активност на черватаmicrobiota, в допълнение към задоволяването на нуждите на бактериите, помага за извличане на калории от храната, консумирана от гостоприемника, помага за съхраняването на тази енергия в мастните му депа, тоест за образуването на мастна тъкан. При експерименти с гнотобиотични (свободни от микроби) мишки, населени с определени бактерии, е доказано, че чревната микрофлора осигурява разграждането на несмилаемите хранителни полизахариди в смилаеми форми от гостоприемника – но това едва ли е новина. Откритието е, че този процес е придружен от увеличаване на абсорбцията на монозахариди от червата и навлизането им в порталната вена, вероятно поради увеличаване на плътността на капилярната мрежа в лигавицата на тънките черва под влияние на микробиотата. Това доведе до увеличаване на чернодробната липогенеза, тоест синтеза на мастни киселини от въглехидрати. Факт е, че чернодробните клетки реагират на повишаване на нивото на глюкоза и инсулин в кръвта, като експресират гените за транскрипционните фактори ChREBP и SREBP-1, които активират гените за биосинтеза на триглицериди, тоест мазнини. Увеличаване на производството на тези транскрипционни фактори се наблюдава след колонизиране на червата на мишка с микробиота. В допълнение, чревните бактерии спомогнаха за поставянето на новопроизведени триглицериди в мастните клетки (адипоцити), пречейки на работата на гените на гостоприемника: микрофлората увеличи активността на необходимата за това липопротеин липаза, потискайки синтеза на нейния инхибитор в епитела на тънките черва.
Тук обаче си струва да припомним, че става дума за мишки, за специфичен ентеротип на тяхната микрофлора (биоценоза, в която преобладават определени групи бактерии) и като цяло за основните функции на микробиотата. Следователно, въз основа на тази работа, не е необходимо да се заключава, че всяка чревна бактерия има вредно въздействие върху гостоприемника, това е просто как хипотезата за множество и взаимосвързанимеханизми на влияние на чревната микробиота върху енергийния метаболизъм на гостоприемника, а с това и надеждата, че коригирането на това влияние ще помогне за справяне с епидемията от затлъстяване [5]. Авторите на работата предполагат, че микробният "биореактор" в един индивид може да бъде по-енергийно ефективен, отколкото в друг. И ние ще се докоснем до факторите, които влияят на това.
Микрофлората при хора с нормално тегло и затлъстяване е различна
Последните експерименти показват, че промените в микрофлората са свързани с причините за затлъстяването, а не с последствията от него. Ако червата на гнотобиотичните мишки се заселят отново с микробиота на затлъстели мишки, животните ще наддават на тегло по-бързо, отколкото ако бактериите са били трансплантирани от слаби мишки. Освен това съставът на микробиотата може да предскаже с 90% вероятност дали човек страда от затлъстяване [6]. Просто си представи! Сега си представете, че чрез промяна на състава на чревната микрофлора на човек ще бъде възможно да се регулира теглото му (фиг. 2).

Фигура 2. Какво е забележителното в състава на чревната микрофлора на човек със затлъстяване?
Многократно е установено, че при затлъстяване се увеличава броят на представителите на типа Firmicutes (например Clostridium coccoides, C. leptum) и семейство Enterobacteriaceae (Esherichia coli). В същото време броят на представителите от типа Bacteroidetes (Bacteroides, Prevotella) намалява, а популациите на бактериите от родовете Bifidobacterium и Lactobacillus намаляват [7]. Досега е доказано, че диета с високо съдържание на мазнини насърчава възпаление на чревната лигавица, медиирано от намаляване на лактобацилите. Това възпаление предразполага към развитие на затлъстяване и инсулинова резистентност, т.е. диабет тип 2. През 2016 г. експерименти с мишки успяха да установят връзка между тези състояния и дефицита на специфични щамове на Lactobacillus reuteri вЛепенки на Пейер. Факт е, че диета, богата на мазнини, осигурява селекция на бактериални щамове, които са устойчиви на оксидативен стрес. И това се оказаха просто лактобацили, които отделят провъзпалителни цитокини. И обратно, „добрите“ щамове на L. reuteri, производителите на противовъзпалителни вещества, бяха изтласкани от популацията [8].
Метаболитни промени
Резултатите от проекта MetaHIT недвусмислено показват, че изобилието на човешката чревна микрофлора корелира с нейните метаболитни маркери, докато бактериалните гени играят почти по-голяма роля в патогенезата на затлъстяването, отколкото нашите собствени.
Сред собствениците на "малкия геном" (23% от всички участници) имаше повече хора с наднормено тегло. Тази група като цяло се характеризира с нарушения в реакцията на тъканите към действието на инсулина, което води до повишаване на концентрацията му в кръвта. Такива хора също показват статистически значимо намаляване на съдържанието на така наречения "добър холестерол" - липопротеини с висока плътност, които пренасят холестерола от различни тъкани до черния дроб за по-нататъшна трансформация и използване. Наблюдава се и тенденция към повишаване на кръвните нива на триглицеридите, свободните мастни киселини и хормона лептин, чиито високи концентрации се считат за независим рисков фактор за развитие на сърдечно-съдови патологии и тромбоза. (Основните рискови фактори включват също специфични липидни профили, високо кръвно налягане, хронично възпаление и тютюнопушене.)
Редица проучвания показват, че при хора, чиято диета е доминирана от растителни компоненти, микробиомът е доминиран от бактерии, които разграждат полизахаридите и това са само представители на вида Bacteroidetes, някои от които предпазват гостоприемника от развитие на локално и системно възпаление. По същото времепри любителите на растителна храна броят на твърдиците намалява, както и ентеробактериите, които често се наричат "патобионти": те са в състояние да създадат възпалителна среда поради липополизахарида на външната им мембрана и да повишат пропускливостта на чревния епител, което води до широкомащабно проникване на липополизахаридни молекули в кръвния поток и провокиране на метаболитна ендотоксемия, и евентуално желание за редовно преяждане. Между другото, така се развиват събитията на фона на диета с високо съдържание на мазнини. Вегетарианската диета, напротив, се свързва от повечето проучвания с намален риск от развитие на метаболитен синдром и свързаните с него „болести на цивилизацията“ [7].
Активното разграждане на растителните фибри от съответните бактерии на дебелото черво води до образуването на монозахариди и късоверижни мастни киселини (SCFA). Последните - особено маслената киселина - са необходими не само за чревната микрофлора, но и за макроорганизма. Например, те намаляват рН на чревното съдържимо, като по този начин изместват редица патобионти от общността, и най-важното, те осигуряват енергия на ентероцитите, предпазват ги от онкотрансформация и потискат възпалителните сигнални пътища. Но дори и тук не всичко е толкова ясно: от една страна, излишъкът от SCFA може да подобри липогенезата и следователно да допринесе за развитието на затлъстяване, от друга страна, някои проучвания показват благоприятен ефект на SCFA върху липидния профил и нивата на кръвната захар. Този положителен ефект може да бъде медииран от SCFA свързване с G-протеин свързани рецептори GPR41 и GPR43, което води до хормонални промени, водещи до усещане за ситост и повишена чувствителност на тъканите към инсулин. Като цяло последствията от производството на големи количества SCFAs от микрофлората се влияят от редица фактори – от вида и количеството хранителни „суровини“ довариации в бактериалния състав, заложени в ранните етапи от развитието на организма. От друга страна, диетичните фибри предотвратяват метаболитни нарушения и независимо от състава на микрофлората. Освен това превантивният ефект на предимно растителна диета върху развитието на атеросклероза е показан от проучвания, свързани с биотрансформацията на L-карнитин: някои чревни бактерии, и доста полезни от друга гледна точка, превръщат L-карнитина, съдържащ се в червеното месо, в атерогенни вещества [7], [12].
Чревните бактерии са в състояние да намалят нивото на триглицеридите в кръвта, да подобрят метаболизма на глюкозата и липидите също поради прякото участие в циркулацията на жлъчните киселини и да намалят мастните резерви чрез активиране на вече споменатия инхибитор на липопротеин липаза [10]. Но все още е трудно да се направят изводи: понякога резултатите от експериментите са твърде противоречиви. Нов преглед ще помогне да се добие представа за противоречията и техните причини и най-важното за възможните механизми, свързващи активността на микробиотата с метаболизма на гостоприемника [10].
Ролята на микрофлората в развитието на диабет тип 1 и тип 2
Лечението и профилактиката наЗД тип 2 са тясно свързани с нормализирането на теглото. И това изисква промяна в естеството на храненето (съотношението на макро- и микроелементи) в комбинация с увеличаване на физическата активност: т.е. важно е да се създадат условия за някакъв енергиен дефицит, когато се изразходват повече калории, отколкото се получават [14]. И въпреки че ролята на чревната микробиоценоза в регулацията на енергийния метаболизъм не е напълно ясна, вече е ясно, че въздействието върху микрофлората определено може да помогне за премахване на затлъстяването и компенсиране на диабет тип 2.
И колкото и да е странно, подобно въздействие може да обърне тревожната ситуация сзаболяване, което е коренно различно патогенетично —DM тип 1. Това е автоимунно заболяване, свързано с агресията на Т-лимфоцитите срещу β-клетките на панкреаса, които произвеждат инсулин. Ако в случай на диабет тип 2 повишаването на нивата на кръвната захар се дължи на тъканна нечувствителност към инсулин (което не позволява на клетките да абсорбират глюкоза), тогава при диабет тип 1 просто няма достатъчно инсулин. Развитието на това заболяване изисква стечение на редица обстоятелства – генетични и екологични, като сред последните, както се оказа, огромна роля играе преструктурирането на чревния микробиом. Нормофлората на червата, веднага след заселването, обучава имунната система на гостоприемника да прави разлика между „ние“ и „те“, да реагира бурно на непознати, но да спре навреме [13]. Очевидно при диабет тип 1 нещо в тази верига се прекъсва.
При деца със ЗД тип 1 и здрави контроли се разкрива значителна разлика в състава на чревната микробиота, като диабетиците имат повишено съотношение Bacteroidetes/Firmicutes и преобладават бактерии, използващи млечна киселина. Здравите деца имат повече производители на маслена киселина. Като цяло се смята, че някои отклонения в състава на микрофлората, възникващи главно през критичните периоди на онтогенезата (по време на ембриогенезата, раждането, кърменето и пубертета), допринасят за увеличаване на провъзпалителната сигнализация с всички произтичащи от това имунни последици [16]. Възможно е, поради съпътстващото увреждане на бариерната функция на чревния епител, бактериалните антигени, освободени в кръвообращението и проникващи в панкреатичните лимфни възли, да взаимодействат с NOD2 рецепторите и да провокират Т клетките да атакуват панкреасните β клетки [17].
Така получените до момента данни формират основатаза по-нататъшно изследване на ролята на чревната микрофлора в механизмите на развитие на затлъстяването и диабет тип 1 и тип 2, както и да посочи възможността за предотвратяване и лечение на тези патологии по нови начини - чрез коригиране на нашия микробиом.