Обща характеристика на протеини, мазнини, въглехидрати
I. Обща характеристика, свойства, функции на белтъците. 3-5
II. Обща характеристика, свойства, функции на въглехидратите. 5-7
III. Обща характеристика, свойства, използване на мазнините. 8-12
IV. Минерали. 12-18
Библиография. 20
Знаем, че нашата храна се състои от протеини, мазнини, въглехидрати, минерали, вода, а също така съдържа витамини. Днес са създадени хранителни консерванти, овкусители и оцветители. В тази връзка се появи нов клон на химията - химията на храните. Този раздел се появи сравнително наскоро, тъй като беше необходимо да се изучават хранителни продукти, създадени чрез генно инженерство, изследване на вещества, създадени за подобряване на вкуса, цвета и съхранението на продукта. В това есе ще говоря за основните компоненти на храната, т.е. за основите на химията на храните - белтъчини, мазнини, въглехидрати, минерални вещества, за тяхното значение и за сложния химичен състав.
I. Обща характеристика, свойства, функции на белтъците.
И.И. основни характеристики
Протеинитеса азотсъдържащи високомолекулни органични вещества със сложен състав и структура на молекулите. Протеинът може да се разглежда като сложен полимер от аминокиселини. Протеините са част от всички живи организми, но те играят особено важна роля в животинските организми, които се състоят от различни форми на протеини (мускули, покривни тъкани, вътрешни органи, хрущяли, кръв) Растенията синтезират протеини (и техните съставки - аминокиселини) от въглероден диоксид CO2 и вода H2O чрез фотосинтеза, усвоявайки останалите елементи на протеините (азот N, фосфор P, сяра S , желязо Fe, магнезий Mg) от разтворими соли в почвата . Животинските организми получават предимно готови аминокиселини с храната и на тяхна основа изграждат протеини на тялото си. Редетеаминокиселини (неесенциални аминокиселини) могат да се синтезират директно от животински организми. Характерна особеност на протеините е тяхното разнообразие, свързано с броя, свойствата и начините на свързване на аминокиселините, включени в тяхната молекула. Протеините действат като ензимни биокатализатори, които регулират скоростта и посоката на химичните реакции в тялото. В комбинация с нуклеиновите киселини те осигуряват функциите на растеж и предаване на наследствени черти, са структурната основа на мускулите и извършват мускулна контракция. Белтъчните молекули съдържат повтарящи се C(0)NH амидни връзки, наречени пептидни връзки (теорията на българския биохимик А.Я. Данилевски). Следователно протеинът е полипептид, съдържащ стотици или хиляди аминокиселинни единици.
Специалната природа на протеина от всеки вид е свързана не само с дължината, състава и структурата на полипептидните вериги, включени в неговата молекула, но и с начина, по който тези вериги са ориентирани. В структурата на всеки протеин има няколко степени на организация:
1. Първичната структура на протеина е специфична последователност от аминокиселини в полипептидна верига.
2. Вторичната структура на протеина е начин на усукване на полипептидната верига в пространството (поради водородна връзка между водорода на амидната група NH и карбонилната група CO, които са разделени от четири аминокиселинни фрагмента).
3. Третичната структура на протеина е реална триизмерна конфигурация на усукана спирала на полипептидна верига в пространството (спирала, усукана в спирала). Третичната структура на протеина определя специфичната биологична активност на протеиновата молекула. Третичната структура на протеина се поддържа благодарение на взаимодействието на различни функционални групи на полипептидната верига: дисулфиден мост (-S-S-) между серни атоми, естерен мостмежду карбоксилната група (-CO-) и хидроксилната (-OH), солевият мост - между карбоксилната (-CO-) и аминогрупите (NH2).
4. Кватернерна структура на протеиновия тип взаимодействие между няколко полипептидни вериги. Например, хемоглобинът е комплекс от четири протеинови макромолекули.
I.II. Физични и химични свойства.
Протеините имат голямо молекулно тегло (104107 g / mol), много протеини са разтворими във вода, но обикновено образуват колоидни разтвори, от които се утаяват с увеличаване на концентрацията на неорганични соли, добавяне на соли на тежки метали, органични разтворители или при нагряване (денатурация).
1. Денатурационно разрушаване на вторичната и третичната структура на протеина.
2. Качествени реакции за протеин: биуретова реакция: виолетово оцветяване при третиране с медни соли в алкална среда (всички протеини дават), ксантопротеинова реакция: жълт цвят под действието на концентрирана азотна киселина, превръщайки се в оранжево под действието на амоняк (не всички протеини дават), черно утаяване (съдържащо сяра) с добавяне на оловен (II) ацетат, натриев хидроксид и нагряване. 3. Хидролиза на протеини при нагряване в алкален или кисел разтвор с образуването на аминокиселини.
I.III. Биологични функции на протеините.
Наборът от химични връзки, характерни за белтъчните макромолекули, предопределя тяхното функционално разнообразие.
1. Каталитични - отнасят се до биологични катализатори.
2. Транспорт - изпълнява функциите за пренасяне на вещества от един клетъчен компартмент в друг или между органи на целия организъм.
3. Регулаторни - регулаторни функции, предимно хормони.
4. Защитни - представениантитела или имуноглобулини.
5. Контрактилен - позволява ви да се свивате и движите, обикновено се съдържа в мускулната тъкан.
6. Структурни – влизат в състава на клетъчните мембрани.
7. Рецептор – участва в предаването на нервен или хормонален сигнал.
8. Резервен и хранителен - резервен и хранителен материал на клетката.
9. Токсични - представени от токсини от отровата на змии, скорпиони, пчели.
Предимно консумираме резервни и хранителни протеини (например месо, питателен протеин от птичи яйца, мляко и други).
Най-често консумираните протеини са:
Албумините са протеини от животински и растителни тъкани. Те са хранителни протеини. Разликите между албумините в животинската и растителната клетка се крият в различните количества метионин и триптофан. Както и много сложни протеини - липопротеини, гликопротеини, фосфопротеини, хромопротеини.
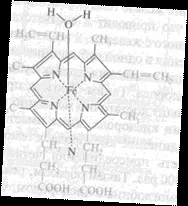
Фрагмент от хромопротеинова молекула.
II. Обща характеристика, свойства, функции на въглехидратите.
Въглехидратите, важен клас природни вещества, се срещат повсеместно в растителни, животински и бактериални организми.
Въглехидрати не е много добър термин, тъй като това е името на голям брой съединения с различна химична структура и биологични функции. Преди повече от 100 години беше предложено този термин да се използва за назоваване на природни съединения, чийто състав съответства на формулата (CH2 O) n, т.е. въглеродни хидрати. Тъй като бяха открити нови въглехидрати, се оказа, че не всички отговарят на тази формула, а някои представители на други класове имат същата формула. Голям принос за развитието на учението за въглехидратите направиха местните учени A.M. Бутлеров, А.А. Коли, Н.Н. Кочетков.
Въглехидратите включват съединения,вариращи от нискомолекулни, съдържащи само няколко въглеродни атома, до вещества, чието молекулно тегло достига няколко милиона.
Въглехидратите съставляват 80% от масата на сухото вещество на растенията и около 2% от сухото вещество на животинските организми.Животните и хората не са в състояние да синтезират захари и да ги приемат с различни хранителни продукти от растителен произход.