Получаване и свойства на арсеновия оксид
В периодичната таблица такъв химичен елемент като арсен заема позиция на границата метал-неметал. По своята активност той е между водорода и медта. Неметалният характер се проявява във факта, че той може да проявява степен на окисление -3 (AsH3 - арсин). Съединенията с положителна степен на окисление +3 имат амфотерни свойства, а със степен +5 се проявяват киселинните му свойства. Какво е арсенов оксид?

Оксиди и хидроксиди
Съществуват следните арсенови оксиди: As2O3 и As2O5. Съществуват и съответните хидроксиди:
- Метаарсенова киселина HAsO2.
- Ортоарсенова киселина H3AsO3.
- Метаарсенова киселина HAsO3.
- Ортоарсенова киселина H3AsO4.
- Пироарсенова киселина H4As2O7.

Какво е арсенов триоксид?
Арсенът образува два оксида, от които As2O3 се нарича триоксид. Това е вещество, което често се използва за медицински цели, но не е точно безвреден химикал. Това е неорганично съединение, което е основният източник на органоарсенови съединения (съединения, съдържащи химична връзка с въглерод) и много други. Много употреби на As2O3 са спорни поради токсичния характер на елемента. Търговското наименование на това съединение е Trisenox.
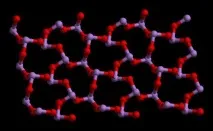
Обща информация за триоксида
Химическата формула на арсеновия триоксид е As2O3. Молекулното тегло на това съединение е 197,841 g/mol. Има много начини за получаване на този оксид. Един от тях е печенето на сулфидна руда. Химическата реакция протича по следния начин:
Повечето оксиди могат да бъдат получени като страничен продукт от обработката на други руди.Арсенопиритът е често срещан примес в златото и медта и отделя арсенов триоксид при нагряване в присъствието на въздух. Това може да доведе до сериозно отравяне.

Структура на арсенов триоксид
Арсеновият триоксид има формула As4O6 в течна и газова фаза (под 800°C). В тези фази той е изоструктурен с фосфорния триоксид (P4O6). Но при температури над 800°C As4O6 се разпада до молекулен As2O3. В тази фаза той е изоструктурен с диизотрон триоксид (N2O3). В твърдо състояние това съединение показва полиморфна способност (способността да съществува в две или повече форми на кристална структура).
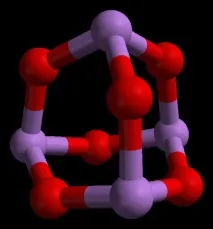
Свойства на арсеновия триоксид
Някои от основните свойства на арсеновия триоксид са следните:
- Триоксидните разтвори образуват слаби киселини с вода. Това е така, защото съединението е амфотерен арсенов оксид.
- Разтворим е в алкални разтвори и дава арсенати.
- Арсеновият триоксид има висока разтворимост в солна киселина (HCl) и накрая дава арсенов трихлорид и концентрирана киселина.
- Той дава пентоксид (As2O5) в присъствието на силни окислители като водороден прекис, озон и азотна киселина.
- Той е почти неразтворим в органични разтворители.
- Изглежда като бяло твърдо вещество в нормалното си физическо състояние.
- Има точка на топене 312,2°C и точка на кипене 465°C.
- Плътността на това вещество е 4,15 g/cm 3 .
Използването на арсенов триоксид в медицината
Този химикал принадлежи към класа противоракови лекарства и се използва при лечението на рак. Токсичността на арсена е добре известна. Но арсеновият триоксид е химиотерапевтиклекарство и се използва за лечение на определени видове рак в продължение на много години. Разтворът, използван за тази обработка, се нарича решение на Фаулър. През 1878 г. Бостънската градска болница съобщава, че това решение може да бъде ефективно за понижаване на броя на белите кръвни клетки на човек.
В резултат на това As2O3 се използва главно за лечение на левкемия, докато не бъде заменен от лъчева терапия. Но след 30-те години на миналия век, той бавно възвръща своята популярност при лечението на левкемия, до появата на съвременната химиотерапия. Този арсенов оксид се счита за най-доброто лечение за хронична миелогенна левкемия. Дори днес това вещество се използва за лечение на специфичен тип остра промиелоцитна левкемия след неуспешна ретиноидна или антрациклинова химиотерапия. Използва се и за лечение на хронична миелоидна левкемия, мултиплен миелом, остра миелоидна левкемия, лимфом, рак на лимфната система.

Използването на триоксид
Арсеновият триоксид се използва широко в производството на безцветно стъкло. Това съединение е полезно и в областта на електрониката за производство на полупроводници и някои сплави. Използва се и в боите. Арсеновият триоксид може да бъде ефективно лечение на мозъчни тумори.
В миналото това вещество се е използвало в стоматологията, но тъй като е силно токсично съединение, използването му от съвременните зъболекари е преустановено. Арсеновият оксид (формула As2O3) също се използва като консервант за дърво, но такива материали са забранени в много части на света. В комбинация с меден ацетат арсеновият триоксид дава яркозелен пигмент.
силно токсично вещество
Сам по себе си триоксидът има висока степен на токсичност.Следователно винаги е необходимо да се вземат необходимите предпазни мерки, преди да се използва. Може да бъде много опасно в следните случаи:
- Храня се. Ако As2O3 случайно попадне в храносмилателния тракт, трябва незабавно да се консултирате с лекар. Не се препоръчва да се опитвате да предизвикате повръщане, преди да потърсите лекарска помощ. Необходимо е да свалите всички тесни дрехи, да свалите вратовръзка, да разкопчаете яка, колан и др.
- Контакт с кожата. В случай на контакт с която и да е повърхност на тялото, незабавно изплакнете засегнатата област обилно с вода. Замърсеното облекло и обувки трябва да се свалят незабавно и да се изперат преди повторна употреба. В случай на сериозен контакт с кожата, трябва незабавно да потърсите медицинска помощ. Измиването на заразената зона с дезинфекционен сапун и нанасянето на антибактериален крем може да бъде полезно.
- Зрителен контакт. Ако As2O3 влезе в контакт с очите, първото нещо, което трябва да направите, е да свалите всички контактни лещи и да изплакнете очите обилно с вода в продължение на 15 минути. Препоръчително е да използвате студена вода. Успоредно с това някой трябва да повика линейка.
- Вдишване. Хората, които са вдишали този газ, трябва да бъдат поставени на друго място с чист въздух. Трябва също да потърсите незабавна медицинска помощ. Ако дишането е затруднено, незабавно трябва да се приложи кислород. Ако пострадалият не може да диша сам, трябва да се направи изкуствено дишане.
- Това съединение може да бъде токсично за хората. Ако в тялото попадне прекомерно количество арсенов триоксид, това може дори да доведе до смърт. Винаги трябва да се използват предпазни очила и ръкавици при работа с As2O3. Работата винаги трябва да се извършва вдобре проветриво помещение.

Странични ефекти
Честите нежелани реакции на това вещество включват симптоми като:
- слаб апетит;
- повръщане;
- гадене;
- болка в корема;
- запек;
- главоболие;
- умора;
- световъртеж;
- треска;
- проблеми с дишането;
- високо ниво на левкоцити;
- висока кръвна захар;
- кожен обрив.
По-рядко срещаните нежелани реакции включват:
- суха уста;
- хаотично дишане;
- болка в гърдите;
- ниско ниво на левкоцити;
- болка в мускулите и костите;
- подуване на лицето и очите;
- диария;
- тремор;
- ниска кръвна захар;
- ниски нива на кислород в кръвта.
Редки нежелани реакции на As2O3:
- неправилен сърдечен ритъм (това може да доведе дори до смърт);
- качване на тегло;
- припадък;
- разсейване;
- кома;
- подут корем;
- потъмняване на кожата.
Животозастрашаващи симптоми на излагане на арсенов триоксид са наддаване на тегло, треска, затруднено дишане, задух, болка в гърдите, кашлица.
Арсеновият триоксид е силно токсично вещество, което може дори да доведе до смърт. Въпреки това, той има своята полза в областта на медицината. Винаги трябва да се вземат предпазни мерки.
химична реакция
Арсеновият триоксид е амфотерен висш арсенов оксид и неговите водни разтвори са леко кисели. По този начин той лесно се разтваря в алкални разтвори за получаване на арсенати. Той е по-малко разтворим в киселини, с изключение на солната.
Само със силнитеокислители като озон, водороден пероксид и азотна киселина, той образува арсенов пентаоксид с +5 степен на киселинност As2O5. По отношение на стабилността на окисление, арсеновият триоксид е различен от фосфорния триоксид, който лесно се запалва до фосфорен пентоксид. Редукцията дава елементарен арсен или арсин (AsH3).

Арсенов пентоксид
Химическата формула на пентоксида е As2O5. Моларната му маса е 229,8402 g/mol. Представлява бял хигроскопичен прах с плътност 4,32 g/cm3. Точката на топене достига 315°C, при която започва да се разлага. Веществото има добра разтворимост във вода и алкохол. Свойствата на арсеновия оксид го правят силно токсичен и опасен за околната среда. Това е неорганично съединение, което е по-рядко срещано, силно токсично и следователно само с ограничена търговска употреба, за разлика от висшия арсенов оксид (формула As2O3).
Арсенът е известен предимно като отрова и канцероген. Неговият триоксид е водоразтворим прах, който произвежда разтвор без цвят, вкус и мирис. Това е бил популярен метод за убиване през Средновековието. Използването му продължава и днес, но за мирни цели и в малки количества.