Получаване на алуминиев оксид от руди
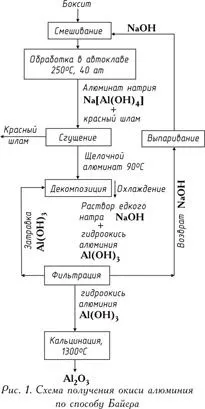
Същността на метода се състои в това, че алуминиевите разтвори бързо се разлагат, когато в тях се въведе алуминиев хидроксид, а разтворът, останал от разлагането след изпаряването му при условия на интензивно смесване при 169-170 ° C, може отново да разтвори алуминиевия оксид, съдържащ се в бокситите. Този метод се състои от следните основни операции:
1). Приготвяне на боксит, което се състои в неговото раздробяване и смилане в мелници; мелниците се доставят с боксит, каустик алкали и малко количество вар, което подобрява отделянето на Al2O3; получената целулоза се подава за излугване;
2). Излугване на боксит (напоследък използваните досега автоклавни блокове с кръгла форма са частично заменени от тръбни автоклави, в които излугването се извършва при температури от 230-250 ° C (500-520 K), което се състои в неговото химично разлагане от взаимодействие

силициевият диоксид, съдържащ се в боксита, взаимодейства с алкали и преминава в разтвор под формата на натриев силикат:
в разтвор натриевият алуминат и натриевият силикат образуват неразтворим натриев алумосиликат; титанови и железни оксиди преминават в неразтворимия остатък, придавайки на остатъка червен цвят; този остатък се наричачервена кал. След завършване на разтварянето, полученият натриев алуминат се разрежда с воден разтвор на основа, докато температурата се понижава със 100°C;
3). Отделяне на алуминатен разтвор от червена кал, обикновено се извършва чрез промиване в специални сгъстители; в резултат на това червената кал се утаява, а алуминатният разтвор се отцежда и след това се филтрира (избистря). В ограничени количества утайката се използва например като добавка към цимента. В зависимост от класа на боксита, 0,6-1,0 тона червена кал (сух остатък) на 1 тон получен алуминиев оксид;
4). Разлагане на алуминатен разтвор. Филтрира се и се изпомпва в големи контейнери с бъркалки (разлагатели). Алуминиевият хидроксид Al(OH)3 се екстрахира от пренаситен разтвор при охлаждане до 60°C (330 K) и постоянно разбъркване. Тъй като този процес протича бавно и неравномерно и образуването и растежът на кристали от алуминиев хидроксид са от голямо значение при по-нататъшната му обработка, голямо количество твърд хидроксид се добавя към разлагащите вещества - семена:

6). Дехидратация на алуминиев хидроксид (калциниране); това е крайната операция на производството на алуминиев оксид; извършва се в тръбни въртящи се пещи, а напоследък и в пещи с турбулентно движение на материалапри температура 1150-1300 о С; суров алуминиев хидроксид, преминаващ през ротационна пещ, изсушен и дехидратиран; при нагряване се извършват последователно следните структурни трансформации:
| Al(OH)3→AlOOH→ γ-Al2O3→ α-Al2O3 | ||
| 200 около С– | 950 около C– | 1200 около С. |
Крайният калциниран двуалуминиев оксид съдържа 30-50% α-Al2O3 (корунд), останалото е γ-Al2O3.
Този метод извлича 85-87% от целия произведен алуминиев оксид. Полученият алуминиев оксид е силно химично съединение с точка на топене 2050 o C.

Електролиза на алуминиев оксид
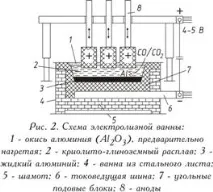
а) самоизпичащи се аноди Zederberg, състоящи се от брикети, така наречените "хлябове" от масата Zederberg (ниско пепелни въглища с 25-35% каменовъглен катран), пълнени в алуминиева обвивка; под действието на висока температура анодната маса се изпича (синтерира);
б) изпечени или "непрекъснати" аноди от големи въглеродни блокове (например 1900 × 600 × 500 mm, тежащи около 1,1 тона).
Сила на тока на електролизерие 150 000 А. Те се свързват към мрежата последователно, т.е. получава се система (серия) - дълъг ред електролизатори.
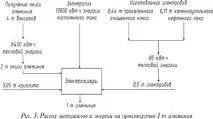
Работното напрежение на банята, което е 4-5 V, е много по-високо от напрежението, при което се разлага алуминиевият оксид, тъй като загубите на напрежение в различни части на системата са неизбежни по време на работа. Балансът на суровините и енергията при производството на 1 тон алуминий е показан на фиг. 3.

Редукция на алуминиев хлорид с манган (метод на Тот)

За алуминия не е възможно рафиниране на електролиза с разлагане на водни солеви разтвори. Тъй като за някои цели степента на пречистване на промишления алуминий (Al 99.5 - Al 99.8), получен чрез електролиза на стопилка от криолит-алуминий, е недостатъчна, дори по-чист алуминий (Al 99, 99 R) се получава от промишлен алуминий или метални отпадъци чрез рафиниране. Най-известният метод за рафиниране етрислойна електролиза.
Трислойно рафиниране чрез електролиза
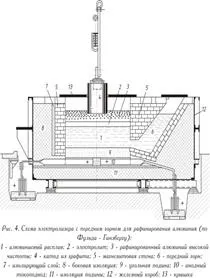
Облечена в стоманен лист, работеща на постоянен ток (показана на Фиг. 4 - виж по-горе), рафиниращата вана се състои от въглищна камина с токопроводи и топлоизолираща магнезитна облицовка. За разлика от електролизата на стопилка от криолит-алуминиев оксид, тук анодът обикновено е разтопен рафиниран метал (долен аноден слой). Електролитът се състои от чисти флуориди или смес от бариев хлорид и алуминиев и натриев флуорид (среден слой). Алуминият, който се разтваря от анодния слой в електролита, се отделя над електролита (горния катоден слой). Чистият метал служи като катод. Токът се подава към катодния слой от графитен електрод.
Ваната работи при 750-800°C, консумацията на енергия е 20 kWh на 1 kg чист алуминий, т.е. малко по-висока, отколкото при конвенционалната електролиза на алуминий.
Анодният метал съдържа 25-35% Cu; 7-12% Zn; 6-9% Si; до 5% Fe и малко количество манган, никел, олово и калай, останалото (40-55%) е алуминий. Всички тежки метали и силиций остават в анодния слой по време на рафинирането. Наличието на магнезий в електролита води до нежелани промени в състава на електролита или до неговото силно зашлаковане. За отстраняване на магнезий шлаките, съдържащи магнезий, се обработват с флюсове или газообразен хлор.

Рафинираният алуминий обикновено има следния състав, %: Fe 0,0005-0,002; Si0,002-0,005; Cu 0,0005-0,002; Zn 0,0005-0,002; Mg следи; Ал почивка.
Рафинираният алуминий се преработва в полуготов продукт в определения състав или се легира с магнезий (виж таблица 1.2.).

| марка | Номер | Допустими примеси*, % | ||||||
| Обща сума | включително | |||||||
| Si | Fe | Ти | Cu | Zn | други | |||
| A199,99R | 3,0400 | 0,01 | 0,006 | 0,005 | 0,002 | 0,003 | 0,005 | 0,001 |
| A199.9H | 3,0300 | 0,1 | 0,050 | 0,035 | 0,006 | 0,005 | 0,04 | 0,003 |
| A199.8H | 3,0280 | 0,2 | 0,15 | 0,15 | 0,03 | 0,01 | 0,06 | 0,01 |
| A199.7H | 3,0270 | 0,3 | 0,20 | 0,25 | 0,03 | 0,01 | 0,06 | 0,01 |
| A199.5H** | 3,0250 | 0,5 | 0,30 | 0,40 | 0,03 | 0,02 | 0,07 | 0,03 |
| A199H | 3,0200 | 1.0 | 0,5 | 0,6 | 0,03 | 0,02 | 0,08 | 0,03 |
| * Доколкото е възможно да се определи чрез конвенционални методи на изследване. ** Чистият алуминий за електротехниката (алуминиеви проводници) се доставя под формата на първичен алуминий 99,5, съдържащ не повече от 0,03% (Ti + Cr + V + Mn); обозначен в този случай като E-A1, номер на материала 3.0256. В противен случай отговаря на VDE-0202. |
Рафиниране чрез органоалуминиеви комплексни съединения изоново топене

Този тип рафинираща електролиза, използван първоначално само в лабораторен мащаб, вече се извършва в малък индустриален мащаб - произвеждат се няколко тона метал годишно. Номиналната степен на пречистване на получения метал е 99,999-99,9999%. Потенциалните области на приложение на метал с такава чистота са криогенната електротехника и електрониката.
Възможно е да се използва разглежданият метод за рафиниране в галванопластиката.
Още по-висока чистота - номинално до A1 99.99999 - може да се получи чрез последващо зоново топене на метала. При преработката на алуминий с висока чистота в полуготов продукт, лист или тел е необходимо, предвид ниската температура на рекристализация на метала, да се вземат специални предпазни мерки. Забележително свойство на рафинирания метал е неговата висока електропроводимост в областта на криогенните температури.
Не намерихте това, което търсихте? Използвайте търсачката: