Статиновата терапия от гледна точка на клиничния фармаколог Лякишев А
*Импакт фактор за 2017 г. според RSCI
Списанието е включено в Списъка на рецензираните научни издания на ВАК.
Прочетете в новия брой
Български кардиологичен научно-производствен комплекс, Министерство на здравеопазването на Руската федерация, Москва
CЦелта на липидопонижаващата терапия при пациенти с коронарна артериална болест епонижаване и поддържане на липопротеините с ниска плътност (LDL) холестерол (CHS) под 100 mg/dL(вижте Таблица Фармакокинетика и Фармакодинамика
За профилактика и лечение на атеросклероза са необходими лекарства, които се понасят добре при продължителна употреба. Известно е, чемонотерапията със статини е придружена от ниска честота на страничните ефекти (1-2%). Най-чести са диспептичните разстройства, по-рядко (при 0,1-1,0% от пациентите) се наблюдава кожен обрив и сърбеж. По време на лечението със симвастатин е възможно повишаване на нивото на аланин и аспарагинови трансаминази в кръвния серум (при приблизително 1% от пациентите). Ако тези показатели се повишат не повече от 3 пъти над горната граница на нормата и не са придружени от поява на клинични симптоми, не се изисква спиране на приема на статини. Още по-рядко нивото на креатин фосфокиназата се повишава, което може да бъде придружено от симптоми на миопатия и изисква спиране на лекарството поради риск от развитие на рабдомиолиза и бъбречна недостатъчност. Честотата на оттегляне на статини поради странични ефекти е по-малко от 2%.
Вероятността от лекарствени взаимодействия със статини се увеличава, когато едно лекарство променя фармакокинетиката или фармакодинамиката на друго лекарство. Статините са силно селективни инхибитори на HMG-CoA редуктазата и нямат значителен афинитет към други ензими или рецепторни системи. В тази връзка, на фармакодинамично ниво, статините не са склонни към лекарствавзаимодействия. Въпреки това, лекарствените взаимодействия могат да променят фармакокинетиката на статините, т.е. процесите на тяхното усвояване, разпределение, метаболизъм и екскреция.
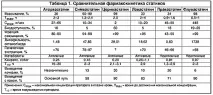
Всички статини се абсорбират бързо след перорално приложение (от 30 до 98%), като максималната концентрация в кръвта се постига в рамките на 0,5-4 часа. Храненето не повлиява значително абсорбцията на симвастатин и церивастатин, повишава концентрацията на ловастатин в кръвта и намалява бионаличността на други статини. Липидопонижаващото действие на статините не зависи значително от приема им по време на хранене или през нощта. С изключение на церивастатин, всички лекарства от тази група се характеризират с интензивна екстракция при първото преминаване през черния дроб.
Всички статини се абсорбират бързо след перорално приложение (от 30 до 98%), като максималната концентрация в кръвта се постига в рамките на 0,5-4 часа. Храненето не повлиява значително абсорбцията на симвастатин и церивастатин, повишава концентрацията на ловастатин в кръвта и намалява бионаличността на други статини. Липидопонижаващото действие на статините не зависи значително от приема им по време на хранене или през нощта. С изключение на церивастатин, всички лекарства от тази група се характеризират с интензивна екстракция при първото преминаване през черния дроб.
След абсорбция от стомашно-чревния тракт до 85% от лекарството се поема от черния дроб и само 5% от активните метаболити влизат в системното кръвообращение. Хипохолестеролемичният ефект се появява след 3 дни от началото на лечението, когато се установи стабилна концентрация на лекарството в кръвта. Максимален ефект се постига след 4-6 седмици. Общият плазмен холестерол се връща към изходното ниво 1 месец след оттеглянето на максималните дози от лекарството. Терапевтичният ефект е доста стабилен,явленията на тахифилаксия при продължително лечение не се наблюдават.
С изключение на правастатин, всички статини са почти напълно свързани с плазмените протеини, главно албумин. Следователно ефектът на активните, несвързани форми на статини върху периферните тъкани е изключително малък. Чернодробна екстракция на статини над 70%. Лекарствените взаимодействия, дължащи се на изместване на статините от връзката им с протеини, са с ограничено значение. Действието на статините се развива бавно, така че временните колебания в концентрацията на несвързаните форми не са значими [23].
След абсорбция всички статини претърпяват значителна биохимична трансформация в черния дроб, което води до тяхната ниска системна бионаличност. Така лактоновите пръстени на ловастатин и симвастатин се хидролизират в хепатоцитите до отваряне на активни форми. Друг път на чернодробна трансформация на повечето статини в активни метаболити е чрез микрозомалния цитохром Р450 (CYP) изоензим 3A4, докато флувастатин се метаболизира с 50-80% чрез изоензима CYP2C9 (Таблица 2).

Много лекарствени взаимодействия със статини са резултат от потискане или индуциране на цитохром Р450 изоензими, които метаболизират повече от половината от всички лекарства, използвани в клиничната практика [24]. Конкуренцията с други лекарства на ниво ензимни реакции може да доведе до повишаване на концентрацията на статини в кръвта и появата на странични ефекти [25]. Интересното е, че същият ефект се причинява от сок от грейпфрут (повече от 1 чаша на ден) [26]. Описани са случаи на развитие на миозит, когато статините се комбинират с лекарства като фибрати; никотинова киселина; имуносупресори (циклоспорин А) при пациенти след сърдечна или бъбречна трансплантация; имидазолови производни,използвани за лечение на гъбични заболявания (кетоконазол, итраконазол) [27, 28]; някои антибиотици от класа на макролидите, особено еритромицин [29]; антидепресанти [30]. Особено поучителна е историята на новия калциев антагонист мибефрадил, който беше забранен през 1998 г. малко след като започна да се използва в клиниката поради увеличаване на случаите на рабдомиолиза при комбиниране със симвастатин (19 случая) и ловастатин (1 случай).
Има данни за увеличаване на протромбиновото време и риска от кървене при пациенти, приемащи индиректни антикоагуланти по време на лечение с ловастатин и флувастатин. В тези случаи за постигане на подходящ антикоагулантен ефект се използват по-малки дози антикоагуланти, по-често проследяване на параметрите на кръвосъсирването. Статините не влияят върху фармакокинетиката на лекарства като b-блокери, диуретици, сърдечни гликозиди, нестероидни противовъзпалителни средства. Лечението със статини се препоръчва временно да се спре при всеки пациент с остри инфекции, големи операции, травми, тежки метаболитни нарушения. Когато спрете приема на статини, няма синдром на отнемане.
Статините се предписват 1 или 2 пъти на ден. Началната доза се повишава на всеки 4 седмици, ако не се достигне желаното ниво на общия плазмен холестерол (по-малко от 5,2 mmol / l). Дозата на лекарството трябва да се намали, когато общият холестерол падне под 3,0 mmol / l (130 mg / dl). Поддържащото лечение със статини трябва да се провежда дълго време (години), ако лекарят очаква да забави прогресията на атеросклерозата или да доведе до нейното обръщане.
Противопоказания за назначаването на статини са активни патологични процеси в черния дроб, първоначално повишени нива на чернодробните ензими (повече от 50% над норматастойности), индивидуална непоносимост към лекарството, бременност и кърмене.
За да се гарантира безопасността на лечението, се изисква биохимичен мониторинг ежемесечно по време на периода на избор на доза (първите 2-3 месеца), по време на поддържаща терапия, биохимичен кръвен тест - 1 път на 3 месеца. Необходимо е по-внимателно проследяване на функционалното състояние на черния дроб при пациенти, които консумират значително количество алкохол.
Статините могат да забавят скоростта на развитие на атеросклерозата, да намалят риска от исхемични лезии на жизненоважни органи, сърдечно-съдови и обща смъртност. Показано е, че пациенти с коронарна артериална болест или други клинични прояви на атеросклероза намаляват и постоянно поддържат общия холестерол на ниво
Референтният списък може да бъде намерен на http://www.rmj.ru
Холетар (търговско име)
Литература:1. Wood D., Durrington P.N., Poulter N. et al. Съвместни британски препоръки за превенция на коронарна болест на сърцето в клиничната практика от името на Британското кардиологично дружество, Британската асоциация по хиперлипидемия, Британското дружество по хипертония и одобрени от Британската диабетна асоциация. Heart, 1998, 80 (Допълнение 2): S1 - S29.
2. Скандинавска група за проучване на оцеляването на симвастатин. Рандомизирано проучване за понижаване на холестерола при 4444 пациенти с коронарна болест на сърцето: скандинавското проучване за оцеляване на симвастатин (4S). Lancet, 1994, 344: 1383 - 1389.
3. Sacks F.M., Pfeffer M.A., Moye L.A. и др. Ефектът на правастатин върху коронарните събития след миокарден инфаркт при пациенти със средни нива на холестерол. Н. англ. J. Med., 1996, 335: 1001-1009.
4. Проучвателна група за дългосрочна интервенция с правастатин при исхемична болест (LIPID). Предотвратяване на сърдечно-съдови инциденти и смърт справастатин при пациенти с коронарна болест на сърцето и широк диапазон от начални нива на холестерол. Н. АНГЛ. J. MED., 1998, 339: 1349 - 1357.
5. Shepherd J., Cobble S.M., Ford J. et al. Профилактика на коронарна болест на сърцето с правастатин при мъже с хиперхолестеролемия. Н. англ. J. Med., 1995, 333: 1301 - 1307.
6. Grundy S.M. Консенсусно становище: ролята на терапията със статини при пациенти с хипертриглицеридемия. Am. J. Cardiol., 1998, 81 (Допълнение 4A): 1B - 6B.
7. Bakker-Arkema R.G., Davidson M.H., Goldstein J.L. et al. Ефикасност и безопасност на нов HMG-CoA редуктазен инхибитор, аторвастатин, при пациенти с хипертриглицеридемия. JAMA, 1996, 275: 128 - 133.
8. Illingworth D.R., Erkelens D.W., Keller U. et al. Определени дневни дози във връзка с хиполипидемичната ефикасност на ловастатин, правастатин и симвастатин. Lancet, 1994, 343: 1554 - 1555.
9. Дейвидсън М.Х. и др. Ефикасност и шестседмична поносимост на симвастатин 80 и 160 mg/ден. Am. J. Cardiol., 1997, 79: 38 - 42.
10. Изследователи на MAAS. Ефект на симвастатин върху коронарна атерома: Многоцентрово анти-атеромно изследване (MAAS). Lancet, 1994, 344: 633 - 638. [Erratum. Lancet, 1994, 344: 762].
11. Stein E.A., Lane M., Laskarzewski P. Ефект на статините върху нивото на триглицеридите. Am. J. Cardiol., 1998, 81 (Допълнение 4A): 27B - 31B.
12. O’Driscoll G., Green D., Taylor R.R. Симвастатин, инхибитор на HMG-CoA редуктазата, подобрява ендотелната функция в рамките на 1 месец. Circulation, 1997, 95: 1126 - 1131.
13. Белоста С., Бернини Ф., Фери Н. и др. Директни съдови ефекти на HMG-CoA редуктазните инхибитори. Atherosclerosis, 1998, 137 (Suppl.): S101 - S109.
14. Corsini A., Pazzucconi F., Arnaboldi L. et al. Директни ефекти на статините върху съдовата стена. Дж.Cardiovasc. Pharmacol., 1998, 31: 773 - 778.
15. Rosenson R.S., Tangney C.C. Антиатеротромботични свойства на статините. Последици за намаляване на сърдечно-съдовите инциденти. JAMA, 1998, 279: 1643 - 1650.
16. Lennernas H., Fager G. Фармакодинамика и фармакокинетика на HMG-CoA редуктазните инхибитори. Clin. Pharmacokinet., 1997, 32: 403 - 425.
17. Corsini A., Bellosta S., Baetta R. et al. Нови прозрения за фармакодинамичните и фармакокинетичните свойства на статините. Pharmacol. Ther., 1999, 84: 413 - 428.
18. Desager L.P., Horsmans Y. Клинична фармакокинетика на HMG-CoA редуктазните инхибитори. Clin. Pharmacokinet., 1996, 31: 348 - 341
19. Muck W. Рационалната оценка на профила на взаимодействие на цервастатин подкрепя неговата ниска склонност към лекарствени взаимодействия. Наркотици, 1998, 56 (Допълнение 1): 15 - 23.
20. Richter W.O., Jacob B.G., Schwandt P. Взаимодействие между фибри и ловастатин. Lancet, 1991, 338: 706.
21. Стърн Р.Х., Гибсън Д.М., Уитфийлд Л.Р. Циметидин не променя фармакокинетиката на аторвастатин или намаляването на LDL-холестерола. Евро. J. Clin. Pharmacol., 1998, 53: 475-478.
22. Стокли И.Х. Лекарствени взаимодействия. Лондон: Pharmaceutical Press. 1996 г.
23. Wrighton S.A., Vandenbranden M., Ring B.J. Човешкото лекарство, метаболизиращо цитохроми P450. J. Pharmacokinet. Biopharm., 1996, 24: 475 - 489.
24. Hamelin B.A., Turgeon J. Хидрофилност/липофилност: значение за фармакологията и клиничните ефекти на HMG-CoA редуктазните инхибитори. Тенденции Pharmacol. Sci., 1998, 19: 26 - 37.
25. Kantola T., Kivisto K.T., Neuvonen P.J. Фармакокинетика и разпределение на лекарствата. Сокът от грейпфрут значително повишава серумните концентрации на ловастатин. Clin. Pharmacol. Ther., 1998, 63: 397 - 403.
26.Kivisto K.T., Kantola T., Neuvonen P.J. Различни ефекти на итраконазол върху фармакокинетиката на флувастатин и ловастатин. бр. J.Clin. Pharmacol., 1998, 46: 49-53.
27. Lees R.S., Lees A.M. Рабдомиолиза от едновременното приложение на ловастатин и противогъбичния агент итраконазол. Н. англ. J. Med., 1995, 333: 664-665.
28. Аянян J.Z., Fuchs C.S., Stone R.M. Ловастатин и рабдомиолиза. Ан. Стажант. Med., 1988, 109: 682-683.
29. Jacobson R.H., Wang P., Glueck C.J. Миозит и рабдомиолиза, свързани с едновременната употреба на симвастатин и нефазодон. JAMA, 1997, 277: 296.
30. Schmassmann-Suhijar d., Bullingham R., Gasser R. et al. Рабдомиолиза, дължаща се на взаимодействие на симвастатин с мибефрадил. Lancet, 1998, 351: 1929 - 1930.