Генна терапия, списание Popular Mechanics

Мускулната дистрофия на Дюшен е едно от редките, но все пак относително често срещани генетични заболявания. Заболяването се диагностицира на възраст от три до пет години, обикновено при момчета, проявявайки се отначало само в трудни движения, до десетгодишна възраст човек, страдащ от такава миодистрофия, вече не може да ходи, до 20-22 години животът му завършва. Причинява се от мутация в гена за дистрофин, който се намира на X хромозомата. Той кодира протеин, който свързва мембраната на мускулната клетка с контрактилните влакна. Функционално това е вид пружина, която осигурява плавно свиване и целостта на клетъчната мембрана. Мутациите в гена водят до дистрофия на скелетната мускулна тъкан, диафрагмата и сърцето. Лечението на заболяването има палиативен характер и може само леко да облекчи страданието. С развитието на генното инженерство обаче има светлина в края на тунела.
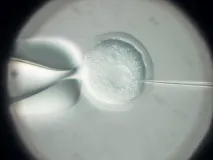
За войната и мира
Генната терапия е доставяне на конструкции на базата на нуклеинови киселини в клетките за лечение на генетични заболявания. С помощта на такава терапия е възможно да се коригира генетичен проблем на ниво ДНК и РНК чрез промяна на процеса на експресия на желания протеин. Например, ДНК с коригирана последователност може да бъде доставена в клетка, от която се синтезира функционален протеин. Или, обратно, възможни са делеции на определени генетични последователности, което също ще помогне за намаляване на вредните ефекти от мутацията. На теория това е просто, но на практика генната терапия се основава на най-сложните технологии за работа с микроскопични обекти и представлява набор от напреднали ноу-хау в областта на молекулярната биология.

„Генът на дистрофина, чиито мутации водят до мускулна дистрофия на Дюшен, е огромен“, казва Вадим Жерновков, директор по развитието на биотехнологичната компания Marlin Biotech, кандидат на биологичните науки. - Включва 2,5 милиона базови двойки, което може да се сравни с броя на буквите в романа "Война и мир". А сега си представете, че сме изтръгнали няколко важни страници от епоса. Ако на тези страници са описани значими събития, тогава разбирането на книгата вече би било трудно. Но с гена всичко е по-сложно. Не е трудно да се намери друго копие на „Война и мир“ и тогава липсващите страници биха могли да бъдат прочетени. Но генът на дистрофина се намира на X хромозомата, а мъжете имат само един. По този начин само едно копие на гена се съхранява в половите хромозоми на момчетата при раждането. Няма другаде да го вземеш.

И накрая, при протеиновия синтез от РНК е важно да се запази рамката за четене. Четящата рамка определя коя група от три нуклеотида се чете като кодон, който съответства на една аминокиселина в протеин. Ако има делеция в гена на ДНК фрагмент, който не е кратен на три нуклеотида, възниква изместване в рамката на четене - кодирането се променя. Това може да се сравни със ситуацията, когато след откъснати страници в цялата останала книга всички букви ще бъдат заменени със следващите по азбучен ред. Вземете абракадабра. Това е същото нещо, което се случва с протеин, който не е синтезиран правилно.
Ще може ли човек да живее до 1000 години: регенеративна медицина
Биомолекулен пластир
Един от ефективните методи на генната терапия за възстановяване на нормалния протеинов синтез е пропускането на екзон с помощта на къси нуклеотидни последователности. В "Марлин Биотек" вечее разработена технологията за работа с гена на дистрофина по този метод. Както е известно, в процеса на транскрипция (синтез на РНК) първо се образува т. нар. предматрична РНК, която включва както белтъчно-кодиращи области (екзони), така и некодиращи области (интрони). След това започва процесът на снаждане, по време на който интроните и екзоните се разделят и се образува "зряла" РНК, състояща се само от екзони. В този момент някои екзони могат да бъдат блокирани, „залепени“ с помощта на специални молекули. В резултат на това зрялата РНК няма да има тези кодиращи области, от които бихме предпочели да се отървем, и по този начин рамката за четене ще бъде възстановена, протеинът ще бъде синтезиран.
„Отстранихме грешки в тази технология in vitro“, казва Вадим Жерновков, тоест върху клетъчни култури, отгледани от клетки на пациенти с миодистрофия на Дюшен. Но отделните клетки не са организъм. Нахлувайки в процесите на клетката, трябва да наблюдаваме на живо последствията, но не е възможно да въвличаме хора в тестовете по различни причини – от етични до организационни. Следователно стана необходимо да се получи модел на мускулна дистрофия на Дюшен с определени мутации на базата на лабораторно животно.
Как да убодете микрокосмоса
Трансгенните животни са животни, получени в лаборатория, в генома на които са направени целенасочено, съзнателно промени. Още през 70-те години на миналия век става ясно, че създаването на трансгени е най-важният метод за изследване на функциите на гените и протеините. Един от най-ранните методи за получаване на напълно генетично модифициран организъм е инжектирането на ДНК в пронуклеуса („ядрения предшественик“) на зиготите на оплодените яйцеклетки. Това е логично, тъй като е най-лесно да се модифицира геномът на животно в самото начало на неговото развитие.
Инжектирането в ядрото на зиготата е много нетривиална процедура, защото говорим за микромащаби. Мишото яйце е с диаметър 100 µm, а пронуклеусът е 20 µm. Операцията се извършва под микроскоп с 400-кратно увеличение, но инжектирането е най-ръчната работа. Разбира се, за „инжекцията“ не се използва традиционна спринцовка, а специална стъклена игла с кух канал вътре, където се събира генният материал. Единият край може да се държи в ръка, а другият е ултра тънък и остър - практически невидим с просто око. Разбира се, такава крехка конструкция от боросиликатно стъкло не може да се съхранява дълго време, така че лабораторията разполага с набор от заготовки, които се изтеглят на специална машина непосредствено преди работа. Използва се специална система за клетъчно контрастно изобразяване без оцветяване - намесата в пронуклеуса е травматична сама по себе си и е рисков фактор за клетъчното оцеляване. Боята би била друг такъв фактор. За щастие яйцеклетките са доста издръжливи, но броят на зиготите, които пораждат трансгенни животни, е само няколко процента от общия брой яйцеклетки, които са били инжектирани с ДНК.
Следващата стъпка е хирургична. В ход е операция за трансплантация на микроинжектирани зиготи във фунията на яйцепровода на мишка реципиент, която ще стане сурогатна майка за бъдещи трансгени. След това лабораторното животно естествено преминава през цикъл на бременност и се ражда потомство. Обикновено в котилото има около 20% трансгенни мишки, което също показва несъвършенството на метода, тъй като тойима голям елемент на случайност. Когато се инжектира, изследователят не може да контролира точно как вмъкнатите ДНК фрагменти ще бъдат интегрирани в генома на бъдещия организъм. Има голяма вероятност от такива комбинации, които ще доведат до смъртта на животното в ембрионален стадий. Въпреки това методът работи и е доста подходящ за редица научни цели.

ДНК ножица
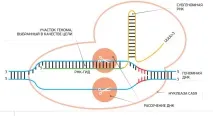
Но има по-ефективен начин, базиран на целево редактиране на генома с помощта на технологията CRISPR/Cas9. „Днес молекулярната биология донякъде прилича на ерата на морските експедиции на дълги разстояния под платна“, казва Вадим Жерновков. — Почти всяка година в тази наука има значими открития, които могат да променят живота ни. Например, преди няколко години микробиолозите откриха имунитет към вирусни инфекции в привидно отдавна изследван вид бактерии. В резултат на по-нататъшни изследвания се оказа, че бактериалната ДНК съдържа специални локуси (CRISPR), от които се синтезират РНК фрагменти, които могат допълнително да се свързват с нуклеинови киселини на чужди елементи, например ДНК или РНК на вируси. Протеинът Cas9, който е нуклеазен ензим, се свързва с такава РНК. РНК служи като ръководство за Cas9, маркирайки специфичен участък от ДНК, в който нуклеазата прави разрез. Преди около три до пет години се появиха първите научни статии, които разработват технологията CRISPR/Cas9 за редактиране на генома.

В сравнение с конструктния метод на случайно вмъкване, новият метод дава възможност да се изберат елементи от системата CRISPR/Cas9 по такъв начин, че точно да се насочат РНК водачите към желаните региони на генома и да се постигне целенасочено изтриване или вмъкване на желаната ДНК последователност. При този метод също са възможни грешки (насочващата РНК понякога се свързва с грешния сайт, към който е насочена), но при използване на CRISPR/Cas9 ефективността на създаване на трансгени вече е около 80%. „Този метод има широки перспективи не само за създаването на трансгени, но и в други области, по-специално в генната терапия“, казва Вадим Жерновков. „Технологията обаче е само в началото на своето пътуване и е доста трудно да си представим, че в близко бъдеще хората ще могат да коригират генния код на хора, използващи CRISPR/Cas9. Докато съществува възможност за грешка, съществува и опасност човек да загуби важна кодираща част от генома.

Млечно лекарство
Българската компания Marlin Biotech успя да създаде трансгенна мишка, в която мутацията, водеща до мускулна дистрофия на Дюшен, е напълно възпроизведена, а следващият етап ще бъде тестването на технологии за генна терапия. Създаването на модели на човешки генетични заболявания на базата на лабораторни животни обаче не е единственото възможно приложение на трансгените. И така, в България и западните лаборатории се работи в областта на биотехнологиите, които позволяват получаването на важни за фармацевтичната индустрия лекарствени протеини от животински произход. Кравите или козите могат да действат като производители, при които е възможно да се промени клетъчният апарат за производството на протеини, съдържащи се в млякото. От млякото е възможно да се извлече лечебен протеин, който се получава не по химичен метод, а с помощта на естественимеханизми, които повишават ефективността на лекарството. В момента са разработени технологии за получаване на такива медицински протеини като човешки лактоферин, проурокиназа, лизозим, атрин, антитромбин и др.