Методи за пречистване на вещества
МИНИСТЕРСТВО НА ОБРАЗОВАНИЕТО И НАУКАТА НА РУСКАТА ФЕДЕРАЦИЯ
ФЕДЕРАЛЕН ДЪРЖАВЕН БЮДЖЕТ
ВИСШЕ ПРОФЕСИОНАЛНО ОБРАЗОВАНИЕ
„Башкирски държавен педагогически
Университет на името на М. Акмула"
(FGBOU VPO BSPU на името на М. Акмула)
План на урока по темата:
"Методи за пречистване на вещества"
Изпълнение: Маркова Е.
Проверил: д.ф.н. Рашидова С.Т.
Методи за пречистване на вещества
Методите за пречистване и разделяне на вещества се основават на използването на техните различия в химичните и физичните свойства. Примери за такива методи на разделяне са прекристализация, сублимация и абсорбция.
Прекристализациятае метод за пречистване, основан на зависимостта на разтворимостта на веществата от температурата. Обикновено прекристализацията се свежда до разтваряне на вещество в подходящ разтворител при една температура и след това отделяне на кристална утайка при различна температура, когато разтворът стане пренаситен. Пренасищането на един солен разтвор може да се постигне и чрез добавяне на различни добавки, като алкохол.
Сублимация или сублимация- директно превръщане на твърдо вещество в пара (обикновено - при нагряване), заобикаляйки течното състояние. Впоследствие парата може да се кондензира в кристали върху охладената повърхност. Сублимацията винаги настъпва при температура под точката на топене на веществото. Способността да сублимират обикновено имат твърди вещества с молекулярна структура (йод, нафталин, амоняк, бензоена киселина). Пречистването чрез сублимация става възможно, когато примесите не са сублимирани.
Дестилацията или дестилациятае метод за пречистване, базиран на превръщането на течност в пара, последвано от кондензация на парата в течност. Методът обикновено се използва заотделяне на течност от разтворени твърди вещества или други нелетливи примеси. Не е възможно да се разделят компоненти с подобен капацитет на изпаряване с този метод.
Водата, получена в резултат на дестилация, се нарича дестилирана.
Методът на прекристализациясе основава на различната зависимост на разтворимостта на веществото и неговите замърсители от температурата. Прекристализацията се извършва, както следва: при повишена температура (60 °C) се приготвя наситен разтвор на веществото, което трябва да се пречисти, полученият разтвор се филтрува през гореща филтрационна фуния за отстраняване на неразтворимите примеси, след което разтворът се охлажда. С понижаване на температурата разтворимостта на веществото намалява и основната част от пречистеното вещество се утаява. Примесите остават в разтвора, тъй като полученият разтвор остава ненаситен по отношение на тях. Получените кристали се филтрират. Методът ви позволява да пречиствате вещества, които са разтворими във вода, например: натриев хлорид, амониев хлорид, калиев дихромат, меден сулфат и др.
Методът на сублимация (сублимация)се използва за пречистване на твърди вещества, които при нагряване могат да преминат от твърдата фаза директно в газа, заобикаляйки течната фаза. Полученият газ кондензира в охладената част на устройството. Дестилацията се извършва при температура, близка до точката на топене на веществото. Пречистването е възможно само от примеси, които не са способни на сублимация. Методът ви позволява да пречиствате вещества, които могат да сублимират, например: йод, сяра, амониев хлорид и др.
Опит 2.1. Пречистване на йод чрез сублимация
1. 0,3 g кристален йод и 0,1 g калиев йодид се претеглят на технохимични везни и се поставят в термоустойчива чаша за сублимация.
2. Стъклото се покрива с облодънна колба със студена вода.
3.Стъклото внимателно се нагрява на електрическа печка на течение. Наблюдава се появата на виолетови пари и отлагането на йод по стените на облодънна колба.
4. След завършване на сублимацията, нагряването се спира, йодните кристали се прехвърлят внимателно върху предварително претеглената хартия.
5. Определя се масата на йод, получен чрез сублимация. Оказа се, че е равно на 0,23 g.
6. Определихме практическия добив на йод по време на пречистването по формулата:
Йодът се пречиства чрез сублимация. Практическият добив на пречистен йод беше
Опит 2.2. Пречистване на вода чрез дестилация
Фигура 1. Апарат за дестилация
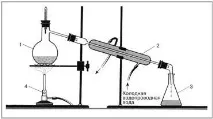
1. Сглобихме блок за дестилация на вода, чиято диаграма е показана на фигура 1
1 - Wurtz колба с пречистена вода;
3 - хладилник Liebig;
4 - приемник за дестилирана течност
5 - студена вода от водопровода;
6 - изтичане на охлаждаща вода
2. Загрейте водата в Wurtz колбата до кипене.
3. Изхвърлете първите порции дестилирана вода.
4. Съберете 20 ml дестилирана вода в конична колба.
5. Проведено изпаряване върху чаша дестилирана вода и обикновена чешмяна вода. Установено е, че при изпаряване на чешмяната вода остава сух остатък (бяло покритие), което показва наличието на примеси в нея. Когато дестилираната вода се изпари, не се образува остатък.
Водата се пречиства чрез дестилация. Установено е, че в дестилираната вода няма примеси от нелетливи вещества.
Опит 2.3. Пречистване на въглероден диоксид
За получаване на въглероден диоксид се използва апарат на Kipp, оборудван с парчета мрамор и 20% солна киселина. Образуването на CO2 става съгласно реакцията:
CaCO3(твърд) + 2HCl(aq) CaCl2(aq) + CO2(газ) + H2O
Катопримесите към основния продукт могат да бъдат водна пара и хлороводород.
1. Газът, получен в апарата на Кип, преминава през вода в епруветка за 2 минути.
2. Проверихме наличието на хлоридни йони в получения разтвор с разтвор на сребърен нитрат. Наблюдава се поява на мътност, което показва образуването на AgCl. Този резултат потвърждава наличието на HCl в газообразните реакционни продукти.
3. Газът, произведен в апарата, беше прекаран през тръба от калциев хлорид, пълна с безводен меден (II) сулфат. Наблюдава се синьо оцветяване на твърдото вещество, което показва наличието на водна пара в газообразните реакционни продукти.
4. Сглобихме инсталацията за получаване на чист въглероден диоксид по схемата, показана на фигура 2.
5. Отсъствието на примеси HCl и H2O в получения въглероден диоксид беше експериментално потвърдено.
Експеримент 2.4 Пречистване на твърди вещества.
Цел на лабораторната работа: чрез прекристализация да се получиmg чист калиев дихромат. Стойносттаmсе дава от учителя на всеки ученик. Преди извършване на лабораторна работа е необходимо да се извършат предварителни изчисления.
Предварителни изчисления (пример при m = 10 g):
Необходимо е да се изчисли количеството сол (в g) и вода (в ml), които ще са необходими за получаване на 10 g чисто вещество. Прекристализацията се извършва чрез нагряване до 60 °C и охлаждане на разтвора до 20 °C.
1. Използвайки референтната литература, според таблицата за разтворимост на солта при различни температури, ние определяме разтворимостта на калиев дихромат при 20 ° C и при 60 ° C. Разтворимостта при 20 °C е 11,1 g сол на 100 g разтвор, при 60 °C - 31,2 g на 100 g разтвор.
2. Изчислете количеството сол, с което може да се получиохлаждане до 20 ° C 100 g разтвор, наситен при 60 ° C: при 60 ° C наситеният разтвор съдържа 31,2 g сол и 68,8 g вода (100 - 31,2), когато този разтвор се охлади до 20 ° C, количеството вода ще остане непроменено - 68,8 g и 31,2 g сол ще бъдат разпределени между разтвора, наситен при 20 ° С и утайката. Определете количеството сол, което ще остане в разтвора. При 20 °C 100 g наситен разтвор съдържа 11,1 g сол и 88,9 g вода. Да направим пропорция:
11,1 g сол ще се разтвори в 88,9 g вода,
След товаmg сол се разтваря в 68,8 g вода
(G);
така че решението ще има:
Така, когато се охлади до 20 ° C, 100 g разтвор, наситен при 60 ° C, съдържащ 31,2 g сол и 68,8 g вода, се образува 22,6 g утайка (чиста сол).
3. Изчислете количеството сол и вода, необходими за получаване на 10 g чиста сол. Нека направим пропорции:
ако вземете 31,2 g сол, се образува 22,6 g утайка,
ако вземемm1 g сол, се образуват 10 g утайка, тогава
(G);
ако вземете 68,8 g вода, се образуват 22,6 g утайка,
ако вземемm2 g вода, тогава се образуват 10 g утайка
(G).
Нека изчислим обема на водата. Плътността на водата е 1 g/ml, следователно:
(ml).
По този начин, за да се получат 10 g чиста сол, е необходимо да се вземат 13,8 g калиев дихромат и 30,4 ml вода. Добавяме 10% към масата на солта, като вземем предвид масата на съдържащите се примеси:
m(соли) = 13.8 + 0.1 13.8 = 15.2 (g).
Работна поръчка
1. Налейте в чаша изчисленото количество вода, измерено с градуиран цилиндър.
2. Претеглете изчисленото количество сол на везната.
3. Стрийте солта в порцеланово хаванче.
4. Поставете смляната сол в чаша вода и загрейте разтворапочти до кипене на електрически котлон с азбестова мрежа, като се разбърква със стъклена пръчица.
5. Полученият разтвор се филтрува през нагънат филтър с помощта на гореща филтърна фуния за отстраняване на неразтворимите примеси.
6. Охладете получения разтвор до 20 °C.
7. Утаените кристали се филтрират през предварително претеглен филтър.
8. Разтворете няколко кристала от получената сол в 2 ml дестилирана вода и добавете 1–2 капки разтвор на сребърен нитрат, за да определите наличието на хлориди.
9. Разтворете няколко кристала от получената сол в 2 ml дестилирана вода и добавете 1–2 капки разтвор на бариев хлорид, за да определите наличието на сулфати.
10. Ако се образуват утайки от сребърен хлорид и / или бариев сулфат, тогава извършваме повторна прекристализация, като предварително сме изчислили количеството вода, необходимо за приготвяне на разтвор, наситен при 60 ° C, съдържащ получената маса сол.
11. Прекристализиран чист калиев дихромат върху филтъра се поставя в порцеланова чаша и се изсушава в пещ при 60 ° C до постоянно тегло (претеглянето се извършва на всеки 15-20 минути, ако след 2 претегляния масата не се е променила, тогава солта се изсушава).
12. Определете масата на получената сол, като извадите масата на филтъра от масата на солта с филтъра.